3.4.2 Электрохимические производства
Электролизом называется окислительно-восстановительная реакция, протекающая при пропускании постоянного электрического тока через расплав или раствор электролита.
Сущность электролиза заключается в следующем: при пропускании электрического тока через расплав или раствор электролита положительные ионы электролита (ионы металлов или водорода) притягиваются катодом, а отрицательные ионы (кислотные остатки или гидроксильные группы) - анодом. Приносимые к катоду от источника тока электроны присоединяются к положительным ионам электролита, восстанавливая их. Одновременно отрицательные ионы электролита отдают свои электроны аноду, от которого они двигаются к источнику тока. Теряя свои электроны, они окисляются в нейтральные атомы или группы атомов. Таким образом, у катода протекает процесс восстановления, а у анода - процесс окисления.
А (+): nA n - - ne - → nA p -
K (-): nB n + + ne - → nB p +
Оба процесса образуют единую окислительно-восстановительную реакцию. Но в отличие от обычных окислительно-восстановительных реакций электроны от восстановителя к окислителю переходят не прямо, а посредством электрического тока. Катод, приносящий электроны, является восстановителем, а анод, уносящий их,- окислителем.
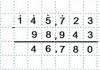
Основными показателями электрохимических производств являются выход по току, степень использования энергии. Расходный коэффициент по энергии, напряжение, приложенное к электролизеру, и др. Большинство вычислений основано на законе Фарадея, согласно которому масса вещества, выделившегося при электролизе пропорционально силе тока I, времени электролиза t и электрохимическому эквиваленту этого вещества Э Э
Масса вещества вычисляется по формуле
где, I - сила тока, F – постоянная Фарадея (96500 Кл)
(г-экв) (1.3.2)
Mr – относительная молекулярная масса вещества,
n – заряд иона (абсолютное значение) в виде которого вещество находится в растворе или в расплаве (т.е. количество отданных или принятых электронов).
Выход по току определяется отношением массы вещества, выделившегося при электролизе, к массе вещества, которое теоретически должно выделится согласно закону Фарадея, и выражается в процентах:
![]() (1.3.3)
(1.3.3)
Масса m теор находится по формуле
Выход по энергии определяется по уравнению
где, Е теор и Е пр – теоретическое и практическое напряжение разложения при электролизе соответственно, В; η - выход по энергии,%.
Выход по энергии может быть вычислен и по количеству затраченной энергии:
![]() (1.3.6)
(1.3.6)
где w теор и w пр – количество энергии, теоретически необходимое и практически затраченное на получение единицы продукта.
 (1.3.7)
(1.3.7)
где 1000 – коэффициент перевода Вт*ч в кВт*ч;
1*10 -6 – число, используемое для перевода граммов в тонны.
Теоретический расход электроэнергии находится по отношению
![]() (1.3.8)
(1.3.8)
где φ разл – напряжение разложения.
Примеры решения задач
1. Какие процессы происходят при электролизе расплава гидроокиси натрия?
В расплаве едкого натра содержатся ионы Nа + и ОН. Окисляющиеся у анода ионы ОН в следующей стадии разлагаются с образованием воды и кислорода. Процесс можно изобразить следующим образом:
К(-): 2Na + + 2е - = 2Na;
А(+): 2ОН - 2e - = Н 2 О + О 2
Два атома кислорода, соединяясь друг с другом, образуют молекулу кислорода О 2 . Таким образом, суммарное уравнение
4NаОН = 4Na + 2Н 2 О + О 2
При электролизе расплавов солей кислородных кислот окисляющиеся ионы кислотных остатков тут же разлагаются на кислород и соответствующие оксиды.
Своеобразно протекает электролиз в водном растворе. Дело в том, что сама вода - электролит, хотя и очень слабый. Таким образом, в водном растворе фактически содержатся два электролита - растворитель и растворенное вещество и соответственно по два вида как положительных, так и отрицательных ионов. Какие из них будут разряжаться, зависит от ряда условий. Как правило, можно руководствоваться следующим. Если положительные ионы электролита являются ионами очень активных металлов, как например Na + или К - , то при электролизе разряжаются не ионы этих металлов, а ионы водорода из воды с выделением свободного водорода и освобождением гидроксильных ионов, что может быть выражено следующим электронно-ионным уравнением:
2H+OH+ 2е - = Н 2 + 2ОН
Если отрицательными ионами электролита являются кислотные остатки кислородных кислот, то при электролизе разряжаются не кислотные остатки этих кислот, а ионы ОН из воды с выделением кислорода, что можно выразить уравнением:
4Н 2 О - 4е - = 4Н + + 4ОН
4ОН - 2Н 2 О+О 2
Складывая оба уравнения, получаем:
2Н 2 О - 4е - = 4H + + O 2
2. Определить выход по току (в%), если в течение 24 ч в электролизере раствора поваренной соли при силе тока 15500А было получено 4200 л электролитической щелочи с концентрацией NaOH 125 кг/м 3.
По уравнению (1.3.4) масса гидроксида натрия теоретически должна была составить
![]()
практически было получено
![]()
Следовательно, выход по току по формуле (1.3.3) будет равен
![]()
Ответ: выход по току 94,6%.
3. Определите фактический расход электроэнергии (в киловатт-часах) на получение хлора массой 1 т и выход по энергии (в%), если среднее напряжение на электролизере 3,35В, выход по току 96%, а электрохимический эквивалент хлора равен 1,323 г/А*ч.
Использовав формулу (1.3.7), определим фактический расход энергии
![]()
Если принять выход по току за 100%, то при теоретическом напряжении разложения NaCl, равном 2,17В, теоретический расход энергии на 1т хлора составит
![]()
В этом случае выход по энергии
![]()
Ответ: выход по энергии 62,2%; 2637 кВ/ч
Задачи для самостоятельного решения
1. Один из способов промышленного получения кальция – электролиз расплавленного хлорида кальция. Какая масса металла будет получена, если известно, что в результате электролиза выделился хлор объемом 896 л (н.у.)?
2. При электролизе раствора хлорида натрия в электролизе, работавшем в течении 24ч при силе тока 30000 А, было получено 8,5 м 3 электролитической щелочи с концентрацией NaOH 120 кг/м 3. рассчитать выход по току (для щелочи)
3. Определить силу тока, необходимые для выработки 100% -ного гидроксида натрия массой 1720 кг в сутки в электролизере с железным катом при его непрерывной работе, если выход по току составляет 96%
4. Вычислить массу хлора, вырабатываемого за год заводом, на котором установлено 5 серий по 150 электролизеров с железными катодами при непрерывной работе в течении 350 дней, силе тока 34000 А и выходе по току 95%. Определить мощность генератора переменного тока электростанции, обеспечивающий потребности завода в электрической энергии при напряжении донной серии 550 В, если КПД выпрямителя тока составляет 95%.
5. Вычислить теоретический и практический расход электроэнергии на 1т 100% NаОН для электролиза раствора хлорида натрия с ртутным катодом. Теоретическое напряжение разложения равно 3,168 В. Определить выход по энергии, если практическое напряжение разложения 4,4 В, а выход по току 92,5%.
6. Какие вещества, и в каком количестве выделяются на угольных электродах, если состав раствора 0,1 моль HgCl 2 и 0,2 моль CuCl 2 и через него пропускается ток силой 10 А в течение 1 ч?
7. При прохождении электрического тока через разбавленный раствор серной кислоты в течении 10 мин выделилось 100 мл водорода при 18С и давлении
755 мм рт. ст. Вычислите силу тока.
8. При электролитическом получении магния в качестве электролита может служит расплавленных хлорид магния. Вычислите выход по току, если в ванне, работающем при силе тока 40000 А, в течении 5 ч, выделилось 72,6 кг магния.
9. Определить количество электричества, необходимое для выделения 1 м 3 водорода и 0,5 м 3 кислорода, получаемое при электролизе воды. Теоретическое напряжение воды равно 1,23 В, а фактическое превышает его в 1,5 – 2 раза. Рассчитать фактический расход электрической энергии.
10. При электролизе раствора содержащего 2,895 г смеси FeCl 2 и FeCl 3 , на катоде выделилось 1,12 г металла. Вычислите массовую долю каждого из компонентов исходной смеси, если электролиз проводили до полного осаждения железа.





Принципа приближения и термодинамической обратимости к экстрактивной ректификации, с одной стороны, и выявить области оптимальности схем экстрактивной ректификации, с другой стороны. Постановка задачи Целью данной работы является разработка технологии разделения азеотропной смеси циклогексан – бензол – этилбензол методом экстрактивной ректификации, обладающей минимальными энергозатратами. Для...
И дидактические основы организации обучения позволяют более доступно объяснять изучаемый материал на уроках физики при изучении темы «Основы электродинамики». Анализ различных технологий позволил составить авторскую технологию развития у учащихся направленности на диалогическое общение при групповой форме обучения. От того, на сколько правильно будет построен процесс обучения при использовании...



Групп – в виде краткого отчета о проделанной работе (демонстрация рисунков, таблиц). Далее идет обсуждение выступлений; учитель продумывает со своими коллегами трудовое задание . 1.1 Межпредметные связи при решении расчетных задач К изучению математики учащиеся средней школы приступают на 7 лет раньше, чем к изучению химии. За этот период обучения они приобретают значительный объем...
Образование нерастворимого вещества в результате химической реакции – это лишь одно из условий получения коллоидного раствора. Другим не менее важным условием является неравенство исходных веществ, взятых в реакцию. Следствием этого неравенства является ограничение роста величины частиц коллоидах растворов, которое привело бы к образованию грубодисперсной системы.
Механизм образования коллоидной частицы рассмотрим на примере образования золя иодистого серебра, который получается при взаимодействии разбавленных растворов азотнокислого серебра и йодистого калия.
AgNO 3 +KI = AgI + KNO 3
Ag + + NO 3 ¯ +K + + I ¯ = AgI ↓ + NO 3 ¯ + K +
Нерастворимые нейтральные молекулы йодистого серебра образуют ядро коллоидной частицы.
Сначала эти молекулы соединяются в беспорядке, образуя аморфную, рыхлую структуру, которая постепенно превращается в высокоупорядоченную кристаллическую структуру ядра. В рассматриваемом нами примере ядро это кристаллик йодистого серебра, состоящий из большого числа (m) молекул AgI:
m - ядро коллоидной частицы
На поверхности ядра происходит адсорбционный процесс. По правилу Пескова-Фаянса, на поверхности ядер коллоидных частиц адсорбируются ионы, входящие в состав ядра частицы, т.е. адсорбируются ионы серебра (Аg +) илиионы иода (I –). Из этих двух видов ионов адсорбируютcя те, которые находятся в избытке.
Так, если получать коллоидный раствор в избытке йодистого калия, то адсорбироваться на частицах (ядрах) будут ионы иода, которые достраивают кристаллическую решетку ядра, естественно и прочно входя в его структуру. При этом образуется адсорбционный слой, который придает ядру отрицательный заряд:
Ионы, адсорбирующиеся на поверхности ядра, придавая ему соответствующий заряд, называются потенциалобразующими ионами.
При этом в растворе находятся и противоположно заряженные ионы, их называют противоионами. В нашем случае это ионы калия (K +), которые электростатически притягиваются к заряженному ядру (величина заряда может достигать I в). Часть противоионов К + прочно связывается электрическими и адсорбционными силам и и входит в адсорбционный слой. Ядро с образовавшимся на нем двойным адсорбционным слоем ионов называется гранулой.
{m . nI – . (n-x) K + } x – (структура гранулы)
Оставшаяся часть противоионов (обозначим их числом "х К + ") образует диффузный слой ионов.
Ядро с адсорбционным и диффузным слоями называется мицеллой:
{m . nI –. (n-x) K + } x – . х К + (структура мицеллы)
При пропускании постоянного электрического тока через коллоидный раствор гранулы и противоионы двинутся к противоположно заряженным электродам соответственно.
Наличие одноименного заряда на поверхности частиц золей является важным фактором его устойчивости. Заряд препятствует слипанию и укрупнению частиц. В устойчивой дисперсной системе частицы удерживаются во взвешенном состоянии, т.е. не происходит выпадения в осадок коллоидного вещества. Это свойство золей называется кинетической устойчивостью.
Строение мицелл золя иодистого серебра, полученного в избытке AgNO 3 , представлено на рис. 1а, в избытке KCI - 1б.
Рис.1.5. Строение мицелл золя иодистоого серебра, полученного в избытке:
а) азотнокислого серебра; б) хлорида калия.
Электролиз – совокупность окислительно-восстановительных процессов, происходящих при пропускании постоянного электрического тока через раствор или расплав электролита с погруженными в него электродами.
Прибор, в котором проводят электролиз, называется электролизером.
Электрод, на котором протекают процессы окисления, называется анодом. В электролизере он заряжен положительно (подключен к положительному полюсу внешнего источника постоянного тока).
Электрод, на котором протекают процессы восстановления, называется катодом. В электролизере он заряжен отрицательно (подключен к отрицательному полюсу внешнего источника постоянного тока).
При приложении напряжения катионы (положительно заряженные частицы) движутся к катоду, анионы (отрицательно заряженные частицы) – к аноду, и там происходит их разряд. На аноде ионы отдают электроны, происходит их окисление. На катоде ионы принимают электроны, происходит их восстановление.
В электродных процессах не всегда участвуют только катионы и анионы электролита, конкуренцию им составляют молекулы растворителя, в частности, воды – если проводят электролиз водного раствора.
Кроме того, участие воды в электрохимических процессах при электролизе может привести и к другому результату. Образующиеся в качестве промежуточных продуктов свободные радикалы ОН (за счет окисления на аноде гидроксид-ионов ) и Н (за счет восстановления на катоде ионов водорода ) обладают высокой реакционной способностью и сильно выраженными соответственно окислительными и восстановительными свойствами. У поверхности электрода они способны вовлекаться во взаимодействие с растворенными в воде веществами. В таких случаях говорят об окислении в анодном и восстановлении в катодном пространствах.
Особенности протекания электрохимических процессов в водных растворах обусловлены способностью молекул воды повергаться как окислению (на аноде), так и восстановлению (на катоде).
Анод (+) рН=0 рН=7 рН=14
2H 2 O – 4e = 2O + 2H + 4ОН – – 4e = 4OH 4ОН – – 4e = 4OH
2О = О 2 4OH = O 2 + 2H 2 O 4OH = O 2 + 2H 2 O
2H 2 O – 4e = 2O + 2H +
Катод (–) рН=0 рН=7 рН=14
2H + + 2e = 2H 2H 2 O + 2e = 2H + 2OH – 2H 2 O + 2e = 2H + 2OH –
2Н = Н 2 или 2H = H 2
Различают первичные и вторичные электродные процессы. Первичные имеют электрохимическую природу, вторичные – неэлектрохимическую. В результате электролиза на электродах (катоде и аноде) выделяются соответствующие продукты восстановления и окисления (первичные процессы), которые в зависимости от условий могут вступать в реакции с растворителем, материалом электрода, друг с другом (рекомбинация атомов) и т.д. (вторичные процессы). В некоторых случаях нельзя однозначно разделить первичный и вторичный процессы. В приведенном выше примере свободные радикалы ОН (на аноде) и Н (на катоде) образовались в результате первичных процессов, а окисление манганат-ионов и восстановление азотной кислоты являлось вторичными процессами. Рассмотрим еще один пример.
В ряде случаев на протекание основных процессов при электролизе накладываются побочные реакции: взаимодействие между продуктами электролиза или реакции продуктов с водой. Для предотвращения вторичных реакций между продуктами электролиза используют диафрагмы (перегородки между анодом и катодом), препятствующие диффузии определенных ионов. Например, в приведенном примере с электролизом раствора хлорида натрия для предотвращения взаимодействия между хлором и гидроксид-ионами катод окружают диафрагмой, препятствующей диффузии ионов натрия и хлора. В результате в катодном пространстве концентрируется щелочь (NaОН). Поэтому в большинстве случаев следует ожидать небольшого различия в составе продуктов при электролизе одного и того же раствора с диафрагмой и без нее.
Е разл = Е А – Е К
Для каждого электролита существует определенное минимальное значение напряжения (от внешнего источника тока), которое необходимо приложить к электродам для протекания электролиза. Оно называется напряжением разложения (E разл).
Напряжение разложения представляет собой разность электродного потенциалов анодного и катодного процессов.
Е разл = Е А – Е К
На катоде в первую очередь происходит восстановление ионов или молекул, входящих в окислительно-восстановительную систему с наиболее положительным потенциалом (являющихся восстановленной формой в окислительно-восстановительных системах с наиболее положительным потенциалом).
1) Если электролизу подвергается расплав , содержащий несколько различных катионов металлов, то в этом случае последовательность восстановления определяется электродными потенциалами металлов в данных условиях (в данном расплаве! ). При этом в первую очередь восстанавливаются катионы металлов, обладающих большим значением электродного потенциала (с конца ряда напряжений для данного расплава).
2) Восстановительные процессы на катоде в водных растворах :
· катионы металлов, расположенных в ряду напряжений после водорода (со стандартным электродным потенциалом больше, чем у водорода): Cu 2+ , Hg 2 2+ , Ag + , Hg 2+ , Pt 2+ ... Pt 4+ . При электролизе они почти полностью восстанавливаются на катоде и выделяются в виде металла.
· катионы металлов, расположенных в начале ряда (со стандартным электродным потенциалом меньше, чем у алюминия): Li + , Na + , K + ... Al 3+ . При электролизе они не восстанавливаются, вместо них восстанавливаются молекулы воды.
· катионы металлов, расположенных в ряду после алюминия и до водорода (со стандартным электродным потенциалом больше, чем у алюминия, но меньше, чем у водорода): Mn 2+ , Zn 2+ , Cr 3+ , Fe 2+ ... H. При электролизе эти катионы восстанавливаются на катоде одновременно с молекулами воды.
3) Если к раствору, содержащему несколько катионов, приложить постепенно возрастающее напряжение, то электролиз начинается тогда, когда достигается потенциал разложения катиона с наиболее положительным потенциалом. Так, при электролизе раствора, содержащего ионы Cu 2+ (Е 0 Cu 2+/ Cu = 0.35 В) и Zn 2+ (Е 0 Zn 2+/ Zn = – 0.76 В), на катоде вначале выделяется медь, и лишь после того, как почти все ионы меди разрядятся, начнет выделяться цинк.
Казалось бы, по значениям электродных потенциалов, в водном растворе можно было бы осадить только металлы, стоящие в ряду напряжений после водорода. Однако, благодаря перенапряжению водорода удается осаждать из водных растворов многие металлы, которые по значениям их стандартных потенциалов осаждаться не должны (например, Zn). Кроме того, характер среды (кислая, нейтральная, щелочная) оказывает влияние на природу разряжаемого металла. Это связано с тем, что – как было показано выше, электродный потенциал зависит от реакции среды.
При пропускании постоянного электрического тока через электролит на электродах протекают химические реакции. Этот процесс называется электролиз, что означает разложение (вещества) с помощью электричества.
В разд. 8.1 было указано, что электролит -это такая жидкость, которая при пропускании через нее электрического тока подвергается химической реакции. Электролитом может быть расплавленная соль, как, например, расплав бромида свинца(Н), либо водный раствор какой-либо кислоты, основания или соли.
Электрический ток подводится к электролиту с помощью электродов - проволочных проводников, металлических стержней или пластин, осуществляющих электрический контакт с электролитом. Отрицательно заряженный электрод это катод, а положительный электрод -анод. Электроды, которые не вступают в химические реакции, находясь в контакте с электролитами и при пропускании через них электрического тока, называются инертными электродами. К числу инертных электродов относятся графит и платина.
ИОННАЯ ТЕОРИЯ ЭЛЕКТРОЛИЗА
Согласно этой теории, прохождение постоянного электрического тока через электролит осуществляется с помощью ионов. На электродах происходит перенос электронов к ионам либо от них. Поэтому процессы, протекающие на электродах, могут рассматриваться как восстановительные или окислительные полуреакции. Таким образом, электролиз представляет собой окислительно-восстановительный процесс.
На аноде всегда осуществляется окислительная полуреакция. В этой реакции анионы теряют электроны и разряжаются, превращаясь в нейтральные частицы. Поэтому анод выступает в роли места стока электронов с анионов.
На катоде всегда осуществляется восстановительная полуреакция. Здесь катионы приобретают электроны и разряжаются, превращаясь в нейтральные частицы. Поэтому катод выступает в роли источника электронов для катионов.
Электролиз расплавленного бромида свинца(Н) состоит из двух полуреакций:
1) на аноде разряжаются бромид-ионы. (Уравнение этой полуреакции имеет
2Вг-(ж.) = Вг2(г.) + 2е-
Эта полуреакция представляет собой окисление.)
2) на катоде разряжаются ионы свинца. (Уравнение этой полуреакции:
РЬ2+(тв.) + 2е- = РЬ(ж.)
Эта полуреакция представляет собой восстановление.)
Следует отметить, что реакции, протекающие на аноде и катоде в каждой конкретной системе, предопределяются полярностью источника тока во внешней электрической цепи. Отрицательный полюс внешнего источника тока (батареи) поставляет электроны одному из электродов электролитической ячейки. Это обусловливает отрицательный заряд данного электрода. Он и становится катодом. Поскольку этот электрод заряжен отрицательно, он в свою очередь вызывает такую электродную реакцию, в которой происходит потребление электронов. Таким образом, на этом электроде осуществляется восстановительный процесс. На другом электроде электроны перетекают из электролитической ячейки обратно во внешнюю цепь, что делает этот электрод положительным электродом. Значит, этот электрод играет роль анода. Из-за его положительного заряда на нем протекает реакция, которая сопровождается отдачей электронов, т. е. окисление.
Схематическое изображение всего процесса электролиза представлено на рис. 10.6.