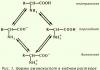
Соединения железа (II)
Соединения железа со степень окисления железа +2 малоустойчивы и легко окисляются до производных железа (III).
Fe 2 O 3 + CO = 2FeO + CO 2 .
Гидроксид железа (II) Fe(OH) 2 в свежеосажденном виде имеет серовато-зеленую окраску, в воде не растворяется, при температуре выше 150 °С разлагается, быстро темнеет вследствие окисления:
4Fe(OH) 2 + O 2 + 2H 2 O = 4Fe(OH) 3 .
Проявляет слабовыраженные амфотерные свойства с преобладанием основных, легко реагирует с неокисляющими кислотами:
Fe(OH) 2 + 2HCl = FeCl 2 + 2H 2 O.
Взаимодействует с концентрированными растворами щелочей при нагревании с образованием тетрагидроксоферрата (II):
Fe(OH) 2 + 2NaOH = Na 2 .
Проявляет восстановительные свойства, при взаимодействии с азотной или концентрированной серной кислотой образуются соли железа (III):
2Fe(OH) 2 + 4H 2 SO 4 = Fe 2 (SO 4) 3 + SO 2 + 6H 2 O.
Получается при взаимодействии солей железа (II) с раствором щелочи в отсутствии кислорода воздуха:
FeSO 4 + 2NaOH = Fe(OH) 2 + Na 2 SO 4 .
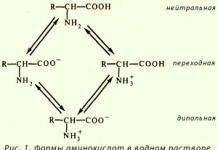
Соли железа (II). Железо (II) образует соли практически со всеми анионами. Обычно соли кристаллизуются в виде зеленых кристаллогидратов: Fe(NO 3) 2 · 6H 2 O, FeSO 4 · 7H 2 O, FeBr 2 · 6H 2 O, (NH 4) 2 Fe(SO 4) 2 · 6H 2 O (соль Мора) и др. Растворы солей имеют бледно-зеленую окраску и, вследствие гидролиза , кислую среду:
Fe 2+ + H 2 O = FeOH + + H + .
Проявляют все свойства солей.
При стоянии на воздухе медленно окисляются растворенным кислородом до солей железа (III):
4FeCl 2 + O 2 + 2H 2 O = 4FeOHCl 2 .
Качественная реакция на катион Fe 2+ - взаимодействие с гексацианоферратом (III) калия (красной кровяной солью) :
FeSO 4 + K 3 = KFe↓ + K 2 SO 4
Fe 2+ + K + + 3- = KFe↓
в результате реакции образуется осадок синего цвета - гексацианоферрат (II) железа (III) - калия.
Степень окисления +3 характерна для железа.
Оксид железа (III) Fe 2 O 3 - вещество бурого цвета, существует в трех полиморфных модификациях.
Проявляет слабовыраженные амфотерные свойства с преобладанием основных. Легко реагирует с кислотами:
Fe 2 O 3 + 6HCl = 2FeCl 3 + 3H 2 O.
С растворами щелочей не реагирует, но при сплавлении образует ферриты :
Fe 2 O 3 + 2NaOH = 2NaFeO 2 + H 2 O.
Проявляет окислительные и восстановительные свойства. При нагревании восстанавливается водородом или оксидом углерода (II), проявляя окислительные свойства:
Fe 2 O 3 + H 2 = 2FeO + H 2 O,
Fe 2 O 3 + CO = 2FeO + CO 2 .
В присутствии сильных окислителей в щелочной среде проявляет восстановительные свойства и окисляется до производных железа (VI):
Fe 2 O 3 + 3KNO 3 + 4KOH = 2K 2 FeO 4 + 3KNO 2 + 2H 2 O.
При температуре выше 1400°С разлагается:
6Fe 2 O 3 = 4Fe 3 O 4 + O 2 .
Получается при термическом разложении гидроксида железа (III):
2Fe(OH) 3 = Fe 2 O 3 + 3H 2 O
или окислением пирита:
4FeS 2 + 11O 2 = 2Fe 2 O 3 + 8SO 2 .
FeCl 3 + 3KCNS = Fe(CNS) 3 + 3KCl,
Является одним из самых распространенных элементов в земной коре.
Физические свойства железа.
Железо - ковкий металл серебристо-белого цвета с высокой химической стойкостью. Оно хорошо переносит высокие температуры и влажности. Быстро тускнеет (ржавеет) на воздухе и в воде. Очень пластичный, хорошо поддается ковке и прокатке. Обладает хорошей тепло- и электропроводностью, отличный ферромагнетик.
Химические свойства железа.
Железо переходный металл. Может иметь степень окисления +2 и +3. Реагирует с водяным паром:
3 Fe + 4 H 2 O = Fe 3 O 4 + 4 H 2 .
Но в присутствии влаги железо ржавеет:
4 Fe + 3 O 2 + 6 H 2 O = 4 Fe (OH ) 3 .
2 Fe + 3 Cl 2 = 2 FeCl 3 .
Fe + H 2 SO 4 = FeSO 4 + H 2 .
Концентрированные кислоты пассивируют железо на холоде, но растворяют при нагревании:
2Fe + 6H 2 SO 4 = Fe 2 (SO 4) 3 + 3SO 2 + 6H 2 O.
Гидроксид железа (II ) получается при действии щелочи на соли железа (II) без доступа кислорода :
F 2 SO 4 + 2NaOH = Fe(OH) 2 + Na 2 SO 4 .
Выделяется осадок белого цвета, который на воздухе быстро окисляется:
4Fe(OH) 2 + O 2 + 2H 2 O = 4Fe(OH) 3 .
Данный гидроксид амфотерный, при нагреве растворяется в щелочах с образованием гексагидроферата:
Fe(OH) 3 + 3KOH = K 3 .
Железо образует две комплексные соли железа :
- Желтая кровяная соль K 4 [ Fe (CN ) 6 ];
- Красная кровяная соль K 3 [ Fe (CN ) 6 ].
Эти соединения являются качественными для определения ионов железа. Соединение берлинская лазурь :
K 4 + Fe 2+ = KFe III + 2K + .
Применение железа.
Железо является важнейшим компонентом процесса дыхания. Он входит в состав гемоглобина крови, участвует в переносе кислорода от легких к тканям. В природе железо встречается в составе руд и минералов.
Подробности Категория: Просмотров: 10184 ЖЕЛЕЗО
, Fe, химический элемент, атомный вес 55,84, порядковый номер 26; расположен в VIII группе периодической системы в одном ряду с кобальтом и никелем, температура плавления - 1529°С, температура кипения - 2450°С; в твердом состоянии имеет синевато-серебристый цвет. В свободном виде железо встречается лишь в метеоритах, которые, однако, содержат примеси Ni, Р, С и других элементов. В природе соединения железа широко распространены повсеместно (почва, минералы, гемоглобин животных, хлорофилл растений), гл. обр. в виде окислов, гидратов окислов и сернистых соединений, а также углекислого железа, из которых и состоит большинство железных руд.
ЖЕЛЕЗО
, Fe, химический элемент, атомный вес 55,84, порядковый номер 26; расположен в VIII группе периодической системы в одном ряду с кобальтом и никелем, температура плавления - 1529°С, температура кипения - 2450°С; в твердом состоянии имеет синевато-серебристый цвет. В свободном виде железо встречается лишь в метеоритах, которые, однако, содержат примеси Ni, Р, С и других элементов. В природе соединения железа широко распространены повсеместно (почва, минералы, гемоглобин животных, хлорофилл растений), гл. обр. в виде окислов, гидратов окислов и сернистых соединений, а также углекислого железа, из которых и состоит большинство железных руд.
Химически чистое железо получается путем нагревания щавелевокислого железа, при чем при 440°С сначала получается матовый порошок закиси железа, обладающий способностью воспламеняться на воздухе (т. н. пирофорическое железо); при последующем восстановлении этой закиси образовавшийся порошок приобретает серый цвет и теряет пирофорические свойства, переходя в металлическое железо. При восстановлении закиси железа при 700°С железо выделяется в виде мелких кристаллов, которые затем сплавляются в вакууме. Другой способ получения химически чистого железа состоит в электролизе раствора солей железа, например FeSО 4 или FeCl 3 в смеси с MgSО 4 , СаСl 2 или NH 4 Cl (при температуре выше 100°С). Однако, при этом железо окклюдирует значительное количество электролитического водорода, вследствие чего приобретает твердость. При прокаливании до 700°С водород выделяется, и железо становится мягким и режется ножом, как свинец (твердость по шкале Моса - 4,5). Весьма чистое железо может быть получено алюминотермическим путем из чистой окиси железо. (см. Алюминотермия). Хорошо образованные кристаллы железа встречаются редко. В полостях больших кусков литого железа иногда образуются кристаллы октаэдрической формы. Характерным свойством железа является его размягчаемость, тягучесть и ковкость при температуре, значительно более низкой, чем температура плавления. При действии на железо крепкой азотной кислоты (не содержащей низших окислов азота), железо покрывается налетом окислов и становится нерастворимым в азотной кислоте.
Соединения железа
Легко соединяясь с кислородом, железо образует несколько окислов: FeO - закись железа, Fe 2 О 3 - окись железа, FeО 3 - ангидрид железной кислоты и FeО 4 – ангидрид наджелезной кислоты. Кроме того, железо образует еще окисел смешанного типа Fe 3 О 4 - закись-окись железа, т. н. железную окалину. В сухом воздухе, однако, железо не окисляется; ржавчина представляет собой водные окислы железа, образующиеся при участии влаги воздуха и СО 2 . Закиси железа FeO соответствует гидрат Fe(OH) 2 и целый ряд солей двухвалентного железа, способных при окислении переходить в соли окиси железа, Fe 2 О 3 , в которой железо проявляет себя в качестве трехвалентного элемента; на воздухе гидрат закиси железа, отличающийся сильными восстановительными свойствами, легко окисляется, переходя в гидрат окиси железа. Гидрат закиси железа слабо растворяется в воде, и раствор этот имеет явственно щелочную реакцию, свидетельствующую об основном характере двухвалентного железа. Окись железа встречается в природе (см. Железный сурик), искусственно же м. б. получена в виде красного порошка при прокаливании железного порошка и при обжигании серного колчедана для получения сернистого газа. Безводная окись железа, Fе 2 O 3 , м. б. получена в двух модификациях, причем переход одной из них в другую происходит при нагревании и сопровождается значительным выделением тепла (самонакаливанием). При сильном прокаливании Fe 2 О 3 выделяет кислород и переходит в магнитную закись-окись, Fe 3 О 4 . При действии щелочей на растворы солей трехвалентного железа выпадает осадок гидрата Fe 4 О 9 H 6 (2Fe 2 О 3 ·3Н 2 О); при кипячении его с водой образуется гидрат Fe 2 О 3 ·Н 2 О, трудно растворяющийся в кислотах. Железо образует соединения с различными металлоидами: с С, Р, S, с галоидами, а также и с металлами, например с Mn, Cr, W, Сu и др.
Соли железа разделяются на закисные - двухвалентного железа (ферро-соли) и на окисные - трехвалентного железа (ферри-соли).
Соли закисного железа
Хлористое железо , FeCl 2 , получается при действии сухого хлора на железо, в виде бесцветных листочков; при растворении железа в НСl хлористое железо получается в виде гидрата FeCl 2 ·4H 2 O и применяется в виде водных или спиртовых растворов в медицине. Йодистое железо , FeJ 2 , получается из железа и йода под водой в виде зеленых листочков и применяется в медицине (Sirupus ferri jodati); при дальнейшем действии йода образуется FeJ 3 (Liquor ferri sesquijodati).
Сернокислое закисное железо, железный купорос , FeSО 4 ·7H 2 О (зеленые кристаллы) образуется в природе в результате окисления пирита и серных колчеданов; эта соль образуется также в качестве побочного продукта при производстве квасцов; при выветривании или при нагревании до 300°С переходит в белую безводную соль - FeSО 4 ; образует также гидраты с 5, 4, 3, 2 и 1 частицами воды; легко растворяется в холодной воде (в горячей до 300%); раствор имеет кислую реакцию вследствие гидролиза; на воздухе окисляется, особенно легко в присутствии другого окисляющегося вещества, например, щавелевокислых солей, которые FeSО 4 вовлекает в сопряженную реакцию окисления, обесцвечивает КМnO 4 ; при этом процесс протекает по следующему уравнению:
2KMnO 4 + 10FeSO 4 +8H 2 SO 4 = 2MnSО 4 + K 2 SО 4 + 5Fe 2 (SO 4) 2 + 8Н 2 О.
Для этой цели, однако, применяется более постоянная на воздухе двойная соль Мора (NH 4) 2 Fe(SО 4) 2 ·6Н 2 О. Железный купорос применяется в газовом анализе для определения окиси азота, поглощаемой раствором FeSО 4 с образованием окрашенного в тёмно-бурый цвет комплекса (FeNО)SО 4 , а также для получения чернил (с дубильными кислотами), в качестве протравы при крашении, для связывания зловонных газов (H 2 S, NH 3) в отхожих местах и т. д.
Закисные соли железа применяются в фотографии благодаря их способности восстанавливать серебряные соединения на скрытом изображении, запечатлевшемся на фотографической пластинке.
Углекислое железо , FeCO 3 , встречается в природе в виде сидерита или железного шпата; получаемое осаждением водных растворов закисных солей железа карбонатами углекислое железо легко теряет СО 2 и окисляется на воздухе до Fe 2 О 3 .
Бикарбонат железа , H 2 Fe(CО 3) 2 , растворим в воде и встречается в природе в железистых источниках, из которых, окисляясь, выделяется на поверхности земли в виде гидрата окиси железа, Fe(OH) 3 , переходящего в бурый железняк.
Фосфорнокислое железо , Fе 3 (РO 4) 2 ·8Н 2 O, белый осадок; встречается в природе слегка окрашенный, вследствие окисления железа, в голубой цвет, в виде вивианита .
Соли окисного железа
Хлорное железо , FeCl 3 (Fe 2 Cl 6), получается при действии избытка хлора на железо в виде гексагональных красных табличек; хлорное железо на воздухе расплывается; из воды кристаллизуется в виде FeCl 3 ·6Н 2 О (желтые кристаллы); растворы имеют кислую реакцию; при диализе постепенно гидролизуется почти до конца с образованием коллоидного раствора гидрата Fe(OH) 3 . FeCl 3 растворяется в спирте и в смеси спирта с эфиром, при нагревании FeCl 3 ·6H 2 О разлагается на НСl и Fe 2 O 3 ; применяется в качестве протравы и в качестве кровоостанавливающего средства (Liquor ferri sesquichlorati).
Сернокислое окисное железо , Fe 2 (SO 4) 3 , в безводном состоянии имеет желтоватый цвет, в растворе сильно гидролизуется; при нагревании раствора выпадают основные соли; железные квасцы, MFe(SO 4) 2 ·12H 2 O, М - одновалентный щелочной металл; лучше всех кристаллизуются аммонийные квасцы, NH 4 Fe(SО 4) 2 ·12Н 2 О.
Окисел FeО 3 - ангидрид железной кислоты, равно как и гидрат этого окисла H 2 FeО 4 - железная кислота - в свободном состоянии не м. б. получены в виду их крайней непрочности; но в щелочных растворах могут существовать соли железной кислоты, ферраты (например K 2 FeО 4), образующиеся при накаливании железного порошка с селитрой или КСlO 3 . Известна также малорастворимая бариевая соль железной кислоты BaFeО 4 ; т. о., железная кислота в некоторых отношениях весьма напоминает серную и хромовую кислоты. В 1926 г. киевским химиком Горалевичем описаны соединения окисла восьмивалентного железа - наджелезного ангидрида FeО 4 , полученные при сплавлении Fe 2 О 3 с селитрой или бертолетовой солью в виде калиевой соли наджелезной кислоты K 2 FeО 5 ; FeО 4 - газообразное вещество, не образующее с водой наджелезной кислоты H 2 FeО 5 , которая, однако, м. б. выделена в свободном состоянии разложением кислотами соли K 2 FeО 5 . Бариевая соль BaFeO 5 ·7Н 2 О, а также кальциевая и стронциевая соли получены Горалевичем в виде неразлагающихся белых кристаллов, выделяющих лишь при 250-300°С воду и при этом зеленеющих.
Железо дает соединения: с азотом - азотистое железо (нитрид) Fe 2 N при нагревании порошка железа в струе NH 3 , с углеродом - карбид Fe 3 C при насыщении в электрической печи железа углем. Кроме того, изучен целый ряд соединений железа с окисью углерода - карбонилы железа , например, пентакарбонил Fe(CO) 5 - слегка окрашенная жидкость с около 102,9°С (при 749 мм, удельный вес 1,4937), затем оранжевое твердое тело Fe 2 (CO) 9 , нерастворимое в эфире и хлороформе, с удельным весом 2,085.
Большое значение имеют цианистые соединения железа . Кроме простых цианидов Fe(CN) 2 и Fe(CN) 3 , железо образует целый ряд комплексных соединений с цианистыми солями, как, например, соли железистосинеродистой кислоты H 4 Fe(CN) 6 , и соли железосинеродистой кислоты H 3 Fe(CN) 6 , например, красная кровяная соль, которые, в свою очередь вступают в реакции обменного разложения с солями закисного и окисного железа, образуя окрашенные в синий цвет соединения - берлинскую лазурь и турнбуллову синь. При замене в солях железистосинеродистой кислоты H 4 Fe(CN) 6 одной группы CN на одновалентные группы (NO, NО 2 , NH 3 , SО 3 , СО) образуются пруссо-соли, например, нитропруссид натрия (нитрожелезистосинеродистый натрий) Na 2 ·2Н 2 О, получаемый действием дымящей HNО 3 на K 4 Fe(CN) 6 , с последующей нейтрализацией содой, в виде рубиново-красных кристаллов, отделяемых кристаллизацией от образующейся одновременно селитры; соответствующая нитрожелезистосинеродистая кислота H 2 кристаллизуется также в виде тёмно-красных кристаллов. Нитропруссид натрия применяется в качестве чувствительного реактива на сероводород и сернистые металлы, с которыми он дает кроваво-красное, переходящее затем в синее, окрашивание. При действии медного купороса на нитропруссид натрия образуется бледно-зелёный нерастворимый в воде и в спирте осадок, применяемый для испытания эфирных масел.
Аналитически железо обнаруживается действием на его соли, в щелочном растворе, желтой кровяной соли. Соли трехвалентного железа образуют при этом синий осадок берлинской лазури. Соли двухвалентного железа образуют синий осадок турнбулловой сини при действии на них красной кровяной соли. С роданистым аммонием NH 4 CNS соли трехвалентного железа образуют растворимое в воде с кроваво-красным окрашиванием родановое железо Fe(CNS) 3 ; с таннином соли окисного железа образуют чернила. Интенсивной окраской отличаются также и медные соли железистосинеродистой кислоты, которые находят себе применение (увахромовый метод) в цветной фотографии. Из соединений железа, применяемых в медицине, кроме упомянутых галоидных соединений железа, имеют значение: металлическое железо (F. hydrogenio reductum), лимоннокислое железо (F. Citricum - 20% Fe), экстракт яблочнокислого железа (Extractum ferri pomatum), железный альбуминат (Liquor ferri albuminatum), ферратин - белковое соединение с 6% железа; ферратоза - раствор ферратина, карниферрин - соединение железа с нуклеином (30% Fe); ферратоген из нуклеина дрожжей (1% Fe), гематоген - 70%-ный раствор гемоглобина в глицерине, гемол - гемоглобин , восстановленный цинковой пылью.
Физические свойства железа
Имеющиеся в литературе числовые данные, характеризующие различные физические свойства железа, колеблются вследствие трудности получения железа в химически чистом состоянии. Поэтому наиболее достоверными являются данные, полученные для электролитического железа, в котором общее содержание примесей (С, Si, Mn, S, Р) не превышает 0,01-0,03%. Приводимые ниже данные в большинстве случаев и относятся к такому железу. Для него температура плавления равна 1528°С ± 3°С (Руер и Клеспер, 1914 г.), a температура кипения ≈ 2450°С. В твердом состоянии железо существует в четырех различных модификациях - α, β, γ и δ, для которых довольно точно установлены следующие температурные пределы:

Переход железа из одной модификации в другую обнаруживается на кривых охлаждения и нагревания критическими точками, для которых приняты следующие обозначения:


Указанные критические точки представлены на фиг. 1 схематическими кривыми нагревания и охлаждения. Существование модификаций δ-, γ- и α-Fe считается в настоящее время бесспорным, самостоятельное же существование β-Fe оспаривается вследствие недостаточно резкого отличия его свойств от свойств α-Fe. Все модификации железа кристаллизуются в форме куба, причем α, β и δ имеют пространственную решетку центрированного куба, а γ-Fe - куба с центрированными гранями. Наиболее отчетливые кристаллографические характеристики модификаций железа получены на рентгеновских спектрах, как это представлено на фиг. 2 (Вестгрин, 1929 г.).

Из приведенных рентгенограмм следует, что для α-, β- и δ-Fe линии рентгеновского спектра одни и те же; они соответствуют решетке центрированного куба с параметрами 2,87, 2,90 и 2,93 Ȧ, а для γ-Fe спектр соответствует решетке куба с центрированными гранями и параметрами 3,63-3,68 А.
Удельный вес железа колеблется в пределах от 7,855 до 7,864 (Кросс и Гилль, 1927 г.). При нагревании удельный вес железа падает вследствие теплового расширения, для которого коэффициенты увеличиваются с температурой, как показывают данные табл. 1 (Дризен, 1914 г.).

Понижение коэффициентов расширения в интервалах 20-800°С, 20-900°С, 700-800°С и 800- 900°С объясняется аномалиями в расширении при переходе через критические точки А С2 и А С3 . Этот переход сопровождается сжатием, особенно резко выраженным в точке А С3 , как показывают кривые сжатия и расширения на фиг. 3. Плавление железа сопровождается расширением его на 4,4% (Гонда и Энда, 1926 г.). Теплоемкость железа довольно значительна по сравнению с другими металлами и выражается для разных температурных интервалов величинами от 0,11 до 0,20 Сal, как показывают данные табл. 2 (Обергоффер и Гроссе, 1927 г.) и построенная на основании их кривая (фиг. 4).

В приведенных данных превращения А 2 , А 3 , А 4 и плавление железа обнаруживаются настолько отчетливо, что для них легко вычисляются тепловые эффекты: А 3 ... + 6,765 Сal, А 4 ... + 2,531 Сal, плавление железа... - 64,38 Сal (по С. Умино, 1926 год, - 69,20 Сal).

Железо характеризуется приблизительно в 6-7 раз меньшей теплопроводностью, чем серебро, и в 2 раза меньшей, чем алюминий; а именно, теплопроводность железа равняется при 0°С - 0,2070, при 100°С - 0,1567, при 200°С - 0,1357 и при 275°С - 0,1120 Cal/см·сек·°С. Наиболее характерными свойствами железа являются магнитные, выражаемые целым рядом магнитных констант, получаемых при полном цикле намагничивания железа. Эти константы для электролитического железа выражаются следующими значениями в гауссах (Гумлих, 1909 и 1918 гг.):

При переходе через точку А с2 ферромагнитные свойства железа почти исчезают и м. б. обнаружены только при очень точных магнитных измерениях. Практически β-, γ- и δ-модификации считаются немагнитными. Электропроводность для железа при 20°С равняется R -1 мо м/мм 2 (где R - электрическое сопротивление железа, равное 0,099 Ω мм 2 /м). Температурный коэффициент электросопротивления а0-100° х10 5 колеблется в пределах от 560 до 660, где
![]()

Холодная обработка (прокатка, ковка, протяжка, штамповка) очень заметно отражается на физических свойствах железа. Так, %-ное изменение их при холодной прокатке выражается следующими цифрами (Геренс, 1911 г.): коэрцитивное напряжение +323%, магнитный гистерезис +222%, электросопротивление + 2%, удельный вес - 1%, магнитная проницаемость - 65%. Последнее обстоятельство делает понятными те значительные колебания физических свойств, которые наблюдаются у разных исследователей: к влиянию примесей нередко присоединяется еще и влияние холодной механической обработки.
О механических свойствах чистого железа известно очень мало. Электролитическое железо, сплавленное в пустоте, обнаружило: временное сопротивление на разрыв 25 кг/мм 2 , удлинение - 60%, сжатие поперечного сечения - 85%, твердость по Бринеллю - от 60 до 70.
Структура железа находится в зависимости от содержания в нем примесей (хотя бы и в незначительных количествах) и предварительной обработки материала. Микроструктура железа, как и других чистых металлов, состоит из более или менее крупных зерен (кристаллитов), носящих здесь название феррита


Размеры и резкость их очертаний зависят гл. обр. от скорости охлаждения железа: чем последняя меньше, тем больше развиты зерна и тем резче их контуры. С поверхности зерна бывают окрашены чаще всего неодинаково вследствие неодинаковой кристаллографии, ориентировки их и неодинакового травящего действия реактивов по разным направлениям в кристалле. Нередко зерна бывают вытянуты в одном направлении в результате механической обработки. Если обработка происходила при невысоких температурах, то на поверхности зерен появляются линии сдвигов (линии Неймана), как результат скольжения отдельных частей кристаллитов по плоскостям их спайности. Эти линии являются одним из признаков наклепа и тех изменений в свойствах, о которых было упомянуто выше.
Железо в металлургии
Термин железо в современной металлургии присваивается лишь сварочному железу, т. е. малоуглеродистому продукту, получаемому в тестообразном состоянии при температуре, не достаточной для плавления железа, но высокой настолько, что отдельные частицы его хорошо свариваются друг с другом, давая после проковки однородный мягкий продукт, не принимающий закалки. Железо (в указанном смысле слова) получается: 1) непосредственно из руды в тестообразном состоянии сыродутным процессом; 2) таким же способом, но при более низкой температуре, недостаточной для сваривания частиц железа; 3) переделом чугуна кричным процессом; 4) переделом чугуна пудлингованием.
1) Сыродутный процесс в наст. время применяется лишь малокультурными народами и в таких местностях, куда не может (по отсутствию удобных путей сообщения) проникнуть американское или европейское железо, получаемое современными способами. Процесс ведется в открытых сыродутных горнах и печах. Сырыми материалами для него служат железная руда (обыкновенно бурый железняк) и древесный уголь. Уголь засыпается в горн в той половине его, куда подводится дутье, руда же - кучей, с противоположной стороны. Образующаяся в толстом слое горящего угля окись углерода проходит через всю толщу руды и, имея высокую температуру, восстанавливает железо. Восстановление руды совершается постепенно - с поверхности отдельных кусков к сердцевине. Начинаясь с верхних частей кучи, оно ускоряется по мере продвижения руды в область более высокой температуры; окись железа при этом переходит сначала в магнитную окись, затем в закись, и, наконец, на поверхности кусков руды появляется металлическое железо. В то же время землистые примеси руды (пустая порода) соединяются с еще не восстановленной закисью железа и образуют легкоплавкий железистый шлак, который вытапливается через щели металлической оболочки, образующей как бы скорлупу в каждом куске руды. Будучи нагретыми до белокалильного жара, эти скорлупки свариваются друг с другом, образуя на дне горна губчатую массу железа - крицу, проникнутую шлаком. Для отделения от последнего вынутую из горна крицу разрубают на несколько частей, из которых каждую проковывают, подваривая, после охлаждения в том же горне в полосы или прямо в изделия (вещи домашнего обихода, оружие). В Индии сыродутный процесс ведется и теперь в сыродутных печах, которые отличаются от горнов только несколько большей высотой - около 1,5 м. Стены печей делаются из глиняной массы (не кирпича) и служат лишь одну плавку. Дутье подается в печь через одну фурму мехами, приводимыми в движение ногами или руками. В пустую печь загружается некоторое количество древесного угля («холостая колоша»), а затем попеременно, отдельными слоями, руда и уголь, при чем количество первой постепенно увеличивается до тех пор, пока не дойдет до определенного опытом отношения к углю; вес всей засыпанной руды определяется желаемым весом крицы, который, вообще говоря, незначителен. Процесс восстановления идет так же, как и в горне; железо тоже полностью не восстанавливается, и получающаяся на лещади крица заключает в себе много железистого шлака. Крицу извлекают разломкой печи и разрубают на части, в 2-3 кг весом. Каждую из них нагревают в кузнечном горне и обрабатывают под молотом; в результате получается превосходное мягкое железо, служащее, между прочим, материалом для изготовления индийской стали «вуц» (булат). Состав его следующий (в %):
Ничтожное содержание элементов - примесей железа - или совершенное их отсутствие объясняется чистотой руды, неполнотой восстановления железа и низкой температурой в печи. Расход древесного угля благодаря малым размерам горнов и печей и периодичности их действия очень велик. В Финляндии, Швеции и на Урале железо выплавляли в сыродутной печи Хусгавеля, в которой можно было регулировать ход процесса восстановления и насыщения железа углеродом; расход угля в ней - до 1,1 на единицу железа, выход которого достигал 90% содержания его в руде.
2) В будущем нужно ожидать развития производства железа непосредственно из руды не применением сыродутного процесса, а восстановлением железа при температуре, недостаточной для образования шлака и даже для спекания пустой породы руды (1000°С). Преимущества такого процесса - возможность применения низкосортных видов топлива, устранение флюса и расхода тепла на плавление шлака.
3) Получение сварочного железа переделом чугуна кричным процессом ведется в кричных горнах гл. обр. в Швеции (у нас - на Урале). Для передела выплавляют специальный чугун, т. н. ланкаширский, дающий наименьший угар. В составе его: 0,3-0,45% Si, 0,5-0,6% Mn, 0,02 Р, <0,01% S. Такой чугун в изломе кажется белым или половинчатым. Горючим в кричных горнах может служить только древесный уголь.
Процесс ведется след. обр.: горн, освобожденный от крицы, но с оставшимся на донной доске спелым шлаком конца процесса, наполняется углем, гл. обр. сосновым, на который укладывается подогретый продуктами горения чугун в количестве 165-175 кг (на 3/8 м 2 поперечного сечения горна приходится 100 кг садки чугуна). Поворотом клапана в воздухопроводе дутье направляется через трубы, расположенные в подсводовом пространстве горна, и нагревается здесь до температуры в 150-200°С, ускоряя т. о. плавление чугуна. Плавящийся чугун все время поддерживается (при помощи ломов) на угле выше фурм. При такой работе вся масса чугуна подвергается окислительному действию кислорода воздуха и углекислоты, проходя зону горения в виде капель. Большая поверхность их способствует быстрому окислению железа и его примесей - кремния, марганца и углерода. Смотря по содержанию этих примесей, чугун в большей или меньшей степени теряет их, прежде чем соберется на дне горна. Т. к. в шведском горне переделывается малокремнистый и маломарганцовый чугун, то, проходя горизонт фурм, он теряет весь свой Si и Мn (окислы которых с закисью железа образуют основной шлак) и значительную часть углерода. Плавление чугуна продолжается 20-25 мин. По окончании этого процесса пускают в горн холодное дутье. Осевший на дно горна металл начинает реагировать с находящимися там же спелыми шлаками, содержащими в себе большой избыток (по сравнению с количеством кремнезема) окислов железа - Fe 3 О 4 и FeO, окисляющих углерод с выделением окиси углерода, что приводит в кипение весь металл. Когда металл загустеет (от потери углерода) и «сядет товаром», последний поднимают ломами выше фурм, пускают опять горячее дутье и плавят «товар».
Во время вторичного плавления металл окисляется кислородом как дутья, так и шлаков, которые из него вытапливаются. На дно горна после первого подъема падает металл, достаточно мягкий для того, чтобы из отдельных наиболее спелых частей его собирать крицу. Но прежде, при употреблении кремнистых сортов чугуна, приходилось прибегать ко второму и даже третьему подъему товара, что, конечно, уменьшало производительность горна, увеличивало расход горючего и угар железа. На результаты работы оказывали влияние расстояние фурм от донной доски (глубина горна) и наклон фурм: чем круче поставлена фурма и меньше глубина горна, тем значительнее действие окислительной атмосферы на металл. Более пологий наклон фурм, как и большая глубина горна, уменьшает непосредственное действие кислорода дутья, предоставляя, т. о., большую роль действию шлака на примеси железа; окисление ими идет медленнее, но зато без угара железа. При всяких данных условиях наивыгоднейшее положение фурм относительно донной доски определяется опытом; в современном шведском горне глаз фурмы устанавливается на расстоянии 220 мм от донной доски, а наклон фурм меняется в тесных пределах - от 11 до 12°.
Получающаяся на дне горна крица заключает в себе, в отличие от сыродутной, очень мало механически увлеченного шлака; что же касается химических примесей железа, то Si, Мn и С м. б. полностью удалены (указываемое анализами ничтожное содержание Si и Мn входит в состав механической примеси - шлака), а сера - только отчасти, окисляясь дутьем во время плавления. В это же время окисляется и фосфор, уходя в шлак в виде фосфорножелезной соли, но последняя затем восстанавливается углеродом, и конечный металл может заключать в себе даже относительно больше фосфора (от угара железа), чем исходный чугун. Вот почему для получения первоклассного металла для экспорта в Швеции берут в передел исключительно чистый в отношении Р чугун. Вынутую из горна готовую крицу разрубают на три части (каждая 50-55 кг) и обжимают их под молотом, придавая вид параллелепипеда.
Длительность процесса передела в шведском кричном горне - от 65 до 80 мин.; в сутки получается от 2,5 до 3,5 тонн обжатых кусков «на огонь», при расходе древесного угля всего 0,32-0,40 на единицу готового материала и выходе его от 89 до 93,5% заданного в передел чугуна. В самое последнее время в Швеции были произведены удачные опыты передела жидкого чугуна, взятого от доменных печей, и ускорения процесса кипения перемешиванием металла при помощи механических граблей; при этом угар снизился до 7%, а расход угля - до 0,25.
О химическом составе шведского и южно-уральского железа дают понятие следующие данные (в %):
Из всех родов железа, получаемых промышленными способами, шведское кричное наиболее приближается к химически чистому и вместо последнего применяется в лабораторной практике и исследовательских работах. От сыродутного железа оно отличается своей однородностью, а от самого мягкого мартеновского металла (литого железа) отсутствием марганца; ему свойственна высшая степень свариваемости, тягучести и ковкости. Шведское кричное железо обнаруживает незначительное временное сопротивление на разрыв - всего около 30 кг/мм 2 , при удлинении в 40% и уменьшении поперечного сечения в 75%. В настоящее время годовая производительность кричного железа в Швеции упала до 50000 т, так как после войны 1914-18 гг. область промышленных применений для этого железа сильно сократилась. Наибольшее количество его идет на изготовление (в Англии гл. обр. и в Германии) высших сортов инструментальной и специальной сталей; в самой Швеции из него делают специальную проволоку («цветочную»), подковные гвозди, хорошо кующиеся в холодном состоянии, цепи и полосовую заготовку для сварных труб. Для последних двух целей особенно важны свойства кричного железа: надежная свариваемость, а для труб, сверх того, высшая устойчивость против ржавления.
4) Развитие производства железа кричным процессом влекло за собой истребление лесов; после того как последние в различных странах были взяты под защиту закона, ограничившего их вырубку годовым приростом, Швеция, а затем и Россия - лесистые страны, изобилующие рудами высокого качества, - сделались главными поставщиками железа на международном рынке в течение всего 18 в. В 1784 г. англичанин Корт изобрел пудлингование - процесс передела чугуна на поду пламенной печи, в топке которой сжигался каменный уголь. После смерти Корта Роджерс и Голл ввели существенные улучшения в конструкцию пудлинговой печи, что способствовало быстрому распространению пудлингования во всех промышленных странах и совершенно изменило характер и размеры производства в них железа в течение первой половины 19 века. Этим процессом получили ту массу металла, которая понадобилась для постройки железных судов, железных дорог, локомотивов, паровых котлов и машин.
Топливом для пудлингования служит длиннопламенный каменный уголь, но там, где его нет, приходилось прибегать и к бурому углю, а у нас на Урале - к дровам. Сосновые дрова дают более длинное пламя, чем каменный уголь; оно хорошо греет, но содержание влаги в дровах не должно превосходить 12%. Впоследствии на Урале была применена к пудлингованию регенеративная печь Сименса. Наконец, в США и у нас (в Волжском и Камском бассейнах) пудлинговые печи работали на нефти, распыляемой в рабочее пространство печи непосредственно.
Для быстроты передела и уменьшения расхода топлива желательно иметь холодный пудлинговый чугун; при выплавке его на коксе, однако, в продукте получается много серы (0,2 и даже 0,3%), а при высоком содержании фосфора в руде - и фосфора. Для обыкновенных торговых сортов железа такой чугун с низким содержанием кремния (менее 1 %), под названием передельного, выплавлялся прежде в большом количестве. Древесноугольный чугун, который переделывался на Урале и в центральной России, не содержал серы и давал продукт, шедший и на изготовление кровельного железа. В настоящее время пудлингование служит для производства качественного металла по особым спецификациям, и потому в пудлинговые печи поступает не обыкновенный передельный чугун, а высококачественный, например, марганцовый или «гематит» (малофосфористый), или, наоборот, сильнофосфористый для производства гаечного железа. Ниже указано содержание (в %) главных элементов в некоторых сортах чугуна, применяемых для пудлингования:

Пудлинговая печь по окончании предыдущей операции обыкновенно имеет на поду нормальное количество шлака для работы со следующей садкой. При переработке сильно кремнистого чугуна шлака остается в печи много, и его приходится спускать; наоборот, белый чугун оставляет под печи «сухим», и работу приходится начинать заброской на под нужного количества шлака, который берут из-под молота («спелый», наиболее богатый магнитной окисью). На шлак забрасывается садка чугуна, подогретая в чугуннике (250-300 кг в ординарных и 500-600 кг в двойных печах); затем в топку забрасывают свежую порцию горючего, прочищают колосники, и в печи устанавливается полная тяга. В течение 25-35 мин. чугун плавится, претерпевая б. или м. значительное изменение в своем составе. Твердый чугун окисляется кислородом пламени, причем железо, марганец и кремний дают двойной силикат, стекающий на под печи; плавящийся чугун обнажает все новые и новые слои твердого чугуна, который тоже окисляется и плавится. В конце периода плавления на поду получаются два жидких слоя - чугуна и шлака, на поверхности соприкосновения которых происходит, хотя и в слабой степени, процесс окисления углерода магнитной окисью железа, о чем свидетельствуют выделяющиеся из ванны пузыри окиси углерода. Смотря по содержанию кремния и марганца в чугуне, в расплавленном металле их остается неодинаковое количество: в малокремнистом древесноугольном чугуне или белом - коксовой плавки - кремний в большинстве случаев выгорает при плавлении полностью; иногда же остается некоторое количество его в металле (0,3-0,25%), равно как и марганца. Фосфор тоже окисляется в это время, переходя в фосфорножелезную соль. От уменьшения веса металла при выгорании названных примесей %-ное содержание углерода может даже возрасти, хотя некоторое количество его несомненно сжигается кислородом пламени и шлаков, покрывающих первые порции расплавленного металла.
Для ускорения выгорания оставшихся количеств кремния, марганца и углерода прибегают к пудлингованию, т. е. перемешиванию чугуна со шлаком при помощи клюшки с загнутым под прямым углом концом. Если металл жидок (серый чугун, сильно углеродистый), то перемешивание не достигает цели, и ванну предварительно делают густой забрасыванием в нее холодного спелого шлака или же уменьшением тяги устанавливают в печи неполное горение, сопровождающееся получением сильно коптящего пламени (томление). Через несколько минут, в течение которых производят непрерывно перемешивание, на поверхности ванны появляются обильные пузыри горящей окиси углерода - продукта окисления углерода чугуна кислородом магнитной окиси, растворенной в основном железистом шлаке. По мере хода процесса окисление С усиливается и переходит в бурное «кипение» всей массы металла, которое сопровождается вспучиванием ее и таким значительным увеличением объема, что часть шлака переливается через порог рабочих отверстий. По мере выгорания С повышается температура плавления металла, и для того, чтобы кипение продолжалось, повышают непрерывно температуру в печи. Оконченное при низкой температуре кипение дает сырой товар, т. е. высокоуглеродистую губчатую массу железа, неспособную свариваться; в горячей печи «садится» спелый товар. Процесс окисления примесей железа в пудлинговой печи начинается за счет кислорода шлака, представляющего сплав однокремнеземика железа (Fe 2 SiО 4) с магнитной окисью и закисью железа переменного состава. В английских печах состав смеси окислов выражается формулой 5Fe 3 О 4 ·5 FeО; по окончании кипения отношение окислов в истощенном шлаке выражается формулой Fe 3 О 4 ·5FeО, т. е. в процессе окисления принимает участие 80% всей магнитной окиси шлака. Реакции окисления м. б. представлены следующими термохимическими уравнениями:

Как видно из этих уравнений, окисление Si, Р и Мn сопровождается выделением тепла и, следовательно, нагревает ванну, тогда как окисление С при восстановлении Fe 3 О 4 в FeO поглощает тепло и потому требует высокой температуры. Этим объясняется порядок удаления примесей железа и то, что выгорание углерода заканчивается скорее в горячей печи. Восстановления Fe 3 О 4 до металла не происходит, т. к. для этого требуется более высокая температура, чем та, при которой идет «кипение».
Севший «товар», для того чтобы стать хорошо сваривающимся железом, нуждается еще в пропаривании: товар оставляют на несколько минут в печи и от времени до времени переворачивают ломами, причем нижние его части кладут наверх; под совокупным действием кислорода пламени и шлаков, пропитывающих всю массу железа, углерод в это время продолжает выгорать. Как только получится некоторое количество хорошо сваривающегося металла, из него, избегая лишнего окисления, начинают накатывать крицы. Всего накатывают по мере поспевания товара от 5 до 10 криц (не более 50 кг каждая); крицы выдерживают (пропаривают) у порога в области высшей температуры и подают под молот для обжатия, чем достигается выделение шлака, и придания им формы куска (сечение от 10x10 до 15x15 см), удобной для прокатки в валках. На место выданных криц перемещаются передвижением вперед следующие за ними, до последней. Длительность процесса при производстве металла высшего качества (волокнистое железо) из спелого (высокоуглеродистого) древесноугольного чугуна была на Урале такова: 1) посадка чугуна - 5 мин., 2) плавление - 35 мин., 3) томление - 25 мин., 4) пудлингование (перемешивание) - 20 мин., 5) пропаривание товара - 20 мин., 6) накатка и пропаривание криц - 40 мин., 7) выдача криц (10-11 шт.) - 20 мин.; всего - 165 мин. При работе на белом чугуне, на обычное торговое железо, длительность процесса сокращалась (в 3ападной Европе) до 100 и даже 75 мин.
Что касается результатов работы, то в разных металлургических районах они менялись в зависимости от рода топлива, качества чугуна и сорта производимого железа. Уральские печи, работавшие на дровах, давали выход годного железа на 1 м 3 дров от 0,25 до 0,3 т; расход нефти у нас на единицу железа - 0,3З, каменного угля в европейских печах - от 0,75 до 1,1. Суточная производительность наших больших печей (садка чугуна 600 кг) при работе на сушеных дровах была 4-5 т; выход материала, пригодного для производства кровельного железа, составлял 95-93% количества поступившего в передел чугуна. В Европе суточная производительность обыкновенных печей (садка 250-300 кг) - около 3,5 т при угаре в 9%, а для высококачественного железа - 2,5 т при угаре в 11%.
По химическому составу и физическим свойствам пудлинговое железо является гораздо худшим продуктом, чем кричное, с одной стороны, и литое мартеновское - с другой. Изготовлявшиеся прежде в 3ападной Европе обыкновенные сорта железа содержали много серы и фосфора, т. к. вырабатывались из нечистых коксовых чугунов, а обе эти вредные примеси только частью переходят в шлак; количество шлака в пудлинговом железе - 3-6%, в качественном металле оно не превосходит 2%. Присутствие шлака сильно понижает результаты механических испытаний пудлингового железа. Ниже приведены некоторые данные в %, характеризующие пудлинговое железо - обыкновенное зап.-европейское и хорошее уральское:

Ценным свойством, ради которого и поддерживается теперь производство пудлингового железа, является его прекрасная свариваемость, имеющая иногда особое значение с точки зрения безопасности. Спецификациями ж.-д. обществ предписывается изготовление из пудлингового железа сцепных устройств, тяг для переводных стрелок и болтов. Благодаря лучшему сопротивлению разъедающему действию воды, пудлинговое железо идет также для производства водопроводных труб. Из него же изготовляют гайки (фосфористый крупнозернистый металл) и высококачественное волокнистое железо для заклепок и цепей.
Строение сварочного железа, обнаруживаемое под микроскопом даже при слабом увеличении, характерно присутствием на фотографическом изображении черных и светлых составляющих; первые принадлежат шлаку, а вторые - зернам или волокнам железа, полученным при вытяжке металла.
Железо торговое
Металлургические заводы изготовляют для нужд промышленности железо двух главных видов: 1) листовое и 2) сортовое.
Листовое железо прокатывается в настоящее время до 3 м ширины; при толщине 1-З мм оно называется у нас тонкокатальным; от 3 мм и выше (обычно до 40 мм) - котельным, резервуарным, корабельным, смотря по назначению, которому соответствуют состав и механические свойства материала. Наиболее мягким является котельное железо; оно содержит обыкновенно 0,10-0,12% С, 0,4-0,5% Mn, Р и S - каждого не более 0,05%; временное сопротивление его на разрыв не д. б. больше 41 кг/мм 2 (но и не меньше 34 кг/мм 2), удлинение при разрыве - около 28%. Резервуарное железо выделывается более твердым и прочным; оно содержит 0,12-0,15% С; 0,5-0,7% Мn и не более 0,06% как Р, так и S; сопротивление разрыву 41-49 кг/мм 2 , удлинение 25-28%. Длина листов котельного и резервуарного железа устанавливается заказом сообразно размерам изделия, склепываемого из листов (избегая лишних швов и обрезков), но обыкновенно она не превышает 8 м, так как ограничивается для тонких листов их быстрым охлаждением вовремя процесса прокатки, а для толстых - весом слитка.
Листовое железо менее 1 мм толщины называется черной жестью; оно служит для изготовления белой жести и как кровельный материал. Для последней цели в СССР прокатывают листы размерами 1422x711 мм, весом 4-5 кг, при толщине 0,5-0,625 мм. Кровельное железо выпускается заводами в пачках весом по 82 кг. За границей черная жесть классифицируется в торговле по номерам специального калибра - от 20-го до 30-го (нормальная толщина германской жести от 0,875 до 0,22 мм, а английской - от 1,0 до 0,31 мм). Жесть изготовляется из самого мягкого литого железа, содержащего 0,08- 0,10% С, 0,3-0,35% Мn, если оно изготовляется из чугуна древесноугольной плавки (у нас), и 0,4-0,5% Мn, если исходным материалом служат коксовый чугун; сопротивление разрыву - от 31 до 34 кг/мм 2 , удлинение - 28-30%. Разновидностью листового железа является волнистое (гофрированное) железо. Оно разделяется по характеру волн на железо с низкими и высокими волнами; в первом - отношение ширины волны к глубине колеблется от 3 до 4, во втором 1-2. Волнистое железо делают толщиной 0,75-2,0 мм и шириной листов 0,72-0,81 м (с низкими волнами) и 0,4-0,6 м (с высокими волнами). Волнистое железо употребляется для кровель, стен легких сооружений, жалюзи, а с высокими волнами, кроме того, идет для постройки бесстропильных перекрытий.
Сортовое железо делится по форме поперечного сечения на два класса: обыкновенное сортовое железо и фасонное.
К первому классу относится железо круглое (при диаметре менее 10 мм называемое проволокой), квадратное, плоское или полосовое. Последнее, в свою очередь, делится на: собственно полосовое - шириной от 10 до 200 мм и толщиной более 5 мм; обручное - той же ширины, но толщиной от 5 до 1 мм, указываемой № калибра (от 3-го до 19-го нормального германского и от 6-го до 20-го нового английского калибра); шинное - от 38 до 51 мм шириной и до 22 мм толщиной; универсальное - от 200 до 1000 мм шириной и не менее 6 мм толщиной (прокатывается в особых валках - универсальных). Как шинное, так и обручное железо выпускается заводами скатами, катаная проволока - мотками; остальные сорта - в виде прямых (правленных) полос, обычно не более 8 м длиной (нормально - от 4,5 до 6 м), но по специальному заказу для бетонных конструкций полосы нарезаются до 18 мм длиной, а иногда и более.
Главнейшие виды фасонного железа: угловое (равнобокое и неравнобокое), коробчатое (швеллерное), тавровое, двутавровое (балки), колонное (квадратное) и зетовое железо; существуют также и некоторые другие менее распространенные виды фасонного железа. По нашему нормальному метрическому сортименту размеры фасонного железа указываются № профиля (№ - число см. ширины полки или наибольшей высоты профиля). Угловое неравнобокое и тавровое железо имеют двойной №; напр., № 16/8 означает угловое с полками в 16 и 8 см или тавровое с полкой в 16 см и высотой тавра 8 см. Наиболее тяжелые профили катаемого у нас фасонного железа: № 15 - углового, № 30 - корытного, № 40 - двутаврового.
Состав обыкновенного сваривающегося сортового железа: 0,12% С, 0,4% Мn, менее 0,05% Р и S - каждого; сопротивление его разрыву 34-40 кг/мм 2 ; но круглое железо для заклепок изготовляется из более мягкого материала состава: менее 0,10% С, 0,25- 0,35% Мn, около 0,03% Р и S - каждого. Сопротивление разрыву 32-35 кг/мм 2 , а удлинение 28-32%. Фасонное не свариваемое, а склепываемое железо («строительная сталь») содержит: 0,15 - 0,20% С, 0,5% Мn, до 0,06% Р и S - каждого; его сопротивление разрыву 40-50 кг/мм 2 , удлинение 25-20%. Для производства гаек изготовляется железо (томасовское), содержащее около 0,1% С, но от 0,3 до 0,5% Р (чем крупнее гайки, тем больше Р). За границей для удовлетворения нужд специальных прокатных заводов в торговле обращается полупродукт - квадратная заготовка, обыкновенно 50 х 50 мм в поперечном сечении.
Первые изделия из железа и его сплавов были найдены при раскопках и датируются примерно 4 тысячелетием до нашей эры. То есть еще древние египтяне и шумеры использовали метеоритные месторождения данного вещества, чтобы изготовлять украшения и предметы быта, а также оружие.
Сегодня соединения железа различного рода, а также чистый металл - это самые распространенные и применяемые вещества. Не зря XX век считался железным. Ведь до появления и широкого распространения пластика и сопутствующих материалов именно это соединение имело для человека решающее значение. Что представляет собой данный элемент и какие вещества образует, рассмотрим в данной статье.
Химический элемент железо
Если рассматривать строение атома, то в первую очередь следует указать его местоположения в периодической системе.
- Порядковый номер - 26.
- Период - четвертый большой.
- Группа восьмая, подгруппа побочная.
- Атомный вес - 55,847.
- Строение внешней электронной оболочки обозначается формулой 3d 6 4s 2 .
- - Fe.
- Название - железо, чтение в формуле - "феррум".
- В природе существует четыре стабильных изотопа рассматриваемого элемента с массовыми числами 54, 56, 57, 58.
Химический элемент железо имеет также около 20 различных изотопов, которые не отличаются стабильностью. Возможные степени окисления, которые может проявлять данный атом:
Важное значение имеет не только сам элемент, но и его различные соединения и сплавы.
Физические свойства
Как простое вещество, железо имеет с ярко выраженным металлизмом. То есть это серебристо-белый с серым оттенком металл, обладающий высокой степенью ковкости и пластичности и высокой температурой плавления и кипения. Если рассматривать характеристики более подробно, то:
- температура плавления - 1539 0 С;
- кипения - 2862 0 С;
- активность - средняя;
- тугоплавкость - высокая;
- проявляет ярко выраженные магнитные свойства.
В зависимости от условий и различных температур, существует несколько модификаций, которые образует железо. Физические свойства их различаются от того, что разнятся кристаллические решетки.

Все модификации имеют различные типы строения кристаллических решеток, а также отличаются магнитными свойствами.
Химические свойства
Как уже упоминалось выше, простое вещество железо проявляет среднюю химическую активность. Однако в мелкодисперсном состоянии способно самовоспламеняться на воздухе, а в чистом кислороде сгорает сам металл.
Коррозионная способность высокая, поэтому сплавы данного вещества покрываются легирующими соединениями. Железо способно взаимодействовать с:
- кислотами;
- кислородом (в том числе воздухом);
- серой;
- галогенами;
- при нагревании - с азотом, фосфором, углеродом и кремнием;
- с солями менее активных металлов, восстанавливая их до простых веществ;
- с острым водяным паром;
- с солями железа в степени окисления +3.
Очевидно, что, проявляя такую активность, металл способен образовывать различные соединения, многообразные и полярные по свойствам. Так и происходит. Железо и его соединения чрезвычайно разнообразны и находят применение в самых разных отраслях науки, техники, промышленной деятельности человека.
Распространение в природе
Природные соединения железа встречаются довольно часто, ведь это второй по распространенности элемент на нашей планете после алюминия. При этом в чистом виде металл встречается крайне редко, в составе метеоритов, что говорит о больших его скоплениях именно в космосе. Основная же масса содержится в составе руд, горных пород и минералов.

Если говорить о процентном содержании рассматриваемого элемента в природе, то можно привести следующие цифры.
- Ядра планет земной группы - 90%.
- В земной коре - 5%.
- В мантии Земли - 12%.
- В земном ядре - 86%.
- В речной воде - 2 мг/л.
- В морской и океанской - 0,02 мг/л.
Самые распространенные соединения железа формируют следующие минералы:
- магнетит;
- лимонит или бурый железняк;
- вивианит;
- пирротин;
- пирит;
- сидерит;
- марказит;
- леллингит;
- миспикель;
- милантерит и прочие.
Это еще далеко список, ведь их действительно очень много. Кроме того, широко распространены различные сплавы, которые создаются человеком. Это тоже такие соединения железа, без которых сложно представить современную жизнь людей. К ним относятся два основных типа:
- чугуны;
- стали.
Также именно железо является ценной добавкой в составе многих никелевых сплавов.
Соединения железа (II)
К таковым относятся такие, в которых степень окисления образующего элемента равна +2. Они достаточно многочисленны, ведь к ним можно отнести:
- оксид;
- гидроксид;
- бинарные соединения;
- сложные соли;
- комплексные соединения.
Формулы химических соединений, в которых железо проявляет указанную степень окисления, для каждого класса индивидуальны. Рассмотрим наиболее важные и распространенные из них.
- Оксид железа (II). Порошок черного цвета, в воде не растворяется. Характер соединения - основный. Способен быстро окисляться, однако и восстанавливаться до простого вещества может также легко. Растворяется в кислотах, образуя соответствующие соли. Формула - FeO.
- Гидроксид железа (II). Представляет собой белый аморфный осадок. Образуется при реакции солей с основаниями (щелочами). Проявляет слабые основные свойства, способен быстро окисляться на воздухе до соединений железа +3. Формула - Fe(OH) 2 .
- Соли элемента в указанной степени окисления.
Имеют, как правило, бледно-зеленую окраску раствора, хорошо окисляются даже на воздухе, приобретая и переходя в соли железа 3. Растворяются в воде. Примеры соединений: FeCL 2 , FeSO 4 , Fe(NO 3) 2 .

Практическое значение среди обозначенных веществ имеют несколько соединений. Во-первых, (II). Это главный поставщик ионов в организм человека, больного анемией. Когда такой недуг диагностируется у пациента, то ему прописывают комплексные препараты, в основе которых лежит рассматриваемое соединение. Так происходит восполнение дефицита железа в организме.
Во-вторых, то есть сульфат железа (II), вместе с медным используется для уничтожения сельскохозяйственных вредителей на посевах. Метод доказывает свою эффективность уже не первый десяток лет, поэтому очень ценится садоводами и огородниками.
Соль Мора
Это соединение, которое представляет собой кристаллогидрат сульфата железа и аммония. Формула его записывается, как FeSO 4 *(NH 4) 2 SO 4 *6H 2 O. Одно из соединений железа (II), которое получило широкое применение на практике. Основные области использования человеком следующие.
- Фармацевтика.
- Научные исследования и лабораторные титриметрические анализы (для определения содержания хрома, перманганата калия, ванадия).
- Медицина - как добавка в пищу при нехватке железа в организме пациента.
- Для пропитки деревянных изделий, так как соль Мора защищает от процессов гниения.
Есть и другие области, в которых находит применение это вещество. Название свое оно получило в честь немецкого химика, впервые обнаружившего проявляемые свойства.
Вещества со степенью окисления железа (III)
Свойства соединений железа, в которых оно проявляет степень окисления +3, несколько отличны от рассмотренных выше. Так, характер соответствующего оксида и гидроксида уже не основный, а выраженный амфотерный. Дадим описание основным веществам.

Среди приведенных примеров с практической точки зрения важное значение имеет такой кристаллогидрат, как FeCL 3* 6H 2 O, или шестиводный хлорид железа (III). Его применяют в медицине для остановки кровотечений и восполнения ионов железа в организме при анемии.
Девятиводный сульфат железа (III) используется для очистки питьевой воды, так как ведет себя как коагулянт.
Соединения железа (VI)
Формулы химических соединений железа, где оно проявляет особую степень окисления +6, можно записать следующим образом:
- K 2 FeO 4 ;
- Na 2 FeO 4 ;
- MgFeO 4 и прочие.
Все они имеют общее название - ферраты - и обладают схожими свойствами (сильные восстановители). Также они способны обеззараживать и обладают бактерицидным действием. Это позволяет использовать их для обработки питьевой воды в промышленных масштабах.
Комплексные соединения
Очень важными в аналитической химии и не только являются особые вещества. Такие, которые образуются в водных растворах солей. Это комплексные соединения железа. Наиболее популярные и хорошо изученные из них следующие.
- Гексацианоферрат (II) калия K 4 . Другое название соединения - желтая кровяная соль. Используется для качественного определения в растворе иона железа Fe 3+ . В результате воздействия раствор приобретает красивую ярко-синюю окраску, так как формируется другой комплекс - берлинская лазурь KFe 3+ . Издревле использовалась как
- Гексацианоферрат (III) калия K 3 . Другое название - красная кровяная соль. Используется как качественный реагент на определение иона железа Fe 2+ . В результате образуется синий осадок, имеющий название турнбулева синь. Также использовалась, как краситель для ткани.

Железо в составе органических веществ
Железо и его соединения, как мы уже убедились, имеют большое практическое значение в хозяйственной жизни человека. Однако, помимо этого, его биологическая роль в организме не менее велика, даже наоборот.
Существует одно очень важное белок, в состав которого входит данный элемент. Это гемоглобин. Именно благодаря ему происходит транспорт кислорода и осуществляется равномерный и своевременный газообмен. Поэтому роль железа в жизненно важном процессе - дыхании - просто огромна.

Всего внутри организма человека содержится около 4 грамм железа, которое постоянно должно пополняться за счет потребляемых продуктов питания.
Класс: 9
Задачи урока:
Образовательная: познакомить учащихся с природными соединениями железа, рассмотреть важнейшие соединения железа (+2) и (+3), их свойства, ознакомить с качественными реакциями на ионы железа (+2) и (+3), показать народнохозяйственное значение соединений железа;
Развивающая: развитие речи, памяти, логического мышления, умений совместной деятельности; развитие и закрепление умений и навыков работать с лабораторным оборудованием;
Воспитательная: формирование мировоззрения, навыков сотрудничества, преемственности знаний, осуществление межпредметных связей, воспитание экологической грамотности, разумного отношения к природе (слайд 2).
Оборудование и реактивы:
образцы природных соединений железа (магнитный железняк, красный железняк, бурый железняк, железный колчедан); растворы хлорида железа (II) и (III), растворы красной кровяной соли и жёлтой кровяной соли, раствор роданида калия, раствор щёлочи; соли: железный купорос, хлорид железа (III), сульфат железа (III), необходимая химическая посуда.
Тип урока: комбинированный.
Ход урока
I. Организационный момент.
II. Актуализация знаний.
1 вариант
1) Fe + H 2 SO 4р-р =
3) Fe + AgNO 3 =
2 вариант
Закончите уравнения реакций. Уравнение №2 рассмотрите с точки зрения ОВР.
3 вариант
Закончите уравнения реакций. Уравнение №2 рассмотрите с точки зрения ОВР.
3) Fe + Cu(NO 3) 2 =
III. Изучение нового материала.
Нахождение железа в природе
Железо (5%) – второй по распространённости металл в земной коре, а в природе занимает 4 место. В природе встречается в виде оксидов и сульфидов:
Fe 3 O 4 – магнитный железняк (магнетит);
Fe 2 O 3 – красный железняк (гематит);
(Врач и алхимик Теофаст Парацельс много путешествовал и в 1530г из России привёз в свою лабораторию в г. Базеле кусок вишнёво – красного минерала – “кровавика”. Минерал действительно оставлял “кровавый” след – красную черту на пергаменте или белом камне. Помощник Парацельса, невежественный монах, решил, что минерал из России – застывшая кровь дьявола. Готовя составные части лекарств прокаливанием солей, полученных из “русского минерала”, монах всякий раз получал порошок красного цвета. Сиреневые кристаллы сульфата и нитрата железа (III), жёлтый хлорид железа (III) или почти белый карбонат железа (II) – все они при нагревании в токе воздуха превращались в “кровавик”. Бросив работу, монах стал повсюду рассказывать, что Парацельс связан с дьяволом. В адрес знаменитого врача посыпались угрозы, и ночью ему пришлось тайно покинуть Базель. Утром толпа горожан разгромила и сожгла его дом).
“Кровавик” - это минерал гематит Fe 2 O 3 . Соли железа при прокаливании разлагаются с выделением этого оксида красного цвета.)
2Fe 2 O 3 *3H 2 O – бурый железняк (лимонит);
FeS 2 – железный колчедан (пирит).
Помимо железа в состав этих минералов входят другие элементы. Природное химически чистое железо бывает только метеоритного происхождения (самый большой метеорит найден в 1920 г. в Юго – Западной Африке, вес 60 т., “Гоба”) (демонстрация коллекции минералов) (Cлайд 3).
Железо образует несколько рядов соединений, чтобы узнать какие мы должны с вами вспомнить, какова особенность строения атома железа и какие степени окисления характерны для железа?
Fe +26 2е, 8е, 14е, 2е
(Fe – элемент 7 группы побочной подгруппы, 4 периода (большой). Заполняется не последний, а предпоследний, 3-й от ядра энергетический уровень, где максимальное число электронов 18, у железа здесь 14 электронов. Железо восстановитель, как и другие металлы, однако в отличие от ранее изученных металлов, атомы железа при окислении отдают не только электроны последнего уровня, приобретая степень окисления +2, но способны к отдаче 1 электрона с предпоследнего энергетического уровня, принимая при этом степень окисления +3. Для железа характерны две основные степени окисления +2 и +3).
Проявляя степени окисления +2 и +3 железо образует 2 ряда соединений.
Соединения железа (+2).
Соединения железа (+2): FeO (оксид железа(II) и Fe(OH) 2 (гидроксид железа(II). Имеют ярко выраженный основный характер. Получают их косвенно. Рассмотрим генетический ряд Fe +2:
Соединения железа (+3).
Соединения железа (+3): Fe 2 О 3 (оксид железа(III)) и Fe(OH) 3 (гидроксид железа(III)). Имеют слабо выраженные амфотерные свойства. Получают их косвенно. Рассмотрим генетический ряд Fe +3:

Катионы железа (+2) легко окисляются кислородом воздуха или другими окислителями до катионов железа (+3). Поэтому белый осадок Fe(OH) 2 (гидроксид железа(II) на воздухе сначала приобретает зелёную окраску, а затем становится бурым, превращаясь в Fe(OH) 3 (гидроксид железа(III) (демонстрационный опыт
)
Соли железа (+2) и (+3).
Железо образует 2 ряда солей Fe +2 и Fe +3 . Для распознавания соединений железа (+2) и (+3) проводят качественные реакции на данные ионы (качественные реакции – это реакции с помощью которых распознают различные вещества, они сопровождаются ярким внешним эффектом).
Качественные реакции на Fe +2 .
Реактивом служит красная кровяная соль.

Качественные реакции на Fe +3.
Реактивом служит жёлтая кровяная соль.
Также для обнаружения ионов железа(III) используют взаимодействие солей железа(III) с роданидом калия или аммония, в результате чего раствор приобретает интенсивно-красное окрашивание.

Техника безопасности: необходимо брать вещества в количествах указанных учителем; при попадании данных химических реактивов на кожу или одежду необходимо смыть реактивы избытком воды; если что-нибудь попало в глаза – промыть водой в течение 10-15 минут.
(просмотр диска; демонстрация образцов солей; опыты учащихся) (Cлайд 4, 5).
Применение соединений железа
Железо выполняет функции кроветворных органов, входит в состав гемоглобина, других сложных белковых животных организмов. В виде чугуна и стали железо находит широкое применение в народном хозяйстве. Из солей железа наибольшее техническое значение имеют сульфаты и хлориды.
FeSO 4 *7H 2 O – железный купорос используется для борьбы с вредителями растений, для приготовления минеральных красок и т.д.;
FeCl 3 – используется как протрава при крашении тканей и в качестве катализатора в органическом синтезе;
Fe 2 (SO 4) 3 *9H 2 O – применяют для очистки воды, в виде квасцов в медицине.
(просмотр диска; демонстрация образцов солей)
На уроке мы с вами рассмотрели соединения железа (+2) и (+3). Познакомились с нахождением железа в природе: минералы магнетит, гематит, лимонит, пирит. Изучили соединения железа (+2) (FeO (оксид железа(II) и Fe(OH) 2 (гидроксид железа(II) и их свойства; соединения железа (+3) (Fe 2 О 3 (оксид железа(III) и Fe(OH) 3 (гидроксид железа(III), их свойства. Рассмотрели лёгкость окисления Fe +2 в Fe +3 кислородом воздуха. Узнали, что железо образует 2 ряда соединений:
Fe +2: реактивом служит красная кровяная соль, образуется тёмно-синий осадок (турнбулева синь);
Fe +3: реактивом служит
1) жёлтая кровяная соль, образуется тёмно-синее окрашивание (берлинская лазурь);
2) роданид калия или аммония, образуется интенсивно-красное окрашивание.
Рассмотрели применение соединений железа: в металлургии, медицине, при очистке воды, при окраске тканей, для борьбы с вредителями и в других отраслях народного хозяйства.
V. Закрепление.
Задача. Какая масса железа может быть получена при действии на 96 г оксида железа(III) избытка оксида углерода(II), если выход реакции составляет 80% от теоретически возможного? (Cлайд 6)

VI. Рефлексия.
Закончите предложения или дайте ответ на поставленный вопрос.
Мне больше всего понравилось…
Сегодня я узнал…
Было сложно…
Было интересно…
Теперь я могу…
Я попробовал…
Домашнее задание: учебник Габриелян О. С. п.14 (стр. 65-67); упр. 5,6 письменно (Cлайд 7).