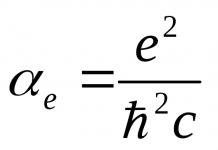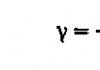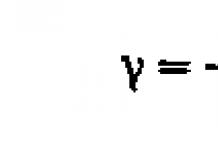Ковалентная связь — самый распространенный тип химической связи, осуществляемой при взаимодействии с одинаковыми или близкими значениями электроотрицательности.
Ковалентная связь — это связь атомов с помощью общих электронных пар.
После открытия электрона проводилось много попыток разработать электронную теорию химической связи. Наиболее удачными стали работы Льюиса (1916 г.), который предложил рассматривать образование связи как следствие возникновения общих для двух атомов электронных пар. Для этого каждый атом предоставляет одинаковое количество электронов и пытается окружить себя октетом или дублетом электронов, характерным для внешней электронной конфигурации инертных газов. Графически образования ковалентных связей за счет неспаренных электронов по методу Льюиса изображают с помощью точек, обозначающих внешние электроны атома.
Образование ковалентной связи согласно теории Льюиса
Механизм образования ковалентной связи
Основным признаком ковалентной связи является наличие общей электронной пары, принадлежащей обоим химически соединенным атомам, поскольку пребывание двух электронов в поле действия двух ядер энергетически выгоднее, чем нахождение каждого электрона в поле своего ядра. Возникновение общей электронной пары связи может проходить по разным механизмам, чаще — по обменному, а иногда — по донорно-акцепторных.
по принципу обменного механизма образования ковалентной связи каждый из взаимодействующих атомов поставляет на образование связи одинаковое количество электронов с антипараллельными спинами. К примеру:
 Общая схема образования ковалентной связи: а) по обменному механизму; б) по донорно-акцепторному механизму
Общая схема образования ковалентной связи: а) по обменному механизму; б) по донорно-акцепторному механизму
по донорно-акцепторному механизму двухэлектронная связь возникает при взаимодействии различных частиц. Одна из них — донор А: имеет неразделенную пару электронов (то есть такую, что принадлежит только одному атому), а другая — акцептор В — имеет вакантную орбиталь.
Частица, которая предоставляет для связи двухэлектронное (неразделенную пару электронов), называется донором, а частица со свободной орбиталью, которая принимает эту электронную пару, — акцептором.
Механизм образования ковалентной связи за счет двухэлектронного облака одного атома и вакантной орбитали другого называется донорно-акцепторным механизмом.
Донорно-акцепторный связь иначе называется семиполярной, поскольку на атоме-доноре возникает частичный эффективный положительный заряд δ+ (за счет того, что его неразделенная пара электронов отклонилась от него), а на атоме-акцепторе — частичный эффективный отрицательный заряд δ- (благодаря тому, что происходит смещение в его сторону неразделенной электронной пары донора).
В качестве примера простого донора электронной пары можно привести ион Н — , который имеет неразделенную электронную пару. В результате присоединения негативного гидрид-иона к молекуле, центральный атом которой имеет свободную орбиталь (на схеме обозначена как пустая квантовая ячейка), например ВН 3 , образуется сложный комплексный ион ВН 4 — с отрицательным зарядом (Н — + ВН 3 ⟶⟶ [ВН 4 ] —) :

Акцептор электронной пары — ион водорода, или просто протон Н + . Его присоединение к молекуле, центральный атом которой имеет неразделенную электронную пару, например к NH 3 , тоже приводит к образованию комплексного иона NH 4 + , но уже с положительным зарядом:

Метод валентных связей
Первая квантово-механическая теория ковалентной связи была создана Гейтлером и Лондоном (в 1927 г.) для описания молекулы водорода, а затем была применена Полингом к многоатомным молекулам. Эта теория называется методом валентных связей , основные положения которого кратко можно изложить так:
- каждая пара атомов в молекуле содержится вместе с помощью одной или нескольких общих электронных пар, при этом электронные орбитали взаимодействующих атомов перекрываются;
- прочность связи зависит от степени перекрывания электронных орбиталей;
- условием образования ковалентной связи является антинаправленность спинов электронов; благодаря этому возникает обобщенная электронная орбиталь с наибольшей электронной плотностью в межъядерном пространстве, которая обеспечивает притяжение положительно заряженных ядер друг к другу и сопровождается уменьшением общей энергии системы.
Гибридизация атомных орбиталей
Несмотря на то, что в образовании ковалентных связей участвуют электроны s-, p- или d-орбиталей, имеющие различные форму и различную ориентацию в пространстве, во многих соединениях эти связи оказываются равноценными. Для объяснения этого явления было введено понятие «гибридизация».
Гибридизация — это процесс смешивания и выравнивания орбиталей по форме и энергии, при котором происходит перераспределение электронных плотностей близких по энергии орбиталей, в результате чего они становятся равноценными.
Основные положения теории гибридизации:
- При гибридизации начальная форма и орбиталей взаимно меняются, при этом образуются новые, гибридизованные орбитали, но уже с одинаковой энергией и одинаковой формы, напоминающей неправильную восьмерку.
- Число гибридизованных орбиталей равно числу выходных орбиталей, участвующих в гибридизации.
- В гибридизации могут участвовать орбитали с близкими по значениям энергиями (s- и p-орбитали внешнего энергетического уровня и d-орбитали внешнего или предварительного уровней).
- Гибридизованные орбитали более вытянуты в направлении образования химических связей и поэтому обеспечивают лучшее перекрытие с орбиталями соседнего атома, вследствие этого становится более прочным, чем образованный за счет электронов отдельных негибридных орбиталей.
- Благодаря образованию более прочных связей и более симметричном распределения электронной плотности в молекуле получается энергетический выигрыш, который с запасом компенсирует расход энергии, необходимой для процесса гибридизации.
- Гибридизованные орбитали должны ориентироваться в пространстве таким образом, чтобы обеспечить взаимное максимальное отдаление друг от друга; в этом случае энергия отталкивания наименьшая.
- Тип гибридизации определяется типом и количеством выходных орбиталей и меняет размер валентного угла, а также пространственную конфигурацию молекул.
 Форма гибридизованных орбиталей и валентных углы (геометрические углы между осями симметрии орбиталей) в зависимости от типа гибридизации: а) sp-гибридизация; б) sp 2 -гибридизация; в) sp 3 -гибридизация
Форма гибридизованных орбиталей и валентных углы (геометрические углы между осями симметрии орбиталей) в зависимости от типа гибридизации: а) sp-гибридизация; б) sp 2 -гибридизация; в) sp 3 -гибридизация
При образовании молекул (или отдельных фрагментов молекул) чаще всего встречаются такие типы гибридизации:
 Общая схема sp-гибридизации
Общая схема sp-гибридизации
Связи, которые образуются с участием электронов sp-гибридизованнных орбиталей, также размещаются под углом 180 0 , что приводит к линейной форме молекулы. Такой тип гибридизации наблюдается в галогенидах элементов второй группы (Be, Zn, Cd, Hg), атомы которых в валентном состоянии имеют неспаренные s- и р-электроны. Линейная форма характерна и для молекул других элементов (0=C=0,HC≡CH), в которых связи образуются sp-гибридизованными атомами.
 Схема sp 2 -гибридизации атомных орбиталей и плоская треугольная форма молекулы, которая обусловлена sp 2 -гибридизацией атомных орбиталей
Схема sp 2 -гибридизации атомных орбиталей и плоская треугольная форма молекулы, которая обусловлена sp 2 -гибридизацией атомных орбиталей
Этот тип гибридизации наиболее характерен для молекул р-элементов третьей группы, атомы которых в возбужденном состоянии имеют внешнюю электронную структуру ns 1 np 2 , где n — номер периода, в котором находится элемент. Так, в молекулах ВF 3 , BCl 3 , AlF 3 и в других связи образованы за счет sp 2 -гибридизованных орбиталей центрального атома.
 Схема sp 3 -гибридизации атомных орбиталей
Схема sp 3 -гибридизации атомных орбиталей
Размещение гибридизованных орбиталей центрального атома под углом 109 0 28` вызывает тетраэдрическую форму молекул. Это очень характерно для насыщенных соединений четырехвалентного углерода СН 4 , СCl 4 , C 2 H 6 и других алканов. Примерами соединений других элементов с тетраэдрической строением вследствие sp 3 -гибридизации валентных орбиталей центрального атома является ионы: BН 4 — , BF 4 — , PO 4 3- , SO 4 2- , FeCl 4 — .
 Общая схема sp 3d -гибридизации
Общая схема sp 3d -гибридизации
Этот тип гибридизации чаще всего встречается в галогенидах неметаллов. В качестве примера можно привести строение хлорида фосфора PCl 5 , при образовании которого атом фосфора (P … 3s 2 3p 3) сначала переходит в возбужденное состояние (P … 3s 1 3p 3 3d 1), а затем подвергается s 1 p 3 d- гибридизации — пять одноэлектронных орбиталей становятся равноценными и ориентируются вытянутыми концами к углам мысленной тригональной бипирамиды. Это и определяет форму молекулы PCl 5 , которая образуется при перекрытии пяти s 1 p 3 d- гибридизованных орбиталей с 3р-орбиталями пяти атомов хлора.
- sp — Гибридизация. При комбинации одной s- i одной р-орбиталей возникают две sp-гибридизованные орбитали, расположенные симметрично под углом 180 0 .
- sp 2 — Гибридизация. Комбинация одной s- и двух р-орбиталей приводит к образованию sp 2 -гибридизованных связей, расположенных под углом 120 0 , поэтому молекула приобретает форму правильного треугольника.
- sp 3 — Гибридизация. Комбинация четырех орбиталей — одной s- и трех р приводит к sp 3 — гибридизации, при которой четыре гибридизованные орбитали симметрично ориентированы в пространстве к четырем вершинам тетраэдра, то есть под углом 109 0 28 `.
- sp 3 d — Гибридизация. Комбинация одной s-, трех р- и одной d- орбиталей дает sp 3 d- гибридизацию, что определяет пространственную ориентацию пяти sp 3 d-гибридизованных орбиталей к вершинам тригональной бипирамиды.
- Другие типы гибридизации. В случае sp 3 d 2 -гибридизации шесть sp 3 d 2 -гибридизованных орбиталей направлены к вершинам октаэдра. Ориентация семи орбиталей к вершинам пентагональной бипирамиды соответствует sp 3 d 3 -гибридизации (или иногда sp 3 d 2 f) валентных орбиталей центрального атома молекулы или комплекса.
Метод гибридизации атомных орбиталей объясняет геометрическую структуру большого количества молекул, однако согласно опытным данным чаще наблюдаются молекулы с несколько другими значениями валентных углов. Например, в молекулах СН 4 , NH 3 и Н 2 О центральные атомы находятся в sp 3 -гибридизованном состоянии, поэтому можно было бы ожидать, что валентные углы в них равны тетраэдрическим (~ 109,5 0). Экспериментально установлено, что валентный угол в молекуле СН 4 на самом деле составляет 109,5 0 . Однако в молекулах NH 3 и Н 2 O значение валентного угла отклоняется от тетраэдрического: он равен 107,3 0 в молекуле NH 3 и 104,5 0 в молекуле Н 2 О. Такие отклонения объясняется наличием неразделенной электронной пары у атомов азота и кислорода. Двухэлектронная орбиталь, которая содержит неразделенную пару электронов, благодаря повышенной плотности отталкивает одноэлектронные валентные орбитали, что приводит к уменьшению валентного угла. У атома азота в молекуле NH 3 из четырех sp 3 -гибридизованных орбиталей три одноэлектронные орбитали образуют связи с тремя атомами Н, а на четвертой орбитали содержится неразделенная пара электронов.
Несвязанная электронная пара, которая занимает одну из sp 3 -гибридизованных орбиталей, направленных к вершинам тетраэдра, отталкивая одноэлектронные орбитали, вызывает асимметричное распределение электронной плотности, окружающей атом азота, и как следствие сжимает валентный угол до 107,3 0 . Аналогичная картина уменьшения валентного угла от 109,5 0 до 107 0 в результате воздействия неразделенной электронной пары атома N наблюдается и в молекуле NCl 3 .
 Отклонение валентного угла от тетраэдрического (109,5 0) в молекуле: а) NН3 ; б) NCl3
Отклонение валентного угла от тетраэдрического (109,5 0) в молекуле: а) NН3 ; б) NCl3
У атома кислорода в молекуле Н 2 О на четыре sp 3 -гибридизованные орбитали приходится по две одноэлектронные и две двухэлектронные орбитали. Одноэлектронные гибридизованные орбитали участвуют в образовании двух связей с двумя атомами Н, а две двухэлектронные пары остаются неразделенными, то есть принадлежащими только атому H. Это увеличивает асимметричность распределения электронной плотности вокруг атома О и уменьшает валентный угол по сравнению с тетраэдрическим до 104.5 0 .
Следовательно, число несвязанных электронных пар центрального атома и их размещения на гибридизованных орбиталях влияет на геометрическую конфигурацию молекул.
Характеристики ковалентной связи
Ковалентная связь имеет набор определенных свойств, которые определяют ее специфические особенности, или характеристики. К ним, кроме уже рассмотренных характеристик «энергия связи» и «длина связи», относятся: валентный угол, насыщенность, направленность, полярность и тому подобное.
1. Валентный угол — это угол между соседними осями связей (то есть условными линиями, проведенными через ядра химически соединенных атомов в молекуле). Величина валентного угла зависит от природы орбиталей, типа гибридизации центрального атома, влияния неразделенных электронных пар, которые не участвуют в образовании связей.
2. Насыщенность . Атомы имеют возможности для образования ковалентных связей, которые могут формироваться, во-первых, по обменному механизму за счет неспаренных электронов невозбуждённого атома и за счет тех неспаренных электронов, которые возникают в результате его возбуждения, а во-вторых, по донорно акцепторному механизму. Однако общее количество связей, которые может образовывать атом, ограничено.
Насыщенность — это способность атома элемента образовывать с другими атомами определенное, ограниченное количество ковалентных связей.
Так, второго периода, которые имеют на внешнем энергетическом уровне четыре орбитали (одну s- и три р-), образуют связи, число которых не превышает четырех. Атомы элементов других периодов с большим числом орбиталей на внешнем уровне могут формировать больше связей.
3. Направленность . В соответствии с методом, химическая связь между атомами обусловлена перекрытием орбиталей, которые, за исключением s-орбиталей, имеют определенную ориентацию в пространстве, что и приводит к направленности ковалентной связи.
Направленность ковалентной связи — это такое размещение электронной плотности между атомами, которое определяется пространственной ориентацией валентных орбиталей и обеспечивает их максимальное перекрытие.
Поскольку электронные орбитали имеют различные формы и различную ориентацию в пространстве, то их взаимное перекрытие может реализоваться различными способами. В зависимости от этого различают σ-, π- и δ- связи.
Сигма-связь (σ-связь) — это такое перекрытие электронных орбиталей, при котором максимальная электронная плотность концентрируется вдоль воображаемой линии, соединяющей два ядра.
Сигма-связь может образовываться за счет двух s-электронов, одного s- и одного р электрона, двух р-электронов или двух d-электронов. Такая σ-связь характеризуется наличием одной области перекрытия электронных орбиталей, она всегда одинарная, то есть образуется только одной электронной парой.

Разнообразие форм пространственной ориентации «чистых» орбиталей и гибридизованных орбиталей не всегда допускают возможность перекрывания орбиталей на оси связи. Перекрывания валентных орбиталей может происходить по обе стороны от оси связи — так называемое «боковое» перекрывания, которое чаще всего осуществляется при образовании π-связей.
Пи-связь (π-связь) — это перекрытие электронных орбиталей, при котором максимальная электронная плотность концентрируется по обе стороны от линии, соединяющей ядра атомов (т.е. от оси связи).
Пи-связь может образоваться при взаимодействии двух параллельных р-орбиталей, двух d-орбиталей или других комбинаций орбиталей, оси которых не совпадают с осью связи.
 Схемы образования π-связей между условными А и В атомами при боковом перекрытии электронных орбиталей
Схемы образования π-связей между условными А и В атомами при боковом перекрытии электронных орбиталей
4. Кратность. Эта характеристика определяется числом общих электронных пар, связывающих атомы. Ковалентная связь по кратности может быть одинарной (простой), двойной и тройной. Связь между двумя атомами с помощью одной общей электронной пары называется одинарной связью (простой), двух электронных пар — двойной связью, трех электронных пар — тройной связью. Так, в молекуле водорода Н 2 атомы соединены одинарной связью (Н-Н), в молекуле кислорода О 2 — двойным (В = О), в молекуле азота N 2 — тройным (N≡N). Особое значение кратность связей приобретает в органических соединениях — углеводородах и их производных: в этане С 2 Н 6 между атомами С осуществляется одинарная связь (С-С), в этилене С 2 Н 4 — двойная (С = С) в ацетилене С 2 Н 2 — тройная (C ≡ C)(C≡C).
Кратность связи влияет на энергию: с повышением кратности растет ее прочность. Повышение кратности приводит к уменьшению межъядерного расстояния (длины связи) и увеличению энергии связи.
 Кратность связи между атомами углерода: а) одинарная σ-связь в этане Н3С-СН3 ; б) двойная σ+π-связь в этилене Н2С = СН2 ; в) тройная σ+π+π-связь в ацетилене HC≡CH
Кратность связи между атомами углерода: а) одинарная σ-связь в этане Н3С-СН3 ; б) двойная σ+π-связь в этилене Н2С = СН2 ; в) тройная σ+π+π-связь в ацетилене HC≡CH
5. Полярность и поляризуемость . Электронная плотность ковалентной связи может по-разному располагаться в межъядерном пространстве.
Полярность — это свойство ковалентной связи, которое определяется областью расположения электронной плотности в межъядерном пространстве относительно соединенных атомов.
В зависимости от размещения электронной плотности в межъядерном пространстве различают полярная и неполярная ковалентные связи. Неполярной связью называется такая связь, при которой общее электронное облако размещается симметрично относительно ядер соединенных атомов и одинаково принадлежит обоим атомам.
Молекулы с таким типом связи называются неполярными или гомоядерными (то есть такими, в состав которых входят атомы одного элемента). Неполярная связь проявляется как правило в гомоядерных молекулах (Н 2 , Cl 2 , N 2 и т.д.) или — реже — в соединениях, образованных атомами элементов с близкими значениями электроотрицательности, например, карборунд SiC. Полярной, (или гетерополярной) называется связь, при которой общее электронное облако несимметричное и смещено к одному из атомов.
Молекулы с полярной связью называются полярными, или гетероядерными. В молекулах с полярной связью обобщенная электронная пара смещается в сторону атома с большей электроотрицательностью. В результате на этом атоме возникает некоторый частичный отрицательный заряд (δ-), который называется эффективным, а у атома с меньшей электроотрицательностью — одинаковый по величине, но противоположный по знаку частичный положительный заряд (δ+). Например, экспериментально установлено, что эффективный заряд на атоме водорода в молекуле хлорида водорода HCl — δH=+0,17, а на атоме хлора δCl=-0,17 абсолютного заряда электрона.
Чтобы определить, в какую сторону будет смещаться электронная плотность полярной ковалентной связи, необходимо сравнить электроны обоих атомов. По возрастанию электроотрицательности наиболее распространенные химические элементы размещаются в такой последовательности:
Полярные молекулы называются диполями — системами, в которых центры тяжести положительных зарядов ядер и отрицательных зарядов электронов не совпадают.
Диполь — это система, которая представляет собой совокупность двух точечных электрических зарядов, одинаковых по величине и противоположных по знаку, находящихся на некотором расстоянии друг от друга.
Расстояние между центрами притяжения называются длина диполя и обозначаются буквой l. Полярность молекулы (или связи) количественно характеризуется дипольным моментом μ, который в случае двухатомной молекулы равен произведению длины диполя на величину заряда электрона: μ=el.
В единицах СИ дипольный момент измеряется в [Кл × м] (Кулон-метры), но чаще пользуются внесистемной единицей [D] (дебай): 1D = 3,33 · 10 -30 Кл × м. Значение дипольных моментов ковалентных молекул меняется в пределах 0-4 D, а ионных — 4-11D. Чем больше длина диполя, тем более полярной является молекула.
Совместная электронное облако в молекуле может смещаться под действием внешнего электрического поля, в том числе и поля другой молекулы или иона.
Поляризуемость — это изменение полярности связи в результате смещения электронов, образующих связь, под действием внешнего электрического поля, в том числе и силового поля другой частицы.
Поляризуемость молекулы зависит от подвижности электронов, которая является тем сильнее, чем больше расстояние от ядер. Кроме того, поляризуемость зависит от направленности электрического поля и от способности электронных облаков деформироваться. Под действием внешнего поля неполярные молекулы становятся полярными, а полярные — еще более полярными, то есть в молекулах индуцируется диполь, который называется приведенным, или индуцированным диполем.
 Схема образования индуцированного (приведенного) диполя из неполярной молекулы под действием силового поля полярной частицы — диполя
Схема образования индуцированного (приведенного) диполя из неполярной молекулы под действием силового поля полярной частицы — диполя
В отличие от постоянных, индуцированные диполи возникают лишь при действии внешнего электрического поля. Поляризация может вызывать не только поляризуемость связи, но и ее разрыв, при котором происходит переход связующего электронной пары к одному из атомов и образуются отрицательно и положительно заряженные ионы.
Полярность и поляризуемость ковалентных связей определяет реакционную способность молекул по отношению к полярным реагентам.
Свойства соединений с ковалентной связью
Вещества с ковалентными связями делятся на две неравные группы: молекулярные и атомные (или немолекулярные), которых значительно меньше, чем молекулярных.
Молекулярные соединения в обычных условиях могут находиться в различных агрегатных состояниях: в виде газов (CO 2 , NH 3 , CH 4 , Cl 2 , O 2 , NH 3), легколетучих жидкостей (Br 2 , H 2 O, C 2 H 5 OH) или твердых кристаллических веществ, большинство из которых даже при очень незначительном нагревании способны быстро плавиться и легко сублимироваться (S 8 , P 4 , I 2 , сахар С 12 Н 22 О 11 , «сухой лед» СО 2).
Низкие температуры плавления, возгонки и кипения молекулярных веществ объясняются очень слабыми силами межмолекулярного взаимодействия в кристаллах. Именно поэтому для молекулярных кристаллов не присуща большая прочность, твердость и электрическая проводимость (лед или сахар). При этом вещества с полярными молекулами имеют более высокие температуры плавления и кипения, чем с неполярными. Некоторые из них растворимы в или других полярных растворителях. А вещества с неполярными молекулами, наоборот, лучше растворяются в неполярных растворителях (бензол, тетрахлорметан). Так, йод, у которого молекулы неполярные, не растворяется в полярной воде, но растворяется в неполярной CCl 4 и малополярном спирте.
Немолекулярные (атомные) вещества с ковалентными связями (алмаз, графит, кремний Si, кварц SiO 2 , карборунд SiC и другие) образуют чрезвычайно прочные кристаллы, за исключением графита, которого имеет слоистую структуру. Например, кристаллическая решетка алмаза — правильный трехмерный каркас, в котором каждый sр 3 -гибридизованный атом углерода соединен с четырьмя соседними атомами С σ-связями. По сути весь кристалл алмаза — это одна огромная и очень прочная молекула. Аналогичное строение имеют и кристаллы кремния Si, который широко применяется в радиоэлектронике и электронной технике. Если заменить половину атомов С в алмазе атомами Si, не нарушая каркасную структуру кристалла, то получим кристалл карборунда — карбида кремния SiC — очень твердого вещества, используемого в качестве абразивного материала. А если в кристаллической решетке кремния между каждыми двумя атомами Si вставить по атому О, то образуется кристаллическая структура кварца SiO 2 — тоже очень твердого вещества, разновидность которого также используют как абразивный материал.
Кристаллы алмаза, кремния, кварца и подобные им по структуре — это атомные кристаллы, они представляют собой огромные «супермолекулы», поэтому их структурные формулы можно изобразить не полностью, а только в виде отдельного фрагмента, например:
 Кристаллы алмаза, кремния, кварца
Кристаллы алмаза, кремния, кварца
Немолекулярные (атомные) кристаллы, состоящие из соединенных между собой химическими связями атомов одного или двух элементов, относятся к тугоплавким веществам. Высокие температуры плавления обусловлены необходимостью затраты большого количества энергии для разрыва прочных химических связей при плавлении атомных кристаллов, а не слабого межмолекулярного взаимодействия, как в случае молекулярных веществ. По этой же причине многие атомные кристаллов при нагревании не плавятся, а разлагаются или сразу переходят в парообразное состояние (возгонка), например, графит сублимируется при 3700 o С.
Немолекулярные вещества с ковалентными связями нерастворимые в воде и других растворителях, большинство из них не проводит электрический ток (кроме графита, которому присуща электропроводность, и полупроводников — кремния, германия и др.).
Длиной ковалентной связи называют расстояние между ядрами атомов, которые образуют связь. Длина связи напрямую связана с радиусом атома - чем он больше, тем длиннее связь.
Значения ковалентных радиусов некоторых атомов (пм; 10 -12 м):
- H = 30 пм;
- F = 58;
- O = 73;
- N = 75;
- C = 77;
- Cl = 99;
- S = 103;
- P = 110;
- Si = 118;
- Al = 130.
В симметричных молекулах (H 2 , F 2 , Cl 2 ...) половину длины связи называют ковалентным радиусом . Зная ковалентный радиус, очень легко вычислять длину ковалентной связи в молекуле. Например, длина ковалентной связи молекулы HF = 30 + 58 = 88 пм.
2. Энергия ковалентной связи
Под энергией ковалентной связи (выражают в ккал/моль или кДж/моль) обычно понимают энергию, которая необходима для разрыва связи (при образовании ковалентной связи энергия выделяется, при разрыве - поглощается). Чем выше энергия связи, тем прочнее связь.
Энергия связи зависит от ее длины - чем длиннее связь в молекуле, тем проще ее разорвать (затратить меньше энергии).
Энергии связи некоторых молекул (кДж/моль):
- H 2 = 453 (длина связи = 60 пм);
- Cl 2 = 242 (198 пм);
- HCl = 431 (129 пм).
3. Полярность ковалентной связи
Данная характеристика отображает расположение электронной пары двух атомов, образующих связь. Степень полярности связи зависит от величины электроотрицательности атомов, образующих связь (чем она больше, тем больше полярность связи). У более полярной ковалентной связи общая пара электронов больше смещена к более электроотрицательному атому (см. понятие электроотрицательности).
Электроотрицателность является табличной величиной, определяемой по шкале Поллинга. Гораздо более важно знать не саму электроотрицательность атома как таковую, но разницу этих значений в молекуле - какой из атомов более электроотрицателен, а какой менее.
Полярность ковалентной связи оценивается количественно при помощи дипольного момента (µ), при этом система из двух равнозначных, но противоположных по знаку, зарядов, называется диполем .
Очень важно различать дипольный момент ковалентной связи (ее полярность) и дипольный момент молекулы в целом. В простых двухатомных молекулах эти два параметра равны между собой. Совсем другая картина наблюдается в сложных молекулах, в которых дипольный момент молекулы складывается из суммы векторов дипольных моментов отдельных связей.
4. Поляризуемость ковалентной связи
Поляризуемость отображает степень способности электронов смещаться под воздействием внешнего электрического поля, формируемого ионами или другими полярными молекулами.
Поляризуемость ковалентной связи прямо пропорциональна ее длине, что, в общем-то, логично - чем дальше от ядра атома находится электрон, тем он слабее им притягивается, поэтому, легче смещается при внешнем воздействии на него. Таким образом, с увеличением длины связи происходит увеличение ее поляризуемости, что, в свою очередь, приводит к возрастанию силы кислот (например, йодистоводородная кислота сильнее фтороводородной).
Поляризуемость и полярность связи являются обратнозависимыми величинами: менее полярная связь больше поляризуется, и наоборот.
5. Насыщаемость ковалентной связи
Насыщаемостью называют способность атома образовывать определенное кол-во ковалентных связей - в образовании связи стремятся принять участие все "неспаренные" электроны атома. Например, атом водорода имеет только один неспаренный электрон, а атом азота - три. По этой причине наиболее устойчивым химическим соединением будет NH 3 , но не NH или NH 2 .
6. Направленность ковалентной связи
Направленность характеризует пространственную ориентацию ковалентной связи относительно других связей молекулы. В молекулах электроны ковалентных связей и свободные пары электронов постоянно испытывают взаимное отталкивание в результате чего ковалентные связи располагаются так, что валентный угол между ними отвечает принципу наименьшего отталкивания между электронами (например, в молекуле воды валентный угол составляет 104,5°).
7. Кратность ковалентной связи
В некоторых случаях между атомами могут возникать не одна, а две (двойная связь) или три (тройная связь) общих электронных пар (так называемые кратные связи).
Двойная ковалентная связь образуется у атомов, имеющих по два неспаренных электрона; тройная - у атомов, имеющих по три неспаренных электрона (см. Множественные связи).
Как видно из таблицы, приведенной ниже, молекула азота примерно в 7 раз "крепче" молекулы фтора.
Таблица зависимости длины и прочности ковалентной связи от ее кратности.
Крайне редко химические вещества состоят из отдельных, не связанных между собой атомов химических элементов. Таким строением в обычных условиях обладает лишь небольшой ряд газов называемых благородными: гелий, неон, аргон, криптон, ксенон и радон. Чаще же всего химические вещества состоят не из разрозненных атомов, а из их объединений в различные группировки. Такие объединения атомов могут насчитывать несколько единиц, сотен, тысяч или даже больше атомов. Сила, которая удерживает эти атомы в составе таких группировок, называется химическая связь .
Другими словами, можно сказать, что химической связью называют взаимодействие, которое обеспечивает связь отдельных атомов в более сложные структуры (молекулы, ионы, радикалы, кристаллы и др.).
Причиной образования химической связи является то, что энергия более сложных структур меньше суммарной энергии отдельных, образующих ее атомов.
Так, в частности, если при взаимодействии атомов X и Y образуется молекула XY, это означает, что внутренняя энергия молекул этого вещества ниже, чем внутренняя энергия отдельных атомов, из которых оно образовалось:
E(XY) < E(X) + E(Y)
По этой причине при образовании химических связей между отдельными атомами выделятся энергия.
В образовании химических связей принимают участие электроны внешнего электронного слоя с наименьшей энергией связи с ядром, называемые валентными . Например, у бора таковыми являются электроны 2 энергетического уровня – 2 электрона на 2s- орбитали и 1 на 2p -орбитали:
При образовании химической связи каждый атом стремится получить электронную конфигурацию атомов благородных газов, т.е. чтобы в его внешнем электронном слое было 8 электронов (2 для элементов первого периода). Это явление получило название правила октета.
Достижение атомами электронной конфигурации благородного газа возможно, если изначально одиночные атомы сделают часть своих валентных электронов общими для других атомов. При этом образуются общие электронные пары.
В зависимости от степени обобществления электронов можно выделить ковалентную, ионную и металлическую связи.
Ковалентная связь
Ковалентная связь возникает чаще всего между атомами элементов неметаллов. Если атомы неметаллов, образующие ковалентную связь, относятся к разным химическим элементам, такую связь называют ковалентной полярной. Причина такого названия кроется в том, что атомы разных элементов имеют и различную способность притягивать к себе общую электронную пару. Очевидно, что это приводит к смещению общей электронной пары в сторону одного из атомов, в результате чего на нем формируется частичный отрицательный заряд. В свою очередь, на другом атоме формируется частичный положительный заряд. Например, в молекуле хлороводорода электронная пара смещена от атома водорода к атому хлора:
Примеры веществ с ковалентной полярной связью:
СCl 4 , H 2 S, CO 2 , NH 3 , SiO 2 и т.д.
Ковалентная неполярная связь образуется между атомами неметаллов одного химического элемента. Поскольку атомы идентичны, одинакова и их способность оттягивать на себя общие электроны. В связи с этим смещения электронной пары не наблюдается:
Вышеописанный механизм образования ковалентной связи, когда оба атома предоставляют электроны для образования общих электронных пар, называется обменным.
Также существует и донорно-акцепторный механизм.
При образовании ковалентной связи по донорно-акцепторному механизму общая электронная пара образуется за счет заполненной орбитали одного атома (с двумя электронами) и пустой орбитали другого атома. Атом, предоставляющий неподеленную электронную пару, называют донором, а атом со свободной орбиталью – акцептором. В качестве доноров электронных пар выступают атомы, имеющие спаренные электроны, например N, O, P, S.
Например, по донорно-акцепторному механизму происходит образование четвертой ковалентной связи N-H в катионе аммония NH 4 + :
Помимо полярности ковалентные связи также характеризуются энергией. Энергией связи называют минимальную энергию, необходимую для разрыва связи между атомами.
Энергия связи уменьшается с ростом радиусов связываемых атомов. Так, как мы знаем, атомные радиусы увеличиваются вниз по подгруппам, можно, например, сделать вывод о том, что прочность связи галоген-водород увеличивается в ряду:
HI < HBr < HCl < HF
Также энергия связи зависит от ее кратности – чем больше кратность связи, тем больше ее энергия. Под кратностью связи понимается количество общих электронных пар между двумя атомами.
Ионная связь
Ионную связь можно рассматривать как предельный случай ковалентной полярной связи. Если в ковалентной-полярной связи общая электронная пара смещена частично к одному из пары атомов, то в ионной она практически полностью «отдана» одному из атомов. Атом, отдавший электрон(ы), приобретает положительный заряд и становится катионом , а атом, забравший у него электроны, приобретает отрицательный заряд и становится анионом .
Таким образом, ионная связь — это связь, образованная за счет электростатического притяжения катионов к анионам.
Образование такого типа связи характерно при взаимодействии атомов типичных металлов и типичных неметаллов.
Например, фторид калия. Катион калия получается в результате отрыва от нейтрального атома одного электрона, а ион фтора образуется при присоединении к атому фтора одного электрона:

Между получившимися ионами возникает сила электростатического притяжения, в результате чего образуется ионное соединение.
При образовании химической связи электроны от атома натрия перешли к атому хлора и образовались противоположно заряженные ионы, которые имеют завершенный внешний энергетический уровень.
Установлено, что электроны от атома металла не отрываются полностью, а лишь смещаются в сторону атома хлора, как в ковалентной связи.
Большинство бинарных соединений, которые содержат атомы металлов, являются ионными. Например, оксиды, галогениды, сульфиды, нитриды.
Ионная связь возникает также между простыми катионами и простыми анионами (F − , Cl − , S 2-), а также между простыми катионами и сложными анионами (NO 3 − , SO 4 2- , PO 4 3- , OH −). Поэтому к ионным соединениям относят соли и основания (Na 2 SO 4 , Cu(NO 3) 2 , (NH 4) 2 SO 4), Ca(OH) 2 , NaOH)
Металлическая связь
Данный тип связи образуется в металлах.
У атомов всех металлов на внешнем электронном слое присутствуют электроны, имеющие низкую энергию связи с ядром атома. Для большинства металлов, энергетически выгодным является процесс потери внешних электронов.
Ввиду такого слабого взаимодействия с ядром эти электроны в металлах весьма подвижны и в каждом кристалле металла непрерывно происходит следующий процесс:
М 0 — ne − = M n + ,
где М 0 – нейтральный атом металла, а M n + катион этого же металла. На рисунке ниже представлена иллюстрация происходящих процессов.
То есть по кристаллу металла «носятся» электроны, отсоединяясь от одного атома металла, образуя из него катион, присоединяясь к другому катиону, образуя нейтральный атом. Такое явление получило название “электронный ветер”, а совокупность свободных электронов в кристалле атома неметалла назвали “электронный газ”. Подобный тип взаимодействия между атомами металлов назвали металлической связью.
Водородная связь
Если атом водорода в каком-либо веществе связан с элементом с высокой электроотрицательностью (азотом, кислородом или фтором), для такого вещества характерно такое явление, как водородная связь.
Поскольку атом водорода связан с электроотрицательным атомом, на атоме водорода образуется частичный положительный заряд, а на атоме электроотрицательного элемента — частичный отрицательный. В связи с этим становится возможным электростатическое притяжения между частично положительно заряженным атомом водорода одной молекулы и электроотрицательным атомом другой. Например водородная связь наблюдается для молекул воды:
Именно водородной связью объясняется аномально высокая температура плавления воды. Кроме воды, также прочные водородные связи образуются в таких веществах, как фтороводород, аммиак, кислородсодержащие кислоты, фенолы, спирты, амины.
Темы кодификатора ЕГЭ: Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь
Внутримолекулярные химические связи
Сначала рассмотрим связи, которые возникают между частицами внутри молекул. Такие связи называют внутримолекулярными .
Химическая связь между атомами химических элементов имеет электростатическую природу и образуется за счет взаимодействия внешних (валентных) электронов , в большей или меньшей степени удерживаемых положительно заряженными ядрами связываемых атомов.
Ключевое понятие здесь – ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ . Именно она определяет тип химической связи между атомами и свойства этой связи.
– это способность атома притягивать (удерживать) внешние (валентные) электроны . Электроотрицательность определяется степенью притяжения внешних электронов к ядру и зависит, преимущественно, от радиуса атома и заряда ядра.
Электроотрицательность сложно определить однозначно. Л.Полинг составил таблицу относительных электроотрицательностей (на основе энергий связей двухатомных молекул). Наиболее электроотрицательный элемент – фтор со значением 4 .
Важно отметить, что в различных источниках можно встретить разные шкалы и таблицы значений электроотрицательности. Этого не стоит пугаться, поскольку при образовании химической связи играет роль атомов, а она примерно одинакова в любой системе.
Если один из атомов в химической связи А:В сильнее притягивает электроны, то электронная пара смещается к нему. Чем больше разность электроотрицательностей атомов, тем сильнее смещается электронная пара.
Если значения электроотрицательностей взаимодействующих атомов равны или примерно равны: ЭО(А)≈ЭО(В) , то общая электронная пара не смещается ни к одному из атомов: А: В . Такая связь называется ковалентной неполярной.
Если электроотрицательности взаимодействующих атомов отличаются, но не сильно (разница электроотрицательностей примерно от 0,4 до 2: 0,4<ΔЭО<2 ), то электронная пара смещается к одному из атомов. Такая связь называется ковалентная полярная .
Если электроотрицательности взаимодействующих атомов отличаются существенно (разница электроотрицательностей больше 2: ΔЭО>2 ), то один из электронов практически полностью переходит к другому атому, с образованием ионов . Такая связь называется ионная .
Основные типы химических связей — ковалентная , ионная и металлическая связи. Рассмотрим их подробнее.
Ковалентная химическая связь
Ковалентная связь – этохимическая связь, образованная за счет образования общей электронной пары А:В . При этом у двух атомов перекрываются атомные орбитали. Ковалентная связь образуется при взаимодействии атомов с небольшой разницей электроотрицательностей (как правило, между двумя неметаллами ) или атомов одного элемента.
Основные свойства ковалентных связей
- направленность ,
- насыщаемость ,
- полярность ,
- поляризуемость .
Эти свойства связи влияют на химические и физические свойства веществ.
Направленность связи характеризует химическое строение и форму веществ. Углы между двумя связями называются валентными. Например, в молекуле воды валентный угол H-O-H равен 104,45 о, поэтому молекула воды — полярная, а в молекуле метана валентный угол Н-С-Н 108 о 28′.

Насыщаемость — это спосбность атомов образовывать ограниченное число ковалентных химических связей. Количество связей, которые способен образовывать атом, называется .
Полярность связи возникает из-за неравномерного распределения электронной плотности между двумя атомами с различной электроотрицательностью. Ковалентные связи делят на полярные и неполярные.
Поляризуемость связи — это способность электронов связи смещаться под действием внешнего электрического поля (в частности, электрического поля другой частицы). Поляризуемость зависит от подвижности электронов. Чем дальше электрон находится от ядра, тем он более подвижен, соответственно и молекула более поляризуема.

Ковалентная неполярная химическая связь
Существует 2 вида ковалентного связывания – ПОЛЯРНЫЙ и НЕПОЛЯРНЫЙ .
Пример . Рассмотрим строение молекулы водорода H 2 . Каждый атом водорода на внешнем энергетическом уровне несет 1 неспаренный электрон. Для отображения атома используем структуру Льюиса – это схема строения внешнего энергетического уровня атома, когда электроны обозначаются точками. Модели точечных структур Люьиса неплохо помогают при работе с элементами второго периода.
H . + . H = H:H
Таким образом, в молекуле водорода одна общая электронная пара и одна химическая связь H–H. Эта электронная пара не смещается ни к одному из атомов водорода, т.к. электроотрицательность у атомов водорода одинаковая. Такая связь называется ковалентной неполярной .

Ковалентная неполярная (симметричная) связь – это ковалентная связь, образованная атомами с равной элетроотрицательностью (как правило, одинаковыми неметаллами) и, следовательно, с равномерным распределением электронной плотности между ядрами атомов.
Дипольный момент неполярных связей равен 0.
Примеры : H 2 (H-H), O 2 (O=O), S 8 .
Ковалентная полярная химическая связь
Ковалентная полярная связь – это ковалентная связь, которая возникает между атомами с разной электроотрицательностью (как правило, разными неметаллами ) и характеризуется смещением общей электронной пары к более электроотрицательному атому (поляризацией).
Электронная плотность смещена к более электроотрицательному атому – следовательно, на нем возникает частичный отрицательный заряд (δ-), а на менее электроотрицательном атоме возникает частичный положительный заряд (δ+, дельта +).
Чем больше различие в электроотрицательностях атомов, тем выше полярность связи и тем больше дипольный момент . Между соседними молекулами и противоположными по знаку зарядами действуют дополнительные силы притяжения, что увеличивает прочность связи.
Полярность связи влияет на физические и химические свойства соединений. От полярности связи зависят механизмы реакций и даже реакционная способность соседних связей. Полярность связи зачастую определяет полярность молекулы и, таким образом, непосредственно влияет на такие физические свойства как температуре кипения и температура плавления, растворимость в полярных растворителях.
Примеры: HCl, CO 2 , NH 3 .
Механизмы образования ковалентной связи
Ковалентная химическая связь может возникать по 2 механизмам:
1. Обменный механизм образования ковалентной химической связи – это когда каждая частица предоставляет для образования общей электронной пары один неспаренный электрон:
А . + . В= А:В
2. образования ковалентной связи – это такой механизм, при котором одна из частиц предоставляет неподеленную электронную пару, а другая частица предоставляет вакантную орбиталь для этой электронной пары:
А: + B= А:В

При этом один из атомов предоставляет неподеленную электронную пару (донор ), а другой атом предоставляет вакантную орбиталь для этой пары (акцептор ). В результате образования связи оба энергия электронов уменьшается, т.е. это выгодно для атомов.
Ковалентная связь, образованная по донорно-акцепторному механизму, не отличается по свойствам от других ковалентных связей, образованных по обменному механизму. Образование ковалентной связи по донорно-акцепторному механизму характерно для атомов либо с большим числом электронов на внешнем энергетическом уровне (доноры электронов), либо наоборот, с очень малым числом электронов (акцепторы электронов). Более подробно валентные возможности атомов рассмотрены в соответствующей .
Ковалентная связь по донорно-акцепторному механизму образуется:
– в молекуле угарного газа CO (связь в молекуле – тройная, 2 связи образованы по обменному механизму, одна – по донорно-акцепторному): C≡O;
– в ионе аммония NH 4 + , в ионах органических аминов , например, в ионе метиламмония CH 3 -NH 2 + ;
– в комплексных соединениях , химическая связь между центральным атомом и группами лигандов, например, в тетрагидроксоалюминате натрия Na связь между алюминием и гидроксид-ионами;
– в азотной кислоте и ее солях — нитратах: HNO 3 , NaNO 3 , в некоторых других соединениях азота;

– в молекуле озона O 3 .
Основные характеристики ковалентной связи
Ковалентная связь, как правило, образуется между атомами неметаллов. Основными характеристиками ковалентной связи являются длина, энергия, кратность и направленность.
Кратность химической связи
Кратность химической связи — это число общих электронных пар между двумя атомами в соединении . Кратность связи достаточно легко можно определить из значения атомов, образующих молекулу.
Например , в молекуле водорода H 2 кратность связи равна 1, т.к. у каждого водорода только 1 неспаренный электрон на внешнем энергетическом уровне, следовательно, образуется одна общая электронная пара.
В молекуле кислорода O 2 кратность связи равна 2, т.к. у каждого атома на внешнем энергетическом уровне есть по 2 неспаренных электрона: O=O.
В молекуле азота N 2 кратность связи равна 3, т.к. между у каждого атома по 3 неспаренных электрона на внешнем энергетическом уровне, и атомы образуют 3 общие электронные пары N≡N.
Длина ковалентной связи
Длина химической связи
– это расстояние между центрами ядер атомов, образующих связь. Ее определяют экспериментальными физическими методами. Оценить величину длины связи можно примерно, по правилу аддитивности, согласно которому длина связи в молекуле АВ приблизительно равна полусумме длин связей в молекулах А 2 и В 2:
Длину химической связи можно примерно оценить по радиусам атомов , образующих связь, или по кратности связи , если радиусы атомов не сильно отличаются.
При увеличении радиусов атомов, образующих связь, длина связи увеличится.
Например
При увеличении кратности связи между атомами (атомные радиусы которых не отличаются, либо отличаются незначительно) длина связи уменьшится.
Например . В ряду: C–C, C=C, C≡C длина связи уменьшается.
Энергия связи
Мерой прочности химической связи является энергия связи. Энергия связи определяется энергией, необходимой для разрыва связи и удаления атомов, образующих эту связь, на бесконечно большое расстояние друг от друга.
Ковалентная связь является очень прочной. Ее энергия составляет от нескольких десятков до нескольких сотен кДж/моль. Чем больше энергия связи, тем больше прочность связи, и наоборот.
Прочность химической связи зависит от длины связи, полярности связи и кратности связи. Чем длиннее химическая связь, тем легче ее разорвать, и тем меньше энергия связи, тем ниже ее прочность. Чем короче химическая связь, тем она прочнее, и тем больше энергия связи.
Например , в ряду соединений HF, HCl, HBr слева направо прочность химической связи уменьшается , т.к. увеличивается длина связи.
Ионная химическая связь

Ионная связь — это химическая связь, основанная на электростатическом притяжении ионов .
Ионы образуются в процессе принятия или отдачи электронов атомами. Например, атомы всех металлов слабо удерживают электроны внешнего энергетического уровня. Поэтому для атомов металлов характерны восстановительные свойства — способность отдавать электроны.

Пример . Атом натрия содержит на 3 энергетическом уровне 1 электрон. Легко отдавая его, атом натрия образует гораздо более устойчивый ион Na + , с электронной конфигурацией благородного газа неона Ne. В ионе натрия содержится 11 протонов и только 10 электронов, поэтому суммарный заряд иона -10+11 = +1:
+11Na ) 2 ) 8 ) 1 — 1e = +11Na +) 2 ) 8
Пример . Атом хлора на внешнем энергетическом уровне содержит 7 электронов. Чтобы приобрести конфигурацию стабильного инертного атома аргона Ar, хлору необходимо присоединить 1 электрон. После присоединения электрона образуется стабильный ион хлора, состоящий из электронов. Суммарный заряд иона равен -1:
+17Cl ) 2 ) 8 ) 7 + 1e = +17Cl — ) 2 ) 8 ) 8
Обратите внимание:
- Свойства ионов отличаются от свойств атомов!
- Устойчивые ионы могут образовывать не только атомы , но и группы атомов . Например: ион аммония NH 4 + , сульфат-ион SO 4 2- и др. Химические связи, образованные такими ионами, также считаются ионными;
- Ионную связь, как правило, образуют между собой металлы и неметаллы (группы неметаллов);
Образовавшиеся ионы притягиваются за счет электрического притяжения: Na + Cl — , Na 2 + SO 4 2- .
Наглядно обобщим различие между ковалентными и ионным типами связи :


Металлическая связь — это связь, которую образуют относительно свободные электроны между ионами металлов , образующих кристаллическую решетку.
У атомов металлов на внешнем энергетическом уровне обычно расположены от одного до трех электронов . Радиусы у атомов металлов, как правило, большие — следовательно, атомы металлов, в отличие от неметаллов, достаточно легко отдают наружные электроны, т.е. являются сильными восстановителями .
Отдавая электроны, атомы металлов превращаются в положительно заряженные ионы . Оторвавшиеся электроны относительно свободно перемещаются между положительно заряженными ионами металлов. Между этими частицами возникает связь , т.к. общие электроны удерживают катионы металлов, расположенные слоями, вместе , создавая таким образом достаточно прочную металлическую кристаллическую решетку . При этом электроны непрерывно хаотично двигаются, т.е. постоянно возникают новые нейтральные атомы и новые катионы.

Межмолекулярные взаимо-действия
Отдельно стоит рассмотреть взаимодействия, возникающие между отдельными молекулами в веществе — межмолекулярные взаимодействия . Межмолекулярные взаимодействия — это такой вид взаимодействия между нейтральными атомами, при котором не появляеются новые ковалентные связи. Силы взаимодействия между молекулами обнаружены Ван-дер Ваальсом в 1869 году, и названы в честь него Ван-дар-Ваальсовыми силами . Силы Ван-дер-Ваальса делятся на ориентационные , индукционные и дисперсионные . Энергия межмолекулярных взаимодейстий намного меньше энергии химической связи.
Ориентационные силы притяжения возникают между полярными молекулами (диполь-диполь взаимодействие). Эти силы возникают между полярными молекулами. Индукционные взаимодействия — это взаимодействие между полярной молекулой и неполярной. Неполярная молекула поляризуется из-за действия полярной, что и порождает дополнительное электростатическое притяжение.
Особый вид межмолекулярного взаимодействия — водородные связи. — это межмолекулярные (или внутримолекулярные) химические связи, возникающие между молекулами, в которых есть сильно полярные ковалентные связи — H-F, H-O или H-N . Если в молекуле есть такие связи, то между молекулами будут возникать дополнительные силы притяжения .
Механизм образования водородной связи частично электростатический, а частично — донорно–акцепторный. При этом донором электронной пары выступают атом сильно электроотрицательного элемента (F, O, N), а акцептором — атомы водорода, соединенные с этими атомами. Для водородной связи характерны направленность в пространстве и насыщаемость .
Водородную связь можно обозначать точками: Н ··· O. Чем больше электроотрицательность атома, соединенного с водородом, и чем меньше его размеры, тем крепче водородная связь . Она характерна прежде всего для соединений фтора с водородом , а также кислорода с водородом , в меньшей степени азота с водородом .

Водородные связи возникают между следующими веществами:
— фтороводород HF (газ, раствор фтороводорода в воде — плавиковая кислота), вода H 2 O (пар, лед, жидкая вода):
— раствор аммиака и органических аминов — между молекулами аммиака и воды;
— органические соединения, в которых связи O-H или N-H : спирты, карбоновые кислоты, амины, аминокислоты, фенолы, анилин и его производные, белки, растворы углеводов — моносахаридов и дисахаридов.
Водородная связь оказывает влияние на физические и химические свойства веществ. Так, дополнительное притяжение между молекулами затрудняет кипение веществ. У веществ с водородными связями наблюдается аномальное повышение тепературы кипения.
Например , как правило, при повышении молекулярной массы наблюдается повышение температуры кипения веществ. Однако в ряду веществ H 2 O-H 2 S-H 2 Se-H 2 Te мы не наблюдаем линейное изменение температур кипения.

А именно, у воды температура кипения аномально высокая — не меньше -61 о С, как показывает нам прямая линия, а намного больше, +100 о С. Эта аномалия объясняется наличием водородных связей между молекулами воды. Следовательно, при обычных условиях (0-20 о С) вода является жидкостью по фазовому состоянию.
1. Пространственная направленность . Если электронные облака перекрываются в направлении прямой, которая соединяет ядра атомов, такая связь называется s-связью (s–s-перекрывание Н 2 , р–рCl 2 , s–рHC1).
При перекрывании p-орбиталей, направленных перпендикулярно оси связи, образуются две области перекрывания по обе стороны оси связи. Такая ковалентная связь называется p-связью. Например, в молекуле азота атомы связаны одной s-связью и двумя p-связями.
Направленность связи определяет пространственную структуру молекул, т. е. их форму и характеризуется наличием строго определенного угла между связями. Например, угол между s-связями в молекуле воды равен 104,5°.

2. Полярность связи определяется асимметрией в распределении общего электронного облака вдоль оси связи.
Если общие электронные пары располагаются симметрично относительно обоих ядер, то такая ковалентная связь называется неполярной.
Если общие электронные пары смещаются к одному из атомов (располагаются несимметрично относительно ядер различных атомов), то такая ковалентная связь называется полярной.
В случае, когда электронная пара смещается в сторону более электроотрицательного атома центры (+) и (–) зарядов не совпадают, и возникает система (электрический диполь) из двух равных по величине, но противоположных по знаку зарядов, расстояние между которыми (l
) называют длиной диполя. Мерой полярности молекул является электрический момент диполя
m, равный произведению абсолютного значения заряда электрона
(q = 1,6 × 10 –19 Кл) на длину диполя l
:
m = q×l .
Единицей измерения m является дебай D, 1 D = 3,33×10 –30 Кл×м.
Задание. Длина диполя молекулы HCl равна 2,2×10 –9 см. Вычислить электрический момент диполя.
2,2×10 –9 см = 2,2×10 –11 м
m = 1,6 × 10 –19 ×2,2×10 –11 = 3,52×10 –30 Кл×м = 3,52×10 –30 /3,33×10 –30 = 1,06 D.
3. Кратность ковалентной связи определяется числом общих электронных пар, которые связывают атомы. Связь между двумя атомами при помощи одной пары электронов называется простой (связи Н – С1, С – Н, Н – О и т. д.). Связь при помощи двух электронных пар называется двойной (этилен Н 2 С = СН 2), при помощи трех электронных пар – тройной (азот N N, ацетилен Н – С С – Н).
4. Длина связи – это равновесное расстояние между ядрами атомов. Длину связи выражают в нанометрах (нм). 1 нм = 10 –9 м. Чем меньше длина связи, тем прочнее химическая связь.
5. Энергия связи равна работе, которую необходимо затратить на разрыв связи. Выражают энергию связи в килоджоулях на моль (кДж/моль). Энергия связи увеличивается с уменьшением длины связи и с увеличением кратности связи. Процесс образования связи протекает с выделением энергии (экзотермический процесс), а процесс разрыва связи – с поглощением энергии (эндотермический процесс).
Гибридизация
Гибридизация – выравнивание орбиталей по форме и энергии.
Sp-гибридизация
Рассмотрим на примере гидрида бериллия ВеН 2 . Электронное строение атома Ве в нормальном состоянии 1s 2 2s 2 . Атом бериллия может вступать во взаимодействие с атомами водородом только в возбужденном состоянии (s ® р-переход).
Ве – 1s 2 2s 1 2p 1

Две образующиеся связи должны быть различны по энергии, так как возникновение одной связано с перекрыванием двух s-орбиталей, вто-
рой – s- и p-орбиталей. Тогда и атомы водорода в молекуле должны быть химически неравноценны: один более подвижен и реакционноспособен, чем другой. Экспериментально это не так – оба атома водорода энергетически равноценны. Для объяснения этого явления Дж.К. Слейтер и Л. Полинг предположили, что «при интерпретации и расчете углов между связями и длины связи целесообразно близкие по энергии связи заменить равным количеством энергетически равноценных связей». Возникающие подобным образом связи являются гибридными.
Таким образом, одна s- и одна р-орбиталь атома бериллия заменяются двумя энергетически равноценными sp-орбиталями, располагающимися под углом 180 о друг к друг, т.е. молекула имеет линейное строение.

sp 2 -гибридизация
Рассмотрим на примере молекулы гидрида бора ВН 3 . Электронное строение атома бора в нормальном состоянии следующее В – 1s 2 2s 2 2p 1 . Он может образовать только одну ковалентную связь. Три же ковалентные связи для атома бора характерны только в возбужденном состоянии В* – 1s 2 2s 1 2p 2

Одна связь, образованная при перекрывании двух s-орбиталей атомов В и Н, энергетически не отличается от двух других, образуемых перекрыванием s- и р-орбиталей. Три sp 2 -гибридные орбитали расположенные под углом 120 о друг к другу, молекула имеет плоское строение. Подобная картина характерна для любых четырехатомных молекул, образованных за счет трех sp 2 -гибридных связей, например, для хлорида бора (BCl 3).

sp 3 -гибридизация
Рассмотрим на примере метана СН 4 . В нормальном состоянии атом углерода с электронным строением 1s 2 2s 2 2p 2 может дать только две ковалентные связи. В возбужденном состоянии он способен быть четырехвалентным с электронным строением 1s 2 2s 1 2р 3 .

Гибридными становятся одна s- и три р-орбитали атома углерода, при этом образуются четыре sp 3 -гибридные, энергетически равноценные орбитали. Молекула метана приобретает тетраэдрическое строение. В центре тетраэдра, все вершины которого геометрически равноценны, находится атом углерода, а в его вершинах атомы водорода. Угол между связями составляет 109 о 28¢.

Силы взаимодействия между молекулами называют ван-дер-ваальсовыми или межмолекулярными. Это взаимодействие обусловлено электростатическим притяжением между отдельными молекулами и характеризуется следующими особенностями:
Действует на сравнительно больших расстояниях, существенно превосходящих размеры самих молекул;
Характеризуется малой энергией, поэтому существенно ослабевает с повышением температуры;
Является ненасыщающимся, т. е. взаимодействие данной молекулы со второй не исключает подобного эффекта по отношению к третьей, четвертой и т. д.
С ростом относительных молярных масс силы межмолекулярного взаимодействия возрастают и, как следствие, повышаются температуры плавления и кипения веществ.
Задание . Вычислить разность электроотрицательностей атомов ΔЭО для связей O–H и О–Мg в соединении Мg(ОН) 2 и определить какая из этих связей более полярна. ЭО(Н) = 2,1 эВ, ЭО(О) = 3,5 эВ, ЭО(Mg) = 1,2 эВ.
Решение:
ΔЭО(O–H) = 3,5 – 2,1 = 1,4; ΔЭО(O–Mg) = 3,5 – 1,2 = 2,3.
Таким образом, связь Mg–О более полярна.
При образовании соединений из элементов, очень отличающихся по электроотрицательности (типичных металлов и типичных неметаллов), общие электронные пары полностью смещаются к более электроотрицательному атому. Например, при горении натрия в хлоре неспаренный 3s-электрон атома натрия спаривается с 3p-электроном атома хлора. Общая электронная пара полностью смещается к атому хлора (Δχ(Cl) = 2,83 эВ, Δχ(Cl) = 0,93 эВ). Чтобы ионная связь возникла необходимо:
1. Наличие атома с четко выраженной тенденцией к отдаче электрона с образованием положительно заряженного иона (катиона), т.е. с малой ЭИ. Потенциал ионизации – энергия, которую необходимо затратить для удаления 1-го электрона с внешней орбитали. Чем меньше потенциал ионизации, тем легче атом теряет электроны, тем сильнее выражены у элемента металлические свойства. Потенциал ионизации растет в пределах периода слева направо, уменьшается сверху вниз.
Процесс отдачи электронов называется окислением.
2. Наличие атома с четко выраженной тенденцией к присоединению электрона с образованием отрицательно заряженных ионов (анионов), т.е. с большим СЭ. Процесс присоединения электронов называется восстановлением.
Cl + e ® Cl –
Типичные ионные соединения образуются при соединении атомов металлов главных подгрупп I и II групп с атомами неметаллов главной подгруппы VII группы (NaCl, KF, СаС1 2).
Между ионной и ковалентной связью нет резкой границы. В газовой фазе вещества характеризуются чисто ковалентной полярной связью, но эти же вещества в твердом состоянии характеризуются ионной связью.