Намокряне- явление, възникващо поради взаимодействието на течни молекули с молекули твърди вещества. Ако силите на привличане между молекулите на течността и твърдото тяло са по-големи от силите на привличане между молекулите на течността, тогава течността се нарича намокряне; ако силите на привличане между течност и твърдо тяло са по-малки от силите на привличане между молекулите на течността, тогава течността се нарича ненамокрянетова е тялото.
Една и съща течност може да бъде мокреща и немокреща по отношение на различни тела. Така водата намокря стъклото, а не намокря мазната повърхност; живакът не намокря стъклото, а медта.
Намокрянето или ненамокрянето от течност на стените на съда, в който се намира, влияе върху формата на свободната повърхност на течността в съда. Ако в съд се налее голямо количество течност, формата на повърхността му се определя от гравитацията, което осигурява равна и хоризонтална повърхност. Но при самите стени повърхността на течността все още е извита.
Нека разгледаме течна молекула близо до стената на съд (фиг. 1). Нека \(~\vec F_1\) е резултантната на силите, действащи върху тази молекула от страната на твърдо тяло, \(~\vec F_2\) - от страната на течните молекули. Силата \(~\vec F_1\) е перпендикулярна на стената, \(~\vec F_2\) е насочена под ъгъл от 45° спрямо стената. За омокряща течност (фиг. 1, а) силови модули Е 1 > Е 2. Резултатът от тези сили \(~\vec F\) е силата молекулярно налягане, нанесени върху молекулите, и трябва да бъдат насочени дълбоко в течността перпендикулярно на нейната повърхност. Следователно повърхността в близост до стените не е хоризонтална, а извита. Кривината на стените на свободната повърхност се доказва по подобен начин за немокряща се течност (фиг. 1, b).

Мярка за намокряне е контактният ъгъл θ - това е ъгълът между равнината, допирателна към повърхността на течността и стената (равнината на повърхността на твърдото тяло). В контактния ъгъл винаги има течност (фиг. 2, а, б). За омокряща течност θ е остър, за ненамокряща течност θ е тъп. При пълно намокряне θ = 0, при пълно ненамокряне θ = 180°. Ако омокрящата течност е върху откритата повърхност на твърдо тяло (фиг. 3, а), тогава тя се разпространява върху тази повърхност. Ако върху откритата повърхност на твърдо тяло има немокряща течност, тогава тя придобива форма, близка до сферичната (фиг. 3, b).

Намокрянето е важно както в ежедневието, така и в индустрията. Доброто омокряне е необходимо при боядисване, измиване, обработка на фотографски материали, нанасяне на боя и лакови покрития, лепилни материали, запояване и при флотационни процеси (обогатяване на руди с ценна скала).
Обратно, при изграждането на хидроизолационни съоръжения са необходими материали, които не се намокрят от вода.
Литература
Аксенович Л. А. Физика в гимназия: Теория. Задачи. Тестове: Учебник. ползи за институции, осигуряващи общо образование. среда, образование / Л. А. Аксенович, Н. Н. Ракина, К. С. Фарино; Ед. К. С. Фарино. - Мн.: Адукация и изпитание, 2004. - С. 181-182.
На границата между течност и твърдо тяло възникват явления на намокряне или ненамокряне поради взаимодействието на течни молекули с твърди молекули:

Фиг. 1 Явление на намокряне (а) и ненамокряне (б) на повърхността на твърдо тяло от течност (контактен ъгъл)
Тъй като явленията на омокряне и ненамокряне се определят от относителните свойства на веществата на течност и твърдо тяло, една и съща течност може да бъде омокряща за едно твърдо тяло и ненамокряща за друго. Например водата намокря стъклото, но не намокря парафина.
Количествена мярка за намокряне е контактен ъгълъгълът, образуван от повърхността на твърдо тяло и допирателна, начертана към повърхността на течност в точката на контакт (течността е вътре в ъгъла).
При намокряне, колкото по-малък е ъгълът, толкова по-силно е намокрянето. Ако контактният ъгъл е нула, се нарича намокряне пълен или съвършен. Случаят на идеално намокряне може приблизително да се опише като разпръскване на алкохол върху чиста стъклена повърхност. В този случай течността се разпространява по повърхността на твърдото вещество, докато покрие цялата повърхност.
В случай на ненамокряне, колкото по-голям е ъгълът, толкова по-силно е ненамокрянето. При стойността на контактния ъгъл се наблюдава пълно ненамокряне. В този случай течността не се придържа към повърхността на твърдото вещество и лесно се търкаля от него. Подобно явление може да се наблюдава, когато се опитаме да измием мазна повърхност със студена вода. Почистващите свойства на сапуна и синтетичните прахове се обясняват с факта, че сапуненият разтвор има по-ниско повърхностно напрежение от водата. Високото повърхностно напрежение на водата не позволява тя да проникне в малки пори и пространства между тъканите.
Явленията на намокряне и ненамокряне играят важна роля в човешкия живот. По време на производствени процеси като лепене, боядисване и запояване е много важно да се осигури намокряне на повърхността. Осигуряването на ненавлажняване е много важно при създаването на хидроизолация и синтезирането на водоустойчиви материали. В медицината явленията на омокряне са важни за осигуряване на движението на кръвта през капилярите, дишането и други биологични процеси.
Явленията на намокряне и ненамокряне се проявяват ясно в тесни тръби - капиляри.
Капилярни явления
ОПРЕДЕЛЕНИЕ
Капилярни явления- е покачването или спадането на течността в капилярите в сравнение с нивото на течността в широките тръби.
Омокрящата течност се издига през капиляра. Течността, която не намокря стените на съда, потъва в капиляра.
Височина h на повдигане на течност през капилярасе определя от отношението:
къде е коефициентът повърхностно напрежениетечности; плътност на течността; капилярен радиус, ускорение свободно падане.
Дълбочината, до която течността се спуска в капиляра, се изчислява по същата формула.
ОПРЕДЕЛЕНИЕ
Извитата повърхност на течността се нарича менискус.
Под вдлъбнат менискус на омокряща течност налягането е по-малко, отколкото под плоска повърхност. Следователно течността в капиляра се издига дотогава. докато хидростатичното налягане на течността, повдигнато в капиляра на нивото на плоската повърхност, компенсира разликата в налягането. Под изпъкналия менискус на неомокрящата течност налягането е по-голямо, отколкото под плоската повърхност, което води до потъване на течността в капиляра.
Капилярни явления можем да наблюдаваме както в природата, така и в ежедневието. Например, почвата има рохкава структура и между отделните й частици има празнини, които са капиляри. При поливане през капиляри водата се издига до кореновата система на растенията, доставяйки им влага. Също така вода в почвата, издигайки се през капилярите. се изпарява. За да се намали ефективността на изпарението, като по този начин се намали загубата на влага, почвата се разхлабва, унищожавайки капилярите. В ежедневието капилярните явления се използват при попиване на влажна повърхност с хартиена кърпа или салфетка.
Примери за решаване на проблеми
ПРИМЕР 1
| Упражнение | В капилярна тръба с радиус 0,5 mm течността се издига с 11 mm. Намерете плътността на тази течност, ако нейният коефициент на повърхностно напрежение е . |
| Решение | откъде идва плътността на течността: Нека преобразуваме единиците в системата SI: радиус на тръбата; височина на повдигане на течността; коефициент на повърхностно напрежение на течността. Ускорение на гравитацията Нека изчислим: |
| отговор | Плътност на течността |
ПРИМЕР 2
| Упражнение | Намерете масата на водата, издигаща се през капилярна тръба с диаметър 0,5 mm. |
| Решение | Височината на течността, издигаща се през капиляра, се определя по формулата: Плътност на течността: Обемът на течния стълб, издигащ се през капиляра, се изчислява като обем на цилиндър с височина и основна площ: Замествайки съотношението за обема на течен стълб във формулата за плътност на течността, получаваме: Като се вземе предвид последната връзка, както и фактът, че радиусът на капиляра, височината на течността, издигаща се по капиляра:
От последната връзка намираме масата на течността: Нека преобразуваме единиците в системата SI: диаметър на тръбата. Ускорение на гравитацията Коефициент на повърхностно напрежение на водата. Нека изчислим: |
| отговор | Маса на водата, издигаща се през капилярната тръба kg. |
Намокрянето е повърхностно явление, състоящо се от взаимодействието на течност с повърхността на твърдо или друго тяло.
Има два вида намокряне:
Потапяне (цялата повърхност на твърдото тяло е в контакт с течността)
Контакт (състои се от 3 фази - твърда, течна, газообразна)
Степента на намокряне се характеризира с контактния ъгъл. Контактният ъгъл (или контактният ъгъл) е ъгълът, образуван от допирателните равнини към междинните повърхности, ограничаващи омокрящата течност, а върхът на ъгъла лежи на линията на разделяне на трите фази. Измерено по метода на сесилната капка. В случая с праховете все още не са разработени надеждни методи, осигуряващи висока степен на възпроизводимост (2008 г.). Предложен е гравиметричен метод за определяне на степента на овлажняване, но той все още не е стандартизиран.
Измерването на степента на овлажняване е много важно в много отрасли
(бои и лакове, фармацевтични, козметични и др.). Например, върху предните стъкла на автомобили се нанасят специални покрития, които трябва да бъдат устойчиви на различни видове замърсяване. Съставът и физичните свойства на покритията за стъкло и контактни лещи могат да бъдат оптимизирани въз основа на резултатите от измерването на контактния ъгъл.
Когато течност влезе в контакт с повърхността на твърдо тяло, са възможни два случая: течността намокря твърдото тяло и не го намокря. Ако например капки живак се поставят върху повърхността на чисто желязо и върху чисто стъкло, то върху повърхността на желязото те ще се разпространят, а върху повърхността на стъклото ще имат форма, близка до сферичната.
Ако силите на взаимодействие между молекулите на твърдото тяло и молекулите на течността са по-големи от силите на взаимодействие между молекулите на течността, тогава течността намокря твърдото вещество (живак-желязо). В друг случай течността не намокря твърдото вещество (живак-желязо).
Извитата повърхност на течност в тесни цилиндрични тръби или близо до стените на съд се нарича менискусПовърхността на намокряща се течност в близост до твърдо тяло се издига и менискусът е вдлъбнат (фиг. 49.1, а) повърхността му в близост до твърдо тяло леко се спуска и менискусът е изпъкнал (фиг. 49.1). , б).
Фигура 49.1
За да определите дали течността се намокря или не се намокря по отношение на твърдо тяло, можете да използвате контактния ъгъл (ъгълът между повърхността на твърдото тяло и допирателната към повърхността на течността в точка M).
За течност, намокряща повърхността на твърдо тяло, контактният ъгъл е остър (< π/2); чем лучше смачивание, тем меньше. Для полного смачивания= 0. Для несмачивающих жидкостей краевой угол изменяется в пределах π/2 << π; при полном не смачивании= π.
Омокрящата течност има вдлъбнат менискус, докато ненамокрящата течност има изпъкнал менискус.
Намокрянето зависи от връзката между силите на адхезия на молекулите на течността с молекулите (или атомите) на намокреното тяло (адхезия) и силите на взаимно сцепление на молекулите на течността (кохезия).
Степента на намокряне се характеризира с контактния ъгъл. Контактният ъгъл (или контактният ъгъл) е ъгълът, образуван от допирателните равнини към междинните повърхности, ограничаващи омокрящата течност, а върхът на ъгъла лежи на линията на разделяне на трите фази. Измерено по метода на сесилната капка. В случая с праховете все още не са разработени надеждни методи, даващи висока степен на възпроизводимост. Предложен е гравиметричен метод за определяне на степента на овлажняване, но той все още не е стандартизиран.
Измерването на степента на овлажняване е много важно в много индустрии (бои, фармацевтика, козметика и др.). Например, върху предните стъкла на автомобили се нанасят специални покрития, които трябва да бъдат устойчиви на различни видове замърсяване. Съставът и физичните свойства на покритията за стъкло и контактни лещи могат да бъдат оптимизирани въз основа на резултатите от измерването на контактния ъгъл.
Например, популярен метод за увеличаване на производството на нефт чрез инжектиране на вода в резервоар се основава на факта, че водата запълва порите и изстисква нефта. В случай на малки пори и чиста вода това далеч не е така, така че трябва да се добавят специални повърхностно активни вещества. Оценката на омокряемостта на скалите при добавяне на разтвори с различен състав може да бъде измерена с различни инструменти.
Омокряемост с вода.
Това свойство се проявява много ясно в способността на водата да се „залепва“ за много предмети, тоест да ги намокря. При изучаването на това явление беше установено, че всички вещества, които лесно се намокрят от вода (глина, пясък, стъкло, хартия и др.), Със сигурност съдържат кислородни атоми. За да се обясни природата на намокрянето, този факт се оказа ключов: енергийно небалансираните молекули на повърхностния слой вода са в състояние да образуват допълнителни водородни връзки с „чужди“ кислородни атоми. Поради повърхностното напрежение и омокрящата способност водата може да се издигне в тесни вертикални канали до височина, по-голяма от тази, разрешена от гравитацията, тоест водата има свойството капилярност.
- Когато разглеждаме молекулярната картина на повърхностния слой на течност, отбелязахме, че молекулите на течността, разположени на повърхността, разделяща течността и газа (въздух или пара от тази течност), почти не се привличат от молекулите на газа (концентрацията на молекулите на газа е твърде ниска ). Ако течността граничи с твърдо вещество, резултатът е различен.
Феномени на границата течност-твърдо вещество
На границата течност-твърдо вещество вече не могат да се игнорират силите на привличане между молекулите на течността и молекулите на твърдото вещество. Освен това в някои случаи силата на привличане между молекулите на течността и твърдото тяло се оказва по-голяма от силата на привличане между молекулите на самата течност. В този случай се казва, че течността намокря твърдото вещество. Ако силите на привличане между молекулите на течността са по-големи от силите на привличане между молекулите на твърдо тяло и молекулите на течност, тогава такава течност се нарича ненамокряща.
Така стъклото се намокря от вода, но не и от живак. Това означава, че силата на привличане между водните молекули и стъклените молекули е по-голяма от силата на привличане на водните молекули. В случая на живак и стъкло, силите на привличане между молекулите на живак и стъкло са малки в сравнение със силите на привличане между молекулите на живак.
Това се потвърждава от следния опит. Окачваме чиста стъклена чиния на везна със скъсено окачване и поставяме под нея съд с вода отдолу. При контакт с вода плочата се намокря и задържа от нея. За да откъснете плочата от водата, трябва да поставите малка тежест върху другия съд на везната (фиг. 7.14, а).
ориз. 7.14
Долната част на отделената плоча се оказва покрита с вода (фиг. 7.14, б). Това доказва, че разкъсването не е станало между повърхностите на плочата и водата, а между слоевете вода. Следователно силата на привличане между стъклените молекули и водните молекули е по-голяма от силата на привличане между водните молекули.
Ако поставим същата стъклена плоча в контакт не с вода, а с живак, тогава долната част на плочата ще остане чиста (фиг. 7.14, c). Това означава, че взаимодействието между живачните молекули е по-силно от взаимодействието между стъклото и живачните молекули. Тук можем да дадем аналогия с опъната верига, която се къса там, където има най-слабото звено.
Много е лесно да се разграничи омокряща течност от ненамокряща течност. За да направите това, достатъчно е да нанесете капка течност върху повърхността на твърдо вещество. Ако течност намокри тяло, тогава капката се разпространява по повърхността; ненамокрящата течност не се разпространява (фиг. 7.15).
![]()
ориз. 7.15
Менискус
Формата на повърхността на течността в точката, където тя влиза в контакт с твърдата стена и газа, зависи от това дали течността намокря или не намокря стените на контейнера. Ако течността се овлажнява, тогава ъгълът Θ между допирателната към повърхността на течността и твърдото тяло на общата граница на трите среди, измерен вътре в течността (контактен ъгъл), е остър (фиг. 7.16, а). В случай, че течността не намокря твърдото вещество, контактният ъгъл Θ е тъп (фиг. 7.16, b). При пълно намокряне Θ = 0°, а при пълно ненамокряне - Θ = 180°.

ориз. 7.16
Хоризонтална е само частта от повърхността на течността, отстранена от стените на съда. Сближавайки противоположните стени (вземайки по-тесен съд), ще намалим хоризонталната част на свободната повърхност на течността (фиг. 7.17, a, b), докато накрая тя изчезне напълно (фиг. 7.17, c). Повърхността на течността става извита. Извитата повърхност на течността се нарича менискус (от гръцката дума menisos - полумесец).

ориз. 7.17
В тесни тръби омокрящите течности имат вдлъбнат менискус (вижте фиг. 7.17, c), ненамокрящите течности имат изпъкнал менискус (фиг. 7.18).
ориз. 7.18
В тесни тръби с пълно намокряне (или ненамокряне) течният менискус е полусфера, чийто радиус е равен на радиуса r на канала на тръбата. Ако намокрянето (или ненамокрянето) е непълно, тогава менискусът на течността в тесни тръби също се приема като част от сфера, чийто радиус R е свързан с радиуса на тръбата чрез отношението r = R cos Θ (фиг. 7.19).

ориз. 7.19
Стойност на омокряне
Намокрянето е важно в промишлеността и ежедневието. Доброто намокряне е необходимо при боядисване и пране, обработка на фотоматериали, нанасяне на бояджийски и лакови покрития и др.
Почистващите свойства на сапуна и синтетичните прахове се обясняват с факта, че сапуненият разтвор има по-ниско повърхностно напрежение от водата. Високото повърхностно напрежение на водата не позволява тя да проникне в пространствата между влакната на тъканта и в малките пори.
Важно е още едно обстоятелство. Молекулите на сапуна имат продълговата форма. Единият от краищата има „афинитет“ към водата и е потопен във вода. Другият край се отблъсква от водата и се прикрепя към мастните молекули. Водните молекули обгръщат мастните частици и помагат за измиването им.
Лепенето на дърво, кожа, каучук и други материали също е пример за използване на омокрящи свойства. Запояването също се свързва с омокрящи и ненамокрящи свойства. За да може разтопената спойка (например сплав от калай и олово) да се разпространи добре по повърхностите на запояваните метални предмети и да полепне по тях, тези повърхности трябва да бъдат старателно почистени от мазнини, прах и оксиди. Калайената спойка може да се използва за запояване на части от мед и месинг. Но алуминият не се намокря от калаена спойка. За запояване на алуминиеви продукти се използва специална спойка, състояща се от алуминий и силиций.
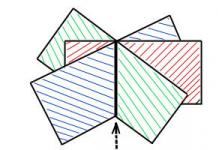
Важен пример за приложението на явлението намокряне и ненамокряне е флотационният процес на обогатяване на рудата. За тази цел рудата се раздробява, така че парчетата ценна скала да загубят контакт с ненужните примеси. След това полученият прах се разклаща във вода, към която се добавят маслени вещества. Маслото обгръща (намокря) ценната скала, но не полепва върху примесите (не ги намокря). В получената суспензия се вдухва въздух. Въздушните мехурчета се придържат към парчета ценна скала, които не са намокрени от вода (поради покритие с маслен филм). Това се случва, защото тънък слой вода между въздушните мехурчета и масления филм, обгръщащ ценната скала, стремейки се да намали повърхността й, разкрива повърхността на масления филм (точно както водата върху мазна повърхност се събира на капки, разкривайки тази повърхност) . Зърната от ценна скала, заедно с въздушните мехурчета, полепнали по тях, се издигат нагоре под въздействието на Архимедова сила, докато ненужните примеси се утаяват на дъното (фиг. 7.20).

ориз. 7.20
Водата намокря повърхностите на някои твърди тела (полепва по тях) и не намокря повърхностите на други. Тези свойства на водата определят много полезни и просто любопитни явления.
От практиката е известно, че капка вода се разпространява върху стъкло и приема формата, показана на фиг. 98, докато живакът на същата повърхност се превръща в малко сплескана капка (фиг. 99). В първия случай казват, че течността мокритвърда повърхност, във втория - не мокринея. Намокрянето зависи от естеството на силите, действащи между молекулите на повърхностните слоеве на контактната среда. За овлажняваща течност силата на привличане между молекулите на течността и твърдото тяло е по-голяма, отколкото между молекулите на самата течност и течността се стреми да увеличи повърхността на контакт с твърдото вещество. За немокряща течност силата на привличане между молекулите на течността и твърдото тяло е по-малка, отколкото между молекулите на течността и течността се стреми да намали повърхността на своя контакт с твърдото тяло.
ориз. 98 Фиг. 99
Към линията на контакт на три среди (точка ЗАе нейното пресичане с равнината на чертежа), се прилагат три сили на повърхностно напрежение, които са насочени тангенциално в повърхността на контакт на съответните две среди (фиг. 98 и 99). Тези сили, приписвани на единица за дължинаконтактните линии са равни на съответните повърхностни напрежения s 12 , s 13 , s 23 . Ъгълът q между допирателните към повърхността на течността и твърдото тяло се нарича контактен ъгъл. Условието за равновесие на капка (фиг. 98) е сумата от проекциите на силите на повърхностно напрежение върху посоката на допирателната към повърхността на твърдото тяло да е равна на нула, т.е.
От условието (67.1) следва, че контактният ъгъл може да бъде остър или тъп в зависимост от стойностите на × s 13 и s 12. Ако s 13 > s 12 , тогава cos q > 0 и ъгълът q е остър (фиг. 98), т.е. течността намокря твърдата повърхност. Ако е 13 < s 12 , тогава cos q< 0 и угол q- тупой (рис. 99), т. е. жидкость не смачивает твердую поверхность. Краевой угол удовлетворяет условию (67.1), если
Ако условието (67.2) не е изпълнено, тогава течна капка 2 не може да бъде в равновесие при никаква стойност на q. Ако s 13 > s 12 + s 23, тогава течността се разпространява по повърхността на твърдото вещество, покривайки го с тънък филм (например керосин върху повърхността на стъклото) - настъпва пълно намокряне (в този случай q = 0 ). Ако s 12 > s 13 + s 23, тогава течността се свива в сферична капка, в границата има само една точка на контакт с нея (например капка вода върху повърхността на парафин) - настъпва пълна консистенция ( в този случай q = p).
Намокряне и ненамокряне са относителни понятия, т.е. течност, която намокря една твърда повърхност, не намокря друга. Например водата намокря стъклото, но не мокри парафина; Живакът не мокри стъкло, но мокри метални повърхности.
Явленията намокряне и немокрене имат голяма стойноств технологиите. Например, при метода за обогатяване на руда с флотация (отделяне на рудата от отпадъчната скала), тя, фино натрошена, се разклаща в течност, която намокря отпадъчната скала и не намокря рудата. През тази смес се продухва въздух и след това се утаява. В този случай скалните частици, навлажнени с течност, потъват на дъното, а зърната от минерали се „залепват“ за въздушни мехурчета и изплуват на повърхността на течността. При обработката на металите те се навлажняват със специални течности, което улеснява и ускорява обработката.