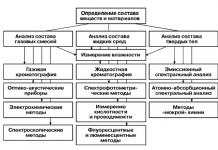
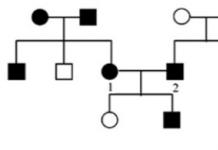
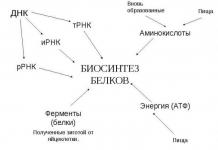
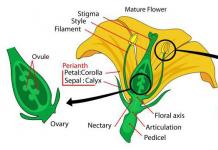
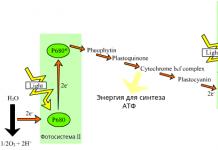
2.2. Историята на създаването на периодичната система.
През зимата на 1867-68 г. Менделеев започва да пише учебника "Основи на химията" и веднага се сблъсква с трудности при систематизирането на фактическия материал. До средата на февруари 1869 г., докато обмисля структурата на учебника, той постепенно стига до извода, че свойствата прости вещества(и това е форма на съществуване химични елементив свободно състояние) и атомните маси на елементите са свързани по определена закономерност.
Менделеев не знаеше много за опитите на неговите предшественици да подредят химичните елементи по нарастващи атомни маси и за инцидентите, възникнали в този случай. Например, той няма почти никаква информация за работата на Шанкуртоа, Нюландс и Майер.
Решаващият етап от неговите мисли идва на 1 март 1869 г. (14 февруари, стар стил). Ден по-рано Менделеев написа молба за десетдневна ваканция, за да инспектира артелите за сирене в провинция Твер: той получи писмо с препоръки за изучаване на производството на сирене от А. И. Ходнев, един от лидерите на Свободното икономическо дружество.
Петербург този ден беше облачен и мразовит. Дърветата скърцаха от вятъра в университетската градина, където гледаха прозорците на апартамента на Менделеев. Още в леглото Дмитрий Иванович изпи чаша топло мляко, след това стана, изми се и отиде на закуска. Настроението му беше прекрасно.
На закуска Менделеев имаше неочаквана идея: да сравни близки атомни маси на различни химични елементи и техните химични свойства. Без да се замисля, на обратната страна на писмото на Ходнев той записва символите за хлор Cl и калий К с доста сходни атомни маси, равни съответно на 35,5 и 39 (разликата е само 3,5 единици). В същото писмо Менделеев скицира символи на други елементи, търсейки подобни „парадоксални“ двойки сред тях: флуор F и натрий Na, бром Br и рубидий Rb, йод I и цезий Cs, за които разликата в масата се увеличава от 4,0 до 5,0 и след това до 6.0. По това време Менделеев не можеше да знае, че "неопределената зона" между явните неметали и метали съдържа елементи - благородни газове, чието откриване по-късно значително ще промени периодичната таблица.
След закуска Менделеев се затвори в кабинета си. Той извади пакет от визиткии започнаха да изписват на обратната им страна символите на елементите и техните основни химични свойства. След малко домакинството чу как от кантората започна да се чува: "Ууу! Рогата. Леле, каква рогата! Ще ги преодолея. Ще ги убия!" Тези възклицания означаваха, че Дмитрий Иванович има творческо вдъхновение. Менделеев премести картите от един хоризонтален ред в друг, ръководейки се от стойностите на атомната маса и свойствата на простите вещества, образувани от атоми на същия елемент. За пореден път на помощ му се притекоха задълбочени познания не органична химия. Постепенно започва да се оформя появата на бъдещата периодична таблица на химичните елементи. И така, отначало той постави карта с елемента берилий Be (атомна маса 14) до картата на алуминиевия елемент Al (атомна маса 27,4), според тогавашната традиция, приемайки берилий за аналог на алуминия. След това обаче, сравнявайки химичните свойства, той постави берилий върху магнезий Mg. След като се съмнява в общоприетата тогава стойност на атомната маса на берилия, той я променя на 9,4 и променя формулата на берилиевия оксид от Be 2 O 3 на BeO (като магнезиев оксид MgO). Между другото, "коригираната" стойност на атомната маса на берилия беше потвърдена едва десет години по-късно. Той действаше също толкова смело и в други случаи.
Постепенно Дмитрий Иванович стига до окончателното заключение, че елементите, подредени във възходящ ред на техните атомни маси, показват ясна периодичност във физичните и химичните свойства. През целия ден Менделеев работеше върху системата от елементи, правейки кратки почивки, за да играе с дъщеря си Олга, да обядва и вечеря.
Вечерта на 1 март 1869 г. той избелва съставената от него таблица и под заглавие „Експеримент на система от елементи, базирана на тяхното атомно тегло и химическо сходство“, я изпраща на печата, като прави бележки за наборчици и поставя датата "17 февруари 1869 г." (това е по стар стил).
Така е открит Периодичният закон, чиято съвременна формулировка е следната: Свойствата на простите вещества, както и формите и свойствата на съединенията на елементите, са в периодична зависимост от заряда на ядрата на техните атоми. .
Менделеев изпраща печатни листове с таблица на елементите на много местни и чуждестранни химици и едва след това напуска Санкт Петербург, за да инспектира фабриките за сирене.
Преди заминаването си той все пак успя да предаде на Н. А. Меншуткин, органичен химик и бъдещ историк на химията, ръкописа на статията "Връзката на свойствата с атомното тегло на елементите" - за публикуване в Руски вестник химическо обществои за докладване на предстояща среща на дружеството.
На 18 март 1869 г. Меншуткин, който по това време е чиновник на обществото, прави малък доклад за Периодичния закон от името на Менделеев. Отначало докладът не привлече особено внимание на химиците, а президентът на Руското химическо дружество академик Николай Зинин (1812-1880) заяви, че Менделеев не прави това, което трябва да прави истинският изследовател. Вярно е, че две години по-късно, след като прочете статията на Дмитрий Иванович „Естествената система от елементи и нейното приложение за посочване на свойствата на определени елементи“, Зинин промени решението си и пише на Менделеев: „Много, много добри, много отлични приближения, дори забавни да четеш, Бог да те благослови с късмет експериментално потвърждениевашите заключения. Н. Зинин, искрено ви предан и дълбоко ви уважавам." Менделеев не поставя всички елементи във възходящ ред на атомните маси; в някои случаи той се ръководеше повече от сходството на химичните свойства. И така, кобалт Co има атомна маса по-голяма от никел Ni, телурът Te също е по-голям от този на йод I, но Менделеев ги поставя в реда Co - Ni, Te - I, а не обратното. В противен случай телурът ще попадне в халогенната група, а йодът ще стане роднина на селена Se.
На жена му и децата му. А може би е знаел, че умира, но не е искал да смущава и вълнува предварително семейството, което обичаше страстно и нежно. В 5:20 ч. 20 януари 1907 г. умира Дмитрий Иванович Менделеев. Погребан е на гробището Волковски в Санкт Петербург, недалеч от гробовете на майка му и сина му Владимир. През 1911 г. Музеят на Д.И. Менделеев, където...
Московска метростанция, изследователски кораб за океанографски изследвания, 101-ви химичен елемент и минерал - менделеевит. Рускоезичните учени-шегаджии понякога питат: „Дмитрий Иванович Менделеев не е ли евреин, болезнено странно фамилно име, не идва ли от фамилията „Мендел“?“ Отговорът на този въпрос е изключително прост: „И четиримата сина на Павел Максимович Соколов, ...
Лицейски изпит, където старият Державин благослови младия Пушкин. Ролята на измервателния уред беше изиграна от академик Ю. Ф. Фрицше, известен специалист по органична химия. Докторска дисертация Д. И. Менделеев завършва Главния педагогически институт през 1855 г. Докторска дисертация "Изоморфизъм във връзка с други отношения на кристална форма към състав" става първата му голяма научна ...
Основно по въпроса за капилярността и повърхностно напрежениетечности и прекарва свободното си време в кръга на младите руски учени: S.P. Боткин, И.М. Сеченов, И.А. Вишнеградски, A.P. Бородина и др. През 1861 г. Менделеев се завръща в Санкт Петербург, където възобновява изнасянето на лекции по органична химия в университета и издава забележителен за онова време учебник: "Органична химия" в...
Всичко материално, което ни заобикаля в природата, независимо дали става дума за космически обекти, обикновени земни обекти или живи организми, се състои от вещества. Има много разновидности от тях. Още в древни времена хората са забелязали, че са в състояние не само да променят физическото си състояние, но и да се превърнат в други вещества, надарени с други свойства в сравнение с оригиналните. Но ето законите, според които се случват такива трансформации на материята, човек не е разбрал веднага. За да се направи това, беше необходимо правилно да се идентифицира основата на материята и да се класифицират елементите, съществуващи в природата. Това става възможно едва в средата на 19 век с откритието периодичен закон. Историята на неговото създаване D.I. Менделеев е предшестван от много години работа, а вековният опит на цялото човечество допринесе за формирането на този вид знание.
Кога бяха положени основите на химията?
Занаятчиите от древни времена са били доста успешни в леенето и топенето на различни метали, знаейки много тайни за тяхната трансмутация. Те предават своите знания и опит на своите потомци, които ги използват до Средновековието. Смяташе се, че е напълно възможно да се превърнат неблагородните метали в ценни, което всъщност е основната задача на химиците до 16 век. Всъщност в такава идея са заложени философските и мистични идеи на древногръцките учени, че цялата материя е изградена от определени „първични елементи“, които могат да се прераждат един в друг. Въпреки очевидната примитивност на този подход, той изигра роля в историята на откриването на Периодичния закон.

Панацея и бяла тинктура
Търсейки основния принцип, алхимиците твърдо вярваха в съществуването на две фантастични вещества. Един от тях бил философският камък, известен в легендите, наричан още еликсир на живота или панацея. Смятало се, че такова лекарство е не само безпроблемен начин за превръщане на живак, олово, сребро и други вещества в злато, но и служи като чудодейно универсално лекарство, което лекува всякакви човешки заболявания. Друг елемент, наречен бяла тинктура, не беше толкова ефективен, но беше надарен със способността да превръща други вещества в сребро.
Разказвайки предисторията на откриването на периодичния закон, е невъзможно да не споменем знанията, натрупани от алхимиците. Те олицетворяват модел на символично мислене. Представители на тази полумистична наука създадоха известно химически моделсвета и протичащите в него процеси на космическо ниво. В стремежа си да разберат същността на всички неща, те записаха най-подробно лабораторни техники, оборудване и информация за химически стъклени съдове, с голяма скрупулезност и старание в предаването на опита си на колеги и потомци.

Необходимост от класификация
Значително количество информация за различни химични елементи за XIX вексе натрупаха достатъчно, което породи естествена потребност и желание на учените да ги систематизират. Но за извършване на такава класификация бяха необходими допълнителни експериментални данни, както и не мистични, а реални знания за структурата на веществата и същността на основата на структурата на материята, която все още не е съществувала. Освен това наличната информация за значението на атомните маси на известните по това време химически елементи, въз основа на които е извършена систематизацията, не е особено точна.
Но опитите за класификация сред естествените учени са правени многократно много преди осъзнаването на истинската същност на нещата, която сега формира основата съвременната наука. Много учени са работили в тази посока. Говорейки накратко за предпоставките за откриването на периодичния закон на Менделеев, трябва да споменем примери за такива комбинации от елементи.
Триади
Учените от онези времена смятат, че свойствата, проявени от най-разнообразните вещества, безспорно зависят от величините на техните атомни маси. Осъзнавайки това, немският химик Йохан Дьоберейнер предложи своя собствена система за класификация на елементите, които съставляват основата на материята. Това се случи през 1829 г. И това събитие беше доста сериозен напредък в науката за този период от нейното развитие, както и важен етап в историята на откриването на периодичния закон. Дьоберейнер обединява известни елементи в общности, като им дава името „триади“. Според съществуващата система масата на екстремните елементи се оказва равна на средната стойност на сумата от атомните маси на члена на групата, който е между тях.

Опитите за разширяване на границите на триадите
В споменатата система Döbereiner имаше достатъчно недостатъци. Например във веригата от барий, стронций, калций нямаше подобен на тях магнезий по структура и свойства. А в общността на телур, селен, сяра нямаше достатъчно кислород. Много други подобни вещества също не успяха да бъдат класифицирани според триадната система.
Тези идеи са развити от много други химици. По-специално, немският учен Леополд Гмелин се стреми да разшири „близките“ граници, като разшири групите от класифицирани елементи, като ги разпредели в реда на еквивалентни тегла и електроотрицателност на елементите. Неговите структури формират не само триади, но и тетради, пентади, но немският химик не успява да схване същността на периодичния закон.
Спирала дьо Шанкуртоа
Дори повече сложна схемаконструкцията на елементите е изобретена от Александър дьо Шанкуртоа. Той ги постави върху равнина, сгъната в цилиндър, като ги разпредели по вертикалите с наклон от 45 ° в реда на увеличаване на атомните маси. Както се очаква, по линии, успоредни на оста на даден обем геометрична фигура, е трябвало да бъдат локализирани вещества с подобни свойства.

Но всъщност идеалната класификация не се получи, тъй като елементи, които изобщо не са свързани, понякога попадат в една и съща вертикала. Например, до алкалните метали се оказа, че манганът има съвсем различно химическо поведение. И една "компания" получи сяра, кислород и елемента титан, който е напълно различен от тях. Подобна схема обаче също допринесе, заемайки своето място в историята на откриването на периодичния закон.
Други опити за създаване на класификации
След описаните, Джон Нюландс предложи своя собствена система за класификация, като отбеляза, че всеки осми член от получената серия показва прилики в свойствата на елементите, подредени в съответствие с увеличаването на атомната маса. На учения му хрумна да сравни намерения модел със структурата на подредбата на музикалните октави. В същото време той присвои пореден номер на всеки от елементите, като ги постави в хоризонтални редове. Но подобна схема отново не се оказа идеална и беше оценена много скептично в научните среди.

От 1964 до 1970 г таблици, подреждащи химичните елементи, също са създадени от Odling и Meyer. Но подобни опити отново имаха своите недостатъци. Всичко това се случи още в навечерието на откриването от Менделеев на периодичния закон. А някои произведения с несъвършени опити за класификация бяха публикувани дори след като таблицата, която използваме и до днес, беше представена на света.
Биография на Менделеев
Блестящ руски учен е роден в град Тоболск през 1834 г. в семейството на директора на гимназията. В къщата освен него имаше още шестнадесет братя и сестри. Не е лишен от внимание, тъй като най-малкият от децата, Дмитрий Иванович, от съвсем малък удиви всички с необикновените си способности. Родителите, въпреки трудностите, се стремяха да му дадат най-много по-добро образование. И така, Менделеев първо завършва гимназията в Тоболск, а след това и Педагогическия институт в столицата, като същевременно поддържа дълбок интерес към науките в душата си. И не само на химията, но и на физиката, метеорологията, геологията, технологиите, приборостроенето, аеронавтиката и други.
Скоро Менделеев защитава дисертация и става асистент в Санкт Петербургския университет, където изнася лекции по органична химия. През 1865 г. той представя докторската си дисертация пред колегите си на тема „За комбинацията на алкохол с вода“. Годината на откриването на периодичния закон е 1969 г. Но това постижение е предшествано от 14 години упорита работа.

За великото откритие
Като се вземат предвид грешките, неточностите, както и положителния опит на колегите, Дмитрий Иванович успя да систематизира химическите елементи по най-удобния начин. Той също така забеляза периодичната зависимост на свойствата на съединенията и простите вещества, тяхната форма от стойността на атомните маси, което се казва в формулировката на периодичния закон, даден от Менделеев.
Но такива прогресивни идеи, за съжаление, не намериха веднага отговор в сърцата дори на руски учени, които приеха това нововъведение много предпазливо. А сред дейците на чуждата наука, особено в Англия и Германия, законът на Менделеев изобщо намери най-върлите противници. Но много скоро ситуацията се промени. Каква беше причината? Блестящата смелост на великия руски учен след известно време се появи на света в доказателство за неговата брилянтна способност за научна далновидност.

Нови елементи в химията
Откриването на периодичния закон и създадената от него структура на периодичната таблица позволи не само да се систематизират веществата, но и да се направят редица прогнози за наличието в природата на много елементи, неизвестни по това време. Ето защо Менделеев успява да приложи на практика това, което други учени не са могли да направят преди него.
Изминаха само пет години и предположенията започнаха да се потвърждават. Французинът Лекок дьо Боабодран открива нов метал, който нарече галий. Свойствата му се оказаха много подобни на екаалуминия, предвиден от Менделеев на теория. След като научиха за това, представителите на научния свят от онези времена бяха зашеметени. Но на това невероятни фактиизобщо не е завършен. Освен това шведът Нилсон открива скандий, чийто хипотетичен аналог е екабор. А германият, открит от Винклер, стана близнак на екасилиция. Оттогава законът на Менделеев започва да се утвърждава и да придобива все повече и повече нови поддръжници.
Нови факти на брилянтна прозорливост
Създателят бил толкова увлечен от красотата на своята идея, че се заел да направи някои предположения, чиято валидност по-късно била най-блестящо потвърдена от практически опити. научни открития. Например, Менделеев подреди някои вещества в таблицата си съвсем не в съответствие с увеличаването на атомните маси. Той предвиждаше, че периодичността в по-дълбок смисъл все пак се наблюдава не само във връзка с увеличаването на атомното тегло на елементите, но и по друга причина. Великият учен се досещал, че масата на един елемент зависи от количеството на някои по-елементарни частици в неговата структура.
Така периодичният закон по някакъв начин подтикна представителите на науката да се замислят за съставните части на атома. И учените от скоро идващия 20-ти век - векът на грандиозните открития - многократно бяха убедени, че свойствата на елементите зависят от големината на зарядите атомни ядраи структурата на нейната електронна обвивка.

Периодично право и модерност
Периодичната таблица, останала непроменена в основата си, впоследствие беше допълвана и променяна многократно. Той образува така наречената нулева група елементи, която включва инертни газове. Проблемът с поставянето на редкоземни елементи също беше успешно решен. Но въпреки допълненията, значението на откриването на периодичния закон на Менделеев в оригинална версиятрудно е да се надцени.
По-късно, с явленията на радиоактивността, причините за успеха на такава систематизация, както и периодичността на свойствата на елементите, бяха напълно разбрани. различни вещества. Скоро изотопите на радиоактивните елементи също намериха своето място в тази таблица. Атомният номер стана основа за класификацията на множество членове на клетките. И в средата на 20-ти век последователността на елементите в таблицата най-накрая беше обоснована в зависимост от запълването на орбиталите на атомите с електрони, движещи се с голяма скорост около ядрото.
В своята работа от 1668 г. Робърт Бойл предоставя списък на неразложими химични елементи. По това време те бяха само петнадесет. В същото време ученият не твърди, че освен елементите, които изброи, няма повече и въпросът за техния брой остава отворен.
Сто години по-късно френският химик Антоан Лавоазие съставя нов списъкот известни на наукатаелементи. 35 бяха включени в неговия списък химични вещества, от които 23 впоследствие бяха признати за тези много неразложими елементи.
Търсенето на нови елементи се извършва от химици от цял свят и напредва доста успешно. Решаващата роля в този въпрос изигра руският химик Дмитрий Иванович Менделеев: именно той излезе с идеята за възможността за връзка между атомната маса на елементите и тяхното място в „йерархията“. По собствените му думи „необходимо е да се търсят... съответствия между индивидуалните свойства на елементите и техните атомни тегла“.
Сравнявайки известните по това време химични елементи, Менделеев, след колосална работа, в крайна сметка открива тази зависимост, общата закономерна връзка между отделните елементи, в която те се появяват като едно цяло, където свойствата на всеки елемент не са нещо съществуващо. само по себе си, но периодично и редовно повтарящо се явление.
Така през февруари 1869 г. тя е формулирана периодичен закон на Менделеев. През същата година на 6 март доклад, изготвен от Д.И. Менделеев, под заглавие „Връзка на свойствата с атомното тегло на елементите“ беше представена от Н.А. Меншуткин на среща на Руското химическо дружество.
През същата година публикацията се появява в немското списание "Zeitschrift für Chemie", а през 1871 г. подробна публикация на D.I. Менделеев, посветена на неговото откритие – „Die periodische Gesetzmässigkeit der Elemente“ (Периодична закономерност на химичните елементи).
Създаване на периодична таблица
Въпреки факта, че идеята е формирана от Менделеев за доста кратък период от време, той не може да формализира заключенията си дълго време. За него беше важно да представи идеята си под формата на ясно обобщение, строга и визуална система. Както Д.И. Менделеев в разговор с професор А.А. Иностранцев: "Всичко ми се събра в главата, но не мога да го изразя в таблица."
Според биографите след този разговор ученият работи върху създаването на масата в продължение на три дни и три нощи, без да си ляга. Той премина през различни опции, при които елементите могат да се комбинират, за да се организират в таблица. Работата се усложнява и от факта, че по време на създаването на периодичната система не всички химични елементи са били известни на науката.
През 1869-1871 г. Менделеев продължава да развива идеите за периодичност, изтъкнати и приети от научната общност. Една от стъпките беше въвеждането на концепцията за мястото на елемент в периодичната система като съвкупност от неговите свойства в сравнение със свойствата на други елементи.
Въз основа на това, а също и въз основа на резултатите, получени в хода на изследването на последователността на промените в стъклообразуващите оксиди, Менделеев коригира стойностите на атомните маси на 9 елемента, включително берилий, индий, уран и др.
По време на работата на Д.И. Менделеев се опита да попълни празните клетки на своята таблица. В резултат на това през 1870 г. той предсказва откриването на елементи, неизвестни по това време на науката. Менделеев изчислява атомните маси и описва свойствата на три елемента, които все още не са открити по това време:
- "екаалуминий" - открит през 1875 г., наречен галий,
- "екабора" - открита през 1879 г., наречена скандий,
- "ekasilicia" - открита през 1885 г., наречена германий.
Следващите му реализирани прогнози са откриването на още осем елемента, включително полоний (открит през 1898 г.), астат (открит през 1942-1943 г.), технеций (открит през 1937 г.), рений (открит през 1925 г.) и Франция (открит през 1999 г.).
През 1900 г. Дмитрий Иванович Менделеев и Уилям Рамзи стигат до заключението, че е необходимо да се включат елементи от специална, нулева група в периодичната система. Днес тези елементи се наричат благородни газове (до 1962 г. тези газове се наричат инертни газове).

Принципът на организация на периодичната система
В масата си Д.И. Менделеев подрежда химичните елементи в редове в ред на увеличаване на масата, като избира дължината на редовете така, че химичните елементи в същата колона да имат сходни химични свойства.
Благородните газове – хелий, неон, аргон, криптон, ксенон и радон не са склонни да реагират с други елементи и показват ниска химическа активност и затова са в най-дясната колона.
За разлика от тях елементите на най-лявата колона – литий, натрий, калий и други реагират бурно с други вещества, процесът е експлозивен. Елементите в други колони на таблицата се държат по подобен начин - вътре в колоната тези свойства са подобни, но варират при преминаване от една колона в друга.
Периодичната система в първата си версия просто отразява състоянието на нещата, съществуващо в природата. Първоначално таблицата не обясняваше по никакъв начин защо това трябва да е така. И едва с появата на квантовата механика стана ясно истинското значение на подреждането на елементите в периодичната таблица.
В природата се срещат химични елементи до уран (съдържа 92 протона и 92 електрона). Започвайки с номер 93, има изкуствени елементи, създадени в лабораторията.
Не губете.Абонирайте се и получете връзка към статията в имейла си.
Всеки, който е ходил на училище, помни, че един от задължителните предмети за изучаване е химията. Може да й хареса или да не й хареса - няма значение. И вероятно много знания в тази дисциплина вече са забравени и не се прилагат в живота. Въпреки това, всеки вероятно си спомня таблицата на химичните елементи на Д. И. Менделеев. За мнозина тя е останала многоцветна таблица, където във всеки квадрат са изписани определени букви, обозначаващи имената на химичните елементи. Но тук няма да говорим за химията като такава, а ще опишем стотици химична реакцияи процеси, но ще говорим за това как се появи периодичната таблица като цяло - тази история ще бъде интересна за всеки човек, а всъщност и за всички, които са гладни за интересна и полезна информация.
Малко предистория
През далечната 1668 г. изключителният ирландски химик, физик и теолог Робърт Бойл публикува книга, в която са развенчани много митове за алхимията и в която говори за необходимостта от търсене на неразложими химични елементи. Ученият даде и списък от тях, състоящ се само от 15 елемента, но допусна идеята, че може да има повече елементи. Това стана отправна точка не само в търсенето на нови елементи, но и в тяхното систематизиране.
Сто години по-късно френският химик Антоан Лавоазие състави нов списък, който вече включваше 35 елемента. 23 от тях по-късно се оказват неразложими. Но търсенето на нови елементи продължи от учени от цял свят. И водеща роляизвестният руски химик Дмитрий Иванович Менделеев играе в този процес - той е първият, който излага хипотезата, че може да има връзка между атомната маса на елементите и тяхното разположение в системата.
Благодарение на усърдната работа и сравнението на химичните елементи, Менделеев успява да открие връзка между елементите, в която те могат да бъдат едно цяло и техните свойства не са нещо, което се приема за даденост, а са периодично повтарящо се явление. В резултат на това през февруари 1869 г. Менделеев формулира първия периодичен закон и още през март неговият доклад „Връзката на свойствата с атомното тегло на елементите“ е представен на Руското химическо дружество от историка на химията Н. А. Меншуткин. След това през същата година публикацията на Менделеев е публикувана в списание Zeitschrift fur Chemie в Германия, а през 1871 г. нова обширна публикация на учения, посветена на неговото откритие, е публикувана от друго немско списание Annalen der Chemie.
Създаване на периодична таблица

До 1869 г. основната идея вече беше формирана от Менделеев и то за доста кратко време, но той не можеше да я формализира в каквато и да е подредена система, която ясно показва какво е какво, той дълго време не можеше. В един от разговорите с колегата си А. А. Иностранцев той дори каза, че всичко вече се е наредило в главата му, но не може да донесе всичко на масата. След това, според биографите на Менделеев, той започва упорита работа на масата си, която продължава три дни без почивка за сън. Бяха подредени всякакви начини за организиране на елементите в таблица и работата беше усложнена от факта, че по това време науката все още не знаеше за всички химични елементи. Но въпреки това таблицата все пак беше създадена и елементите бяха систематизирани.
Легенда за съня на Менделеев
Мнозина са чували историята, че Д. И. Менделеев е мечтал за масата си. Тази версия беше активно разпространявана от гореспоменатия колега на Менделеев, А. А. Иностранцев, като забавна история, с която той забавляваше своите ученици. Той каза, че Дмитрий Иванович си легнал и насън ясно видял масата си, в която всички химически елементи били подредени в правилния ред. След това студентите дори се пошегуваха, че по същия начин е открита и 40° водка. Но все пак имаше реални предпоставки за историята на съня: както вече споменахме, Менделеев работеше на масата без сън и почивка, а Иностранцев веднъж го намери уморен и изтощен. Следобед Менделеев реши да си почине и известно време по-късно се събуди внезапно, веднага взе лист хартия и изобрази върху него готова маса. Но самият учен опроверга цялата тази история със сън, като каза: „Мислех за това от може би двадесет години, а вие си мислите: седях и изведнъж... готово е. Така че легендата за съня може да е много привлекателна, но създаването на масата е било възможно само чрез упорита работа.

По-нататъшна работа
В периода от 1869 до 1871 г. Менделеев развива идеите за периодичност, към които научната общност е склонна. И един от важните етапи на този процес беше разбирането, че всеки елемент в системата трябва да бъде разположен въз основа на съвкупността от неговите свойства в сравнение със свойствата на други елементи. Въз основа на това, а също и въз основа на резултатите от изследванията в промяната на стъклообразуващите оксиди, химикът успява да промени стойностите на атомните маси на някои елементи, сред които са уран, индий, берилий и други.
Разбира се, Менделеев иска да запълни празните клетки, останали в таблицата възможно най-скоро, и през 1870 г. той предсказва, че скоро ще бъдат открити неизвестни на науката химични елементи, чиито атомни маси и свойства успява да изчисли. Първите от тях са галий (открит през 1875 г.), скандий (открит през 1879 г.) и германий (открит през 1885 г.). След това прогнозите продължиха да се реализират и бяха открити още осем нови елемента, сред които: полоний (1898), рений (1925), технеций (1937), франций (1939) и астат (1942-1943). Между другото, през 1900 г. Д. И. Менделеев и шотландският химик Уилям Рамзи стигат до извода, че елементите от нулевата група също трябва да бъдат включени в таблицата - до 1962 г. те се наричат инертни, а след това - благородни газове.
Организация на периодичната система
Химичните елементи в таблицата на Д. И. Менделеев са подредени в редове, в съответствие с увеличаването на тяхната маса, а дължината на редовете е избрана така, че елементите в тях да имат сходни свойства. Например, благородни газове като радон, ксенон, криптон, аргон, неон и хелий не реагират лесно с други елементи, а също така имат ниска химическа активност, поради което се намират в най-дясната колона. А елементите на лявата колона (калий, натрий, литий и т.н.) реагират перфектно с други елементи, а самите реакции са експлозивни. Казано по-просто, във всяка колона елементите имат сходни свойства, вариращи от една колона до друга. Всички елементи до No 92 се намират в природата, а с No 93 започват изкуствените елементи, които могат да бъдат създадени само в лабораторията.
В първоначалния си вариант периодичната система се разбираше само като отражение на съществуващия в природата ред и нямаше обяснения защо всичко трябва да е така. И едва когато се появи квантовата механика, истинското значение на реда на елементите в таблицата стана ясно.
Уроци по творчески процес
Говорейки за това какви поуки от творческия процес могат да бъдат извлечени от цялата история на създаването на периодичната таблица на Д. И. Менделеев, можем да приведем като пример идеите на английски изследовател в областта на креативно мисленеГреъм Уолъс и френският учен Анри Поанкаре. Нека ги разгледаме накратко.
Според Поанкаре (1908) и Греъм Уолъс (1926) има четири основни етапа в творческото мислене:
- Обучение- етапът на формулиране на основната задача и първите опити за нейното решаване;
- Инкубация- етапът, през който има временно отвличане на вниманието от процеса, но работата по намирането на решение на проблема се извършва на подсъзнателно ниво;
- прозрение- етапът, на който се намира интуитивното решение. Освен това, това решение може да бъде намерено в ситуация, която абсолютно не е от значение за задачата;
- Преглед- етапът на тестване и внедряване на решението, на който се извършва проверката на това решение и евентуалното му по-нататъшно развитие.
Както виждаме, в процеса на създаване на своята таблица Менделеев интуитивно следва тези четири етапа. Колко ефективно е това може да се прецени по резултатите, т.е. защото таблицата е създадена. И като се има предвид, че създаването му е огромна крачка напред не само за химическата наука, но и за цялото човечество, горните четири етапа могат да се прилагат както за изпълнение на малки проекти, така и за изпълнение на глобални планове. Основното нещо, което трябва да запомните, е, че нито едно откритие, нито едно решение на проблем не могат да бъдат намерени сами, колкото и да ни се иска да ги видим насън и колкото и да спим. За да успеете, независимо дали става въпрос за създаване на таблица с химични елементи или разработване на нов маркетингов план, трябва да имате определени знания и умения, както и умело да използвате потенциала си и да работите усилено.
Желаем Ви успех в начинанията и успешно изпълнение на плановете Ви!
Министерство на образованието и науката на Руската федерация
Отдел за образование на администрацията на Твер
Общинска образователна институция
„Вечер (заменяем) общообразователно училище№ 2, Твер
Конкурс за ученически есета "Кръгозор"
Резюме по темата:
Историята на откриването на периодичния закон и периодичната таблица на химичните елементи от Дмитрий Иванович Менделеев
студент от 8-ма група на MOU VSOSH № 2, Твер
Ръководител:
учител по химия от най-висока категория
МОУ ВСОШ № 2, Твер
Въведение……………………………………………………………………………………………………………………………. .......... ........................3
1. Предпоставки за откриване на Периодичния закон ……..4
1.1. Класификация …………………………………………..4
1.2. Триадите на Дьоберейнер и първите системи от елементи……………………………….4
1.3. Спирала на Шанкуртоа ………………………………………………………………………..5
1.5 Таблици на Одлинг и Майер…………………………………………………………….7
2. Откриване на периодичния закон……………………………….9
Заключение………………………………………………………………………………. 16
Литература………………………………………………………………………….17
Въведение
Периодичният закон и периодичната таблица на химичните елементи са в основата на съвременната химия.
Менделеев назова градове, фабрики, учебни заведения, изследователски институти. В чест на Русия е одобрен златен медал - той се присъжда за изключителна работа в областта на химията. Името на учения е дадено на Руското химическо дружество. В чест на годишните регионални Менделеевски четения се провеждат в Тверска област. Дори елементът със сериен номер 101 получи името менделевий в чест на Дмитрий Иванович.
Основната заслуга е откриването на периодичния закон и създаването на периодична система от химични елементи, което увековечи името му в световната наука. Този закон и периодичната система са в основата на цялото по-нататъшно развитие на учението за атомите и елементите, те са основата на химията и физиката на нашите дни.
Обективен:проучете предпоставките за възникването на периодичния закон и периодичната система от химични елементи и оценете приноса към това откритие на Дмитрий Иванович Менделеев.
1. Предпоставки за откриването на Периодичния закон
Търсенето на основата на естествената класификация на химичните елементи и тяхното систематизиране започва много преди откриването на Периодичния закон. По времето, когато е бил открит Периодичния закон, са били известни 63 химични елемента, описани са съставът и свойствата на техните съединения.
1.1 Класификация
Един изключителен шведски химик разделя всички елементи на метали и неметали въз основа на различията в свойствата на простите вещества и образуваните от тях съединения. Той определи, че металите съответстват на основни оксиди и основи, а неметалните - на киселинни оксиди и киселини.
Таблица 1. Класификация
1.2. Триадите на Дьоберейнер и първите системи от елементи
През 1829 г. немският химик Йохан Волфганг Дьоберейнер прави първия значителен опит да систематизира елементите. Той забелязал, че някои елементи, сходни по своите свойства, могат да бъдат комбинирани в групи от три, които той нарече триади.
Същността на предложения закон за триадата на Дьоберейнер беше, че атомната маса на средния елемент на триадата е близка до половината от сбора (средно аритметично) от атомните маси на двата крайни елемента на триадата. Въпреки факта, че триадите на Деберейнер са до известна степен прототипите на групите на Менделеев, тези представи като цяло са все още твърде несъвършени. Липсата на магнезий в едно семейство калций, стронций и барий, или кислород в семейството на сяра, селен и телур, е резултат от изкуствено ограничаване на агрегатите от подобни елементи само до тройни съюзи. Много показателен в този смисъл е провалът на Деберейнер да отдели триада от четири елемента със сходни свойства: P, As, Sb, Bi. Дьоберейнер ясно вижда дълбоки аналогии в химичните свойства на фосфора и арсена, антимона и бисмута, но, ограничавайки се предварително до търсенето на триади, не може да намери правилното решение. Половин век по-късно Лотар Майер ще каже, че ако Дьоберейнер дори за кратко се беше отклонил от своите триади, той веднага щеше да види приликата на всички тези четири елемента едновременно.
Въпреки че Дьоберейнер естествено не успя да разбие всички известни елементи на триади, законът за триадите ясно показва съществуването на връзка между атомната маса и свойствата на елементите и техните съединения. Всички по-нататъшни опити за систематизиране се основават на разположението на елементите в съответствие с техните атомни маси.
1.3. Спирала на Шанкуртоа (1862 г.)
Професорът от Парижкото висше училище Александър Бегие дьо Шанкуртоа подреди всички известни по това време химични елементи в една последователност на увеличаване на техните атомни маси и приложи получената серия към повърхността на цилиндъра по линия, излизаща от основата му в ъгъл от 45 ° спрямо равнината на основата (т.нар. земна спирала). Когато повърхността на цилиндъра беше разгъната, се оказа, че по вертикални линии, успоредни на оста на цилиндъра, има химически елементи с подобни свойства. И така, литий, натрий, калий паднаха на една вертикала; берилий, магнезий, калций; кислород, сяра, селен, телур и др. Недостатъкът на спиралата на дьо Шанкуртоа е фактът, че по една и съща линия с химическа природаВ същото време елементи с напълно различно химическо поведение също се оказаха елементи. Манганът попада в групата на алкалните метали, а титанът, който няма нищо общо с тях, попада в групата на кислорода и сярата. Така за първи път се роди идеята за периодичността на свойствата на елементите, но те не й обърнаха внимание и скоро беше забравена.
Малко след спиралата на дьо Шанкуртоа американският учен Джон Нюландс прави опит да съпостави химичните свойства на елементите с техните атомни маси. Подреждайки елементите във възходящ ред на техните атомни маси, Нюландс забеляза, че има сходство в свойствата между всеки осми елемент. Нюландс нарече намерения модел закон за октавите по аналогия със седемте интервала на музикалната скала. В своята таблица той подреди химичните елементи във вертикални групи от по седем елемента всяка и по този начин установи, че (с малка промянаот порядъка на някои елементи), подобни по химични свойства елементи се появяват на една и съща хоризонтална линия. Джон Нюландс, разбира се, беше първият, който даде серия от елементи, подредени във възходящ ред на атомните маси, присвоил съответния сериен номер на химичните елементи и забелязал систематична връзка между този ред и физичните химични свойстваелементи. Той пише, че в такава последователност се повтарят свойствата на елементите, чиито еквивалентни тегла (маси) се различават със 7 единици или със стойност, кратна на 7, т.е. сякаш осмият елемент по реда повтаря свойства на първата, тъй като в музиката осмата нота се повтаря първа.
Нюландс се опита да придаде универсален характер на тази зависимост, която всъщност има за светлинни елементи. В неговата таблица подобни елементи бяха подредени в хоризонтални редове, но елементи с напълно различни свойства често се оказваха в един и същи ред. Лондонското химическо дружество посрещна неговия закон за октави с безразличие и предложи на Нюландс да се опита да подреди елементите по азбучен ред и да идентифицира всеки модел.
1.5 Таблици на Одлинг и Майер
През същата 1864 г. се появява първата маса на немския химик Лотар Майер; В него бяха включени 28 елемента, разположени в шест колони според техните валентности. Майер умишлено ограничи броя на елементите в таблицата, за да подчертае закономерната (подобна на триадите на Дьоберейнер) промяна в атомната маса в серии от подобни елементи.
Фиг. 3. Таблица на Майер на химичните елементи
През 1870 г. Майер публикува нова таблица, наречена Природата на елементите като функция на тяхното атомно тегло, състояща се от девет вертикални колони. Подобни елементи бяха разположени в хоризонталните редове на таблицата; Майер остави някои клетки празни. Таблицата беше придружена от графика на атомния обем на елемента спрямо атомното тегло, която има характерна форма на трион, която идеално илюстрира термина « периодичност », вече предложена по това време от Менделеев.
2. Откриване на периодичния закон
Има няколко истории от близки хора за това как е бил открит Периодичния закон; тези истории са предавани устно от очевидци, след което проникват в пресата и се превръщат в своеобразна легенда, която все още не е проверена поради липсата на съответни документални данни. Интересна е историята на професора по геология от Санкт Петербург. Университет (), близък приятел. , който посети точно в онези дни, когато открива периодичния закон, дава любопитни щрихи за това как е работил по създаването на своята система от елементи, който публикува историята, пише:
„За финалния творчески процес на интуицията на Менделеев, уважаемият професор Александър Александрович Иностранцев любезно ме информира в най-високата степенинтересни неща. Веднъж, вече като секретар на Физико-математическия факултет, А. А. отиде да посети Менделеев, с когото като учен и близък приятел беше в постоянна връзка. духовно общение. Вижда: Д. И. стои на бюрото, очевидно в мрачно, потиснато състояние.
Какво правиш, Дмитрий Иванович?
Менделеев говори за това, което по-късно е въплътено в периодичната таблица на елементите, но в този момент законът и таблицата все още не са били формирани: „Всичко се е развило в главата ми“, добави Менделеев горчиво, „но не мога да го изразя на маса.” Малко по-късно се случи следното. Менделеев прекарва три дни и три нощи, без да си ляга, работейки на бюрото, опитвайки се да обедини резултатите от своята мисловна конструкция в таблица, но опитите да постигне това бяха неуспешни. Накрая, под влиянието на силна умора, Менделеев си легна и веднага заспа. „Виждам насън маса, където елементите са подредени според нуждите. Събудих се, веднага го записах на лист - само на едно място впоследствие се оказа необходимата поправка.
Освен това е необходимо да се вземе предвид неговото свидетелство в „Основи на химията“ за това как при окончателната формулировка на своята класификация на елементите той е използвал карти, на които са написани данни за отделни елементи. Картите бяха необходими именно за идентифициране на все още неизвестната връзка между елементите, а не изобщо за окончателния й дизайн. И най-важното, както се вижда от първоначалната чернова на таблицата, картите с елементите, написани върху тях, първоначално бяха разположени не в реда на групи и редове (периоди), а само в реда на групите (периодите все още не бяха отворен в началото). Групите бяха поставени една под друга и именно разположението на групите доведе до откритието, че вертикалните колони (периоди) на елементите се прилягат един към друг, образувайки общ непрекъснат ред от елементи, в който определени химични свойства са периодично се повтаря. Това всъщност беше откритието на периодичния закон.
Освен това, ако съществуването не само на групи, но и на периоди на елементи вече беше известно, тогава нямаше да има нужда да се прибягва до карти за отделни елементи.
Третата история, предадена отново от думите на самия него, идва от близък приятел - изключителен чешки химик. Тази история е публикувана от Браунер през 1907 г. след смъртта на неговия голям приятел; през 1930г той е препечатан в сборник с произведения на чехословашки химици. По време на Втората световна война Джералд Друс включва тази история в биографията си на Богуслав Браунер. Според Браунер, той му разказал за това как съставянето на учебник по химия, тоест „Основи на химията“, помогнало за откриването и формулирането на периодичния закон.
"Когато започнах да пиша моя учебник", каза Браунър, "почувствах, че е необходима система, която да ми позволи да разпределя химически елементи. Открих, че всички съществуващи системи са изкуствени и следователно неподходящи за целта ми; Опитах се да установя естествени системи За тази цел написах върху малки парчета картон знаците на елементите и техните атомни тегла, след което започнах да ги групирам различни начиниспоред приликата им. Но този метод не ме удовлетвори, докато не подредих кашоните една след друга според увеличаването на атомното тегло. Когато поставих първия ред в таблицата:
H=1, Li=7, Be=9, B=11, C=12, N=14, O=16, F=19,
Открих, че следните елементи могат да образуват втори ред под първия, но да започват под li. След това открих това в този нов ред:
Na=23, Mg=24, Al=27, Si=28, P=31, S=32, Cl=35,5
натрият повтаря всяко свойство на лития; същото се случва и със следните елементи. Същото повторение се случва в третия ред, след определен период, и продължава във всички редове.
Такава е историята, предадена от думите му. Освен това, в обяснението и развитието на тази история се казва, че той „подреди подобни елементи в групи и, в зависимост от увеличаването на атомните тегла, в редове, в които свойствата и природата на елемента се променят постепенно, както може да се види по-горе. От лявата страна на масата му бяха "електроположителни" елементи, от дясната "електроотрицателни". Той провъзгласи своя закон със следните думи"
По този начин историята, предадена от него от думи, не засяга цялото откритие като цяло и не цялата история на създаването на естествената система от елементи, а само последния етап от това откритие, когато на базата на вече създадена система, той успя да открие и формулира периодичния закон на химичните вещества, лежащи в основата на тази система.елементи. Накратко, историята, дадена от Браунер, не се отнася до историята на съставянето на системата от елементи, а до историята на формулирането на периодичния закон на базата на вече съставена система.
Указание за съществуването на четвърта версия се съдържа в редакционния послеслов към втория том с избрани произведения, публикуван през 1934 г. и съдържащи произведения, свързани с периодичния закон. пише, че в посочения том "само една статия" коментар j "ai trouve la loi periodique" не е поставен като по-биографичен. По някаква причина той не е дал връзки къде е публикувана тази статия. Тази статия, естествено, предизвика огромен интерес, тъй като, съдейки по името му, можеше да се очаква, че най-накрая ще даде отговор на въпроса, интересуващ всички химици за това как е бил открит периодичният закон, и този отговор ще бъде получен не от трети страни от думи , но от него самия. Позоваването на факта, че тази статия е изключена от проф. като уж по-биографична по своята същност изглеждаше напълно неоснователно. Ето защо тя трябваше да бъде включена в сборника на трудовете по периодичния закон, а не да бъде изключена от тази колекция. че във френското списание за чиста и приложна химия за 1899 г. всъщност е публикувана статия под интригуващото заглавие „Коментар j“ ai trouve le systeme periodique des elements“ („Как открих периодичната система mu елементи"). В бележка под линия към тази статия редакторите на списанието съобщават, че са се обърнали към Д. И. Менделеев по повод избирането му през 1899 г. чуждестранен член-кореспондент на Парижката академия на науките с молба да напише за списание за неговата периодична система. изпълни тази молба с голямо удоволствие и изпрати работата си, написана на руски език, във френско списание. Преводът на това произведение на френски език е извършен от самите редактори.
Най-близкото запознаване с текста, публикуван на Френскистатия показва, че това не е някакво нова работа, но точен преводот неговата книга "Периодичен закон на химичните елементи", за която пише енциклопедичен речникБрокхаус и Ефрон и е публикуван в XXIII том на този речник през 1898 г. Очевидно преводачът или редакторите на френското списание, за да придадат по-голям интерес, смениха привидно твърде сухото заглавие: „Периодичен закон на химичните елементи“ на интригуващото: „Как намерих периодичната таблица на елементите“. Иначе всичко остана непроменено и той не добави нищо биографично към статията си.
Това са легендите и историите за това как е била открита периодичната таблица на химичните елементи. Всички неясноти, генерирани от тях по-горе, могат да се считат за елиминирани благодарение на откриването и изследването на нови материали, свързани с историята на това велико откритие.

Фиг.4. "Опит от системата от елементи"
На 6 март 1869 г., на заседание на Руското химическо дружество, в отсъствието на Менделеев (Менделеев е бил в сирене в Тверска област и вероятно е спрял в имението си "Боблово" в Московска област), съобщение за беше направено откриването на периодичния закон, след като получи за следващия брой на списанието си („Журнал на Руското химическо общество“) статия.
През 1871 г. в последната статия „Периодичен закон на химичните елементи“ Менделеев дава следната формулировка на периодичния закон: „Свойствата на елементите и следователно свойствата на образуваните от тях прости и сложни тела са в периодично зависимост от атомното тегло." В същото време Менделеев придаде на периодичната си таблица форма, която стана класическа (т.нар. кратка версия).
За разлика от своите предшественици, Менделеев не само състави таблица и посочи наличието на несъмнени модели в числените стойности на атомните тегла, но и реши да назове тези модели общо правоприродата. Въз основа на предположението, че атомната маса определя свойствата на даден елемент, той си позволи да промени приетите атомни тегла на някои елементи и да опише подробно свойствата на елементите, които все още не са открити.

Фиг.5. Периодична система от химични елементи
Д. И. Менделеев дълги години се бори за признаването на Периодичния закон; идеите му получават признание едва след като са открити елементите, предсказани от Менделеев: галий (Пол Лекок дьо Бойсбаудран, 1875), скандий (Ларс Нилсон, 1879) и германий (Клеменс Винклер, 1886) - съответно екаалуминий и екаиликон. От средата на 1880-те Периодичният закон най-накрая е признат за един от теоретични основихимия.
Заключение
Периодичният закон изигра огромна роляв развитието на химията на др естествени науки. Открита е взаимната връзка между всички елементи, техните физични и химични свойства. Това постави пред естествената наука научен и философски проблем от голямо значение: тази взаимна връзка трябва да бъде обяснена. След откриването на Периодичния закон стана ясно, че атомите на всички елементи трябва да бъдат изградени по единен принцип, а структурата им трябва да отразява периодичността на свойствата на елементите. Така периодичният закон се превърна във важно звено в еволюцията на атомната и молекулярната наука, оказвайки значително влияние върху развитието на теорията за структурата на атома. Той също така допринася за формулирането на съвременната концепция за "химичен елемент" и усъвършенстването на идеите за прости и сложни вещества. Напредъкът в атомната физика, вкл ядрената енергияи синтеза на изкуствени елементи, стана възможен само благодарение на Периодичния закон.
„Новите теории, брилянтните обобщения ще идват и си отиват. Нови идеи ще заменят вече остарелите ни концепции за атома и електрона. Най-големите откритияи експериментите ще анулират миналото и отворените хоризонти, които днес са невероятни по новост и широта - всичко това ще дойде и ще си отиде, но Периодичният закон на Менделеев винаги ще живее и ще ръководи търсенията.
Библиография
2. . Основи на химията. - Т. 2. - М. - Л.: Гошимиздат, 1947. - 389 с.
3. . Избрани лекции по химия. - М .: По-високо. училище, 1968г. - 224 стр.
4. . Нови материали за историята на откриването на периодичния закон. - М.-Л.: Издателство Акад. Науки на СССР, 1950 г. - 145 стр.
пет.. Философски анализ на първите произведения по периодичния закон (). - М.: Издателство на акад. Науки на СССР, 1959 г. - 294 стр.
6. . Философия на изобретението и изобретение във философията. - Т.2. - М.: Наука и училище, 1922.- С.88.