1.Mely szénhidrogéneket nevezzük telítetlennek és hogyan osztják fel őket? Írj általános képletek Nem telített szénhidrogének.
A telítetlen szénhidrogének azok, amelyek egy vagy több többszörös kötést tartalmaznak. Fő osztályok telítetlen szénhidrogének: alkének, alkinek és alkadiének.
2. Az alkének a következők:
3)
3. Az alapján modern ötletek az elektronpályákról, jellemezze az etilénmolekulában lévő kémiai kötések természetét. 
4. Egy etilén molekulában a σ-kötések száma egyenlő:
2) 5
5. Milyen típusú izoméria figyelhető meg telített és telítetlen szénhidrogénekben? 
6. Rajzolj összehúzódásokat szerkezeti képletek minden olyan szénhidrogén, amelynek molekulaképlete . Nevezze meg ezeket a kapcsolatokat! 
7. Miért nagyobb az etilén sorozat szénhidrogéneiben az izomerek száma, mint a telített szénhidrogénekben? Ennek bizonyítására adja meg a szénhidrogének izomerjeit molekuláris képletekÉs . 
8. A pentén-1 izomerje az
3) 2-metil-butén-1
9. A propén homológja az
1) butén-1
10. Hogyan állítják elő az etilént és az etilén sorozat szénhidrogéneit? Írja fel a megfelelő reakciók egyenleteit! 
11. Mi kémiai tulajdonságai rendelkezik az etilénnel és homológjaival? Erősítse meg válaszát a megfelelő reakciók egyenleteivel. 
 12. Írja fel az etilén és propilén égésének reakcióegyenleteit, valamint kölcsönhatásukat brómos vízzel és kálium-permanganát oldattal!
12. Írja fel az etilén és propilén égésének reakcióegyenleteit, valamint kölcsönhatásukat brómos vízzel és kálium-permanganát oldattal! 
13. Hogyan lépnek reakcióba a propilén és a butének a hidrogén-halogenidekkel? E példák segítségével magyarázza el Markovnyikov uralmának lényegét. 
14. Milyen célokra használják az etilént és a propilént?
Az etilént etilénglikol, polietilén, etilalkohol. Ezenkívül az etilén felgyorsítja a gyümölcsök érését. Az izopropil-alkoholt és a polipropilént propilénből nyerik.
15. Milyen reakciókat nevezünk polimerizációs reakcióknak? Írja fel a propilén polimerizációs reakciójának egyenletét! 
16. Írjon egyenleteket! kémiai reakciók, megerősítve genetikai kapcsolat a szerves vegyületek osztályai között az 5. sémában. 
 1. feladat Számítsa ki:
1. feladat Számítsa ki:
a) mekkora térfogatú és tömegű etilén nyerhető 160 ml 0,8 g/cm3 sűrűségű etil-alkoholból; b) mekkora térfogatú abszolút (vízmentes) etil-alkohol (ρ=0,8 g/cm3) nyerhető 100 m3 etilénből (n.s.) 
 2. feladat Az etilén brómos vízen való átvezetésekor az oldat tömege 7 g-mal nőtt Mekkora térfogatú gáz reagált és mekkora tömegű 1,2-dibróm-etán keletkezett (sz.)?
2. feladat Az etilén brómos vízen való átvezetésekor az oldat tömege 7 g-mal nőtt Mekkora térfogatú gáz reagált és mekkora tömegű 1,2-dibróm-etán keletkezett (sz.)? 
3. feladat Mekkora térfogatú etilénre (sz.) lesz szükség 126 kg etilén-oxid előállításához, ha tömeghányad az etilén termelési vesztesége 0,1? 
4. feladat Mekkora levegőmennyiség szükséges 50 liter propilén elégetéséhez (n.o.)? 
mi a különbség a szigma és pi kötések között etilén és acetilén molekulákban → és megkaptam a legjobb választ
Yatyan Ivanov[guru] válasza
A szigmakötések létrejöhetnek hibrid és/vagy nem hibrid pályákon, de mindig az atomok középpontjait összekötő tengely mentén irányulnak. A szénatomban a szigma kötések csak hibrid pályákon keresztül jönnek létre Pi kötések csak a molekula síkjára (és az atomok középpontjait összekötő egyenesre) merőlegesen elhelyezkedő nem hibrid p-pályák révén. A pi-kötést a p-pályák oldalirányú átfedése jellemzi a molekula síkja felett és alatt elektronfelhők(pályák) a szigma kötésben nagyobbak, mint a pi kötésben, ezért a szigma kötés erősebb Az etilén és az acetilén molekulákban lévő kötések jellemzői - Mindkét molekulában a szénatomok szigma kötésekkel kapcsolódnak a hidrogénatomokhoz (hibrid pályák). a szénatomok átfedésben vannak a hidrogénatomok nem hibrid s-pályáival - Mindkét molekulában többszörös kötések vannak a szénatomok között, azaz vannak szigmakötések és pi-kötések is - A C2H4 etilénmolekulában a szénatom a következő állapotban van sp2 hibridizáció (3 hibrid sp2 -pálya és 1 nem hibrid p-pálya); a C2H2 acetilénmolekulában a szénatom sp-hibridizált állapotban van (2 hibrid sp-pálya és 2 nem-hibrid p-pálya - Ezért az etilénmolekulában kettős kötés van a szénatomok között (1 szigma és 1 pi kötés), acetilén molekulában pedig hármas kötés (1 szigma és 2 pi kötés kölcsönösen elhelyezkedő merőleges síkok) . Hossz S-S csatlakozások az acetilén molekulában kisebb, mint az etilén molekulában, és a kötés erőssége mind az etilént, mind az acetilént addíciós reakciók jellemzik a pi-kötésnél, amely kevésbé erős, és ezért reaktívabb, mint a szigma kötés. Az acetilén molekulában az addíció 2 szakaszban megy végbe: először az egyik pi kötés mentén, majd a másik mentén.
Válasz tőle Xenia[guru]
A szigma kötések egyszeri, egyszerű, erős kötések.
A Pi-kötések nem erős kötések.
És hogy milyen anyagokban nem számít.
A csatlakozási vonal mentén s-atomi pályák átfedésével hajtják végre atomok, pi kötések, akkor fordulnak elő, ha az atomi kötésvonal két oldalán lévő p-atomi pályák átfedik egymást. Úgy gondolják, hogy a pi kötés több kötésben valósul meg - kettős kötés egy szigma és egy pi kötésből áll, hármas - egy szigma és két ortogonális pi kötésből.
Kidolgozta a szigma és pi kötés fogalmát Linus Pauling a múlt század 30-as éveiben. Egy s- és három p-valencia elektron atom szén vannak kitéve hibridizációés négy ekvivalens sp 3 hibridizált elektron lesz, amelyen keresztül négy ekvivalens kémiai kötések V molekula metán. A metánmolekulában lévő összes kötés egyenlő távolságra van egymástól, tetraéder konfigurációt alkotva.
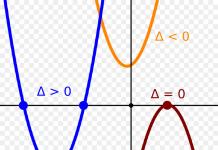
Kettős kötés kialakulása esetén a szigma kötések sp 2 hibridizált pályák révén jönnek létre. Az ilyen kötések száma egy szénatomban összesen három, és ugyanabban a síkban helyezkednek el. A kötések közötti szög 120°. A pi kötés a jelzett síkra merőlegesen helyezkedik el (1. ábra).
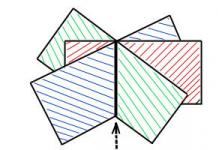
Hármas kötés kialakulása esetén a szigma kötések sp-hibridizált pályák révén jönnek létre. Az ilyen kötések száma egy szénatomon összesen kettő, és 180°-os szöget zárnak be egymással. Egy hármas kötés két pi kötése egymásra merőleges (2. ábra).
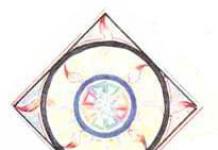
Aromás rendszer kialakulása esetén pl. benzol C 6 H 6, a hat szénatom mindegyike sp 2 hibridizációs állapotban van, és három szigma kötést képez 120°-os kötési szöggel. Minden szénatom negyedik p-elektronja merőleges a benzolgyűrű síkjára (3. ábra). Általában egy egyszeres kötés jelenik meg, amely a benzolgyűrű összes szénatomjára kiterjed. Két nagy pi-kötés régió jön létre elektronsűrűség a szigma kötéssík mindkét oldalán. Egy ilyen kötéssel a benzolmolekula összes szénatomja egyenértékűvé válik, ezért egy ilyen rendszer stabilabb, mint egy három lokalizált kettős kötéssel rendelkező rendszer. A nem lokalizált pi kötés a benzolmolekulában a szénatomok közötti kötési sorrend növekedését és a magok közötti távolság csökkenését okozza, azaz kémiai kötés hossza d cc egy benzolmolekulában 1,39 Å, míg d C-C = 1,543 Å és d C=C = 1,353 Å.
L. Pauling szigma és pi kötések koncepciója szerves részévé vált vegyértékkötés elmélet. Az atompálya hibridizációjáról mára animált képeket fejlesztettek ki.
Maga L. Pauling azonban nem elégedett meg a szigma- és pi-kötések leírásával. Egy elméleti szimpóziumon szerves kémia emlékének szentelve F. A. Kekule(London, 1958. szeptember) elhagyta a σ, π-leírást, javasolta és megindokolta hajlított kémiai kötés elmélet. Új elmélet egyértelműen figyelembe vették fizikai jelentése kovalens kémiai kötés, nevezetesen Coulomb elektronkorreláció.
Megjegyzések
Lásd még
| Kémiai kötés | |||||||
|---|---|---|---|---|---|---|---|
|
|||||||
| Intermolekuláris kölcsönhatás |
|||||||
Wikimédia Alapítvány.
2010.
Nézze meg, mit jelent a „Pi-kötés” más szótárakban:
A kommunikáció a technológiában az információ (jelek) távolságon keresztüli továbbítása. Tartalom 1 Történelem 2 Kommunikáció típusai 3 Jel ... Wikipédia KAPCSOLAT, kapcsolatok, kapcsolatról, kapcsolatban és (valakivel lenni) kapcsolatban, feleségek. 1. Ami összeköt, összeköt valamit valamivel; olyan kapcsolat, amely valami között valami közöset hoz létre, kölcsönös függést, feltételességet. „...A tudomány és a... Szótár
Ushakova
- (koreai: 조선민주주의인민공화국의 통신) ezek mind a KNDK-ban működő kommunikációs szolgáltatások. A KNDK izolacionista politikája miatt polgárai nem használhatják az internetet. Tartalom 1 Telefonos kommunikáció 1.1 ... Wikipédia És, előz. a kommunikációról, kapcsolatban és kapcsolatban; és. 1. Kölcsönös függőségi viszony, feltételesség. Közvetlen, közvetett, logikai, szerves, oksági o. C. tények, jelenségek, események. C. az ipar között és mezőgazdaság . S. tudomány és......
Enciklopédiai szótár
A kapcsolat a közösség, a kapcsolat vagy a következetesség kapcsolata. Kommunikáció - az információ távolsági továbbításának képessége (beleértve: rádiórelé kommunikációt, cellás kommunikációt, műholdas kommunikációt és más típusokat). Az atomok kémiai kötése ... Wikipédia
Kommunikáció (film, 1996) Ennek a kifejezésnek más jelentése is van, lásd: Kommunikáció (film). Kötött kapcsolat... Wikipédia Tengelykapcsoló, összekötő lengőkar. Gondolatok, fogalmak összekapcsolása, eszmetársítás. Lásd unió.. hatásos kapcsolat... Orosz szinonimák és hasonló kifejezések szótára. alatt. szerk. N. Abramova, M.: Orosz szótárak, 1999. kapcsolat, logika, koherencia, ... ...
Szinonimák szótára Főnév, g., használt. gyakran Morfológia: (nem) mi? kapcsolatok, mi? kapcsolatok, (lásd) mi? kapcsolat mivel? kapcsolat, miről? a kommunikációról; pl. Mi? kapcsolat, (nem) mi? kapcsolatok, mi? kapcsolatok, (lásd) mi? kapcsolatok, mi? kapcsolatok, mi? a kapcsolatokról 1. A kapcsolatokat kapcsolatoknak nevezzük... ...
Dmitriev magyarázó szótára Információk kommunikációja, továbbítása és fogadása különféle eszközökkel; ipar, információtovábbítást biztosítva. S. fontos szerepet játszik a termelésben gazdasági tevékenység társadalom és kormány, felfegyverkezve...... Nagy Szovjet Enciklopédia
Egy szigma és egy pi kötésből áll, a hármas kötés egy szigma és két ortogonális pi kötésből áll.
A szigma és pi kötések koncepcióját Linus Pauling dolgozta ki a múlt század 30-as éveiben.
L. Pauling szigma és pi kötések koncepciója a vegyértékkötések elméletének szerves részévé vált. Az atompálya hibridizációjáról mára animált képeket fejlesztettek ki.
Maga L. Pauling azonban nem elégedett meg a szigma- és pi-kötések leírásával. A F.A. Kekule emlékének szentelt elméleti szerves kémia szimpóziumon (London, 1958. szeptember) elhagyta a σ, π-leírást, javasolta és alátámasztotta a hajlított kémiai kötés elméletét. Az új elmélet egyértelműen figyelembe vette a kovalens kémiai kötések fizikai jelentését.
Enciklopédiai YouTube
1 / 3
Pi kötések és sp2 hibridizált pályák
A szénatom szerkezete. Szigma és pi kötések. Hibridizáció. 1. rész
Kémia. Kovalens kémiai kötés V szerves vegyületek. Foxford Online Oktatási Központ
Feliratok
Az utolsó videóban a szigma kommunikációról beszéltünk. Egy izolált szénatomnak van egy 2s pályája és 3 2p pályája az x tengely mentén, az y tengely mentén és a z tengely mentén. hidrogén atom. Ez az atom itt lesz. . A jobb megértés érdekében nézzük meg az acetilén példáját.