2.2. Үелэх систем үүссэн түүх.
1867-68 оны өвөл Менделеев "Химийн үндэс" сурах бичгийг бичиж эхэлсэн бөгөөд баримт материалыг системчлэхэд тэр даруй бэрхшээлтэй тулгарсан. 1869 оны 2-р сарын дунд үе гэхэд тэрээр сурах бичгийн бүтцийг тунгаан бодож байхдаа аажмаар түүний шинж чанаруудтай гэсэн дүгнэлтэд хүрчээ. энгийн бодисууд(мөн энэ бол оршихуйн нэг хэлбэр юм химийн элементүүдчөлөөт төлөвт) ба элементүүдийн атомын масс нь тодорхой загвараар холбогддог.
Менделеев өмнөх хүмүүсийн химийн элементүүдийг атомын массыг нэмэгдүүлэх дарааллаар байрлуулах оролдлого, энэ тохиолдолд тохиолдсон тохиолдлын талаар сайн мэдэхгүй байв. Жишээлбэл, түүнд Шанкуртуа, Ньюландс, Мейер нарын ажлын талаар бараг мэдээлэл байгаагүй.
Түүний бодлын шийдвэрлэх үе шат 1869 оны 3-р сарын 1-нд (2-р сарын 14, хуучин хэв маяг) ирэв. Нэг өдрийн өмнө Менделеев Тверь муж дахь артелийн бяслагны сүүний үйлдвэрийг шалгахын тулд арав хоногийн чөлөө авах хүсэлтээ бичжээ: тэрээр Чөлөөт эдийн засгийн нийгэмлэгийн удирдагчдын нэг А.И.Ходневээс бяслаг үйлдвэрлэлийг судлах зөвлөмж бүхий захидал хүлээн авчээ.
Санкт-Петербург хотод тэр өдөр бүрхэг, хүйтэн жавартай байв. Менделеевийн байшингийн цонхыг хардаг их сургуулийн цэцэрлэгийн моднууд салхинд хийсч байв. Дмитрий Иванович орондоо хэвтэж байхдаа аяга бүлээн сүү ууж, босоод нүүрээ угааж, өглөөний цайгаа уув. Тэр гайхалтай сайхан сэтгэлтэй байсан.
Өглөөний цайны үеэр Менделеев янз бүрийн химийн элементүүдийн ижил төстэй атомын масс, тэдгээрийн химийн шинж чанарыг харьцуулах санаанд оромгүй санаа төрсөн. Хоёр ч удаа бодолгүйгээр, арын талХодневын захидалд тэрээр 35.5 ба 39-тэй тэнцүү атомын масстай хлор Cl ба калийн К-ийн тэмдэглэгээг бичжээ (ялгаа нь ердөө 3.5 нэгж). Үүнтэй ижил захидал дээр Менделеев бусад элементүүдийн тэмдэглэгээг зурж, тэдгээрийн хооронд ижил төстэй "парадоксик" хосуудыг хайж олжээ: фтор F ба натрийн Na, бром Br ба рубидиум Rb, иод I ба цезий Cs, тэдгээрийн массын зөрүү 4.0-ээс 5.0 хүртэл нэмэгддэг. , дараа нь 6.0 хүртэл. Илт металл бус ба металлуудын хоорондох "тодорхойгүй бүс" нь үнэт хий агуулсан элементүүдийг агуулж байгааг Менделеев тэр үед мэдэж чадахгүй байсан бөгөөд тэдгээрийг нээсэн нь дараа нь үечилсэн хүснэгтийг ихээхэн өөрчлөх болно.
Өглөөний цайгаа уусны дараа Менделеев ажлын өрөөндөө цоожлоо. Тэр нэг боодол гаргаж ирэв нэрийн хуудасмөн тэдгээрийн ар тал дээр элементүүдийн тэмдэг, тэдгээрийн химийн үндсэн шинж чанаруудыг бичиж эхлэв. Хэсэг хугацааны дараа гэрийнхэн оффисын дууг сонсов: "Хөөх, би тэднийг алах болно!" Эдгээр уриалга нь Дмитрий Иванович бүтээлч урам зоригтой байсан гэсэн үг юм. Менделеев картуудыг нэг хэвтээ эгнээнээс нөгөөд шилжүүлж, атомын массын утгууд болон ижил элементийн атомуудаас үүссэн энгийн бодисын шинж чанарыг удирдан чиглүүлсэн. Дахин нэг удаа нарийн мэдлэг түүнд тусалсан органик хими. Химийн элементүүдийн ирээдүйн үечилсэн системийн хэлбэр аажмаар гарч ирэв. Тиймээс тэр эхлээд бериллий Be элементтэй карт тавьсан. атомын масс 14) хөнгөн цагаан элементийн картын хажууд Al (атомын масс 27.4) тухайн үеийн уламжлалын дагуу бериллийг хөнгөн цагааны аналог гэж андуурчээ. Гэсэн хэдий ч дараа нь химийн шинж чанарыг харьцуулсны дараа тэрээр магнийн Mg дээр бериллийг байрлуулсан. Тэрээр бериллийн атомын массын нийтээр хүлээн зөвшөөрөгдсөн утгыг эргэлзэж, 9.4 болгож, бериллийн ислийн томъёог Be 2 O 3-аас BeO (магнийн исэл MgO гэх мэт) болгон өөрчилсөн. Дашрамд хэлэхэд бериллийн атомын массын "зассан" утгыг зөвхөн арван жилийн дараа баталсан. Тэр бусад тохиолдлуудад ч гэсэн зоригтой ажилласан.
Аажмаар Дмитрий Иванович атомын массыг нэмэгдүүлэх дарааллаар байрлуулсан элементүүд нь физик, химийн шинж чанарын тодорхой үечлэлийг харуулдаг гэсэн эцсийн дүгнэлтэд хүрчээ. Өдрийн турш Менделеев элементүүдийн систем дээр ажиллаж, охин Ольгатайгаа тоглож, өдрийн хоол, оройн хоол идэхээр хэсэг хугацаанд завсарлав.
1869 оны 3-р сарын 1-ний орой тэрээр өөрийн зохиосон хүснэгтээ бүрмөсөн шинэчлэн бичиж, "Атомын жин ба химийн ижил төстэй байдал дээр суурилсан элементүүдийн системийн туршлага" нэрээр хэвлэх үйлдвэрт илгээж, бичгийн машинчдад тэмдэглэл хийжээ. "1869 оны 2-р сарын 17" гэсэн огноог тавьсан (энэ бол хуучин хэв маяг).
Үелэх хуулийг ингэж нээсэн бөгөөд орчин үеийн томъёолол нь дараах байдалтай байна: Энгийн бодисын шинж чанар, түүнчлэн элементийн нэгдлүүдийн хэлбэр, шинж чанар нь тэдгээрийн атомын цөмийн цэнэгээс үе үе хамааралтай байдаг.
Менделеев дотоод, гадаадын олон химичдэд элементүүдийн хүснэгт бүхий хэвлэмэл хуудсыг илгээж, үүний дараа л бяслагны үйлдвэрүүдийг шалгахаар Санкт-Петербургээс гарчээ.
Явахаасаа өмнө тэрээр органик химич, ирээдүйн химийн түүхч Н.А.Меншуткинд Оросын сэтгүүлд хэвлүүлэхээр "Элементүүдийн атомын жинтэй шинж чанаруудын хамаарал" өгүүллийн гар бичмэлийг хүлээлгэн өгчээ. химийн нийгэммөн удахгүй болох нийгэмлэгийн хурал дээр харилцах зорилгоор.
1869 оны 3-р сарын 18-нд тухайн үед компанийн бичиг хэргийн ажилтан байсан Меншуткин Менделеевийн нэрийн өмнөөс Үеийн хуулийн талаар товч илтгэл тавьжээ. Уг илтгэл эхэндээ химичүүдийн анхаарлыг төдийлөн татаагүй бөгөөд Оросын химийн нийгэмлэгийн ерөнхийлөгч, академич Николай Зинин (1812-1880) Менделеев жинхэнэ судлаач хүний хийх ёстой зүйлийг хийхгүй байна гэж мэдэгджээ. Хоёр жилийн дараа Дмитрий Ивановичийн "Элементүүдийн байгалийн систем ба зарим элементийн шинж чанарыг илэрхийлэхэд ашиглах нь" өгүүллийг уншсаны дараа Зинин бодлоо өөрчилж, Менделеевт бичсэн: "Маш, маш сайн, маш сайн холболтууд, бүр хөгжилтэй. унших, Бурхан танд амжилт хүсье V туршилтын баталгааТаны дүгнэлт. Н.Зинин, танд чин сэтгэлээсээ хандаж, таныг гүнээ хүндэтгэж байна." Менделеев бүх элементүүдийг атомын массын өсөлтийн дарааллаар байрлуулаагүй; зарим тохиолдолд химийн шинж чанаруудын ижил төстэй байдлыг илүү удирдан чиглүүлдэг. Тиймээс кобальт Ко илүү их байдаг. атомын масс нь никель Ni, теллур Те нь иод I-ээс их байдаг, гэхдээ Менделеев тэдгээрийг Co - Ni, Te - I гэсэн дарааллаар байрлуулсан бөгөөд эсрэгээр теллур нь галогенийн бүлэгт багтах болно иод нь селенийн Se-ийн хамаатан болно.
Эхнэр хүүхдүүддээ. Эсвэл үхэх гэж байгаагаа мэдэж байсан ч халуун дотноор хайрладаг гэр бүлээ урьдчилан үймүүлж, санаа зовохыг хүсээгүй юм болов уу." Өглөөний 5:20 цагт 1907 оны 1-р сарын 20-нд Дмитрий Иванович Менделеев таалал төгсөв. Түүнийг ээж, хүү Владимир нарын булшнаас холгүй орших Санкт-Петербург хотын Волковское оршуулгын газарт оршуулжээ. 1911 онд Оросын дэвшилтэт эрдэмтдийн санаачилгаар Д.И. Менделеев, хаана ...
Москвагийн метроны буудал, далай судлалын судалгааны хөлөг онгоц, 101-р химийн элемент, эрдэс - менделеевит. Орос хэлээр ярьдаг эрдэмтэд, хошигнолчид заримдаа: "Дмитрий Иванович Менделеев еврей хүн биш гэж үү, энэ бол маш хачирхалтай овог, "Мендель" овогоос гаралтай юм биш үү?" гэж асуудаг. Энэ асуултын хариулт маш энгийн: "Павел Максимович Соколовын дөрвөн хүү бүгд ...
Өвгөн Державин залуу Пушкиныг адисалсан лицей шалгалт. Тоолуурын дүрд органик химийн нэрт мэргэжилтэн, академич Ю.Ф.Фрицше тоглосон. Д.И.Менделеевийн нэр дэвшигчийн диссертаци 1855 онд Сурган хүмүүжүүлэх ерөнхий дээд сургуулийг төгссөн.Түүний "Изоморфизм нь кристалл хэлбэрийн бусад хамааралтай холбоотой" сэдэвт бүтээл нь түүний анхны томоохон шинжлэх ухааны...
Голчлон хялгасан судасны асуудал болон гадаргуугийн хурцадмал байдалшингэн зүйл хийж, чөлөөт цагаа Оросын залуу эрдэмтдийн тойрогт өнгөрөөсөн: С.П. Боткина, И.М. Сеченова, И.А. Вышнеградский, A.P. 1861 онд Менделеев Санкт-Петербургт буцаж ирээд, их сургуульд органик химийн чиглэлээр лекц уншихаа үргэлжлүүлж, "Органик хими" хэмээх сурах бичгийг хэвлүүлжээ.
Биднийг хүрээлэн буй байгальд байгаа бүх материал сансрын объектууд, энгийн дэлхийн объект буюу амьд организм, бодисуудаас бүрддэг. Тэдгээрийн олон сорт байдаг. Эрт дээр үед ч хүмүүс өөрсдийн бие махбодийн төлөв байдлыг өөрчлөх төдийгүй анхныхаасаа өөр шинж чанартай бусад бодис болгон хувиргах чадвартай болохыг анзаарсан. Гэвч хүмүүс материйн ийм хувирал ямар хууль тогтоомжийн дагуу явагддагийг шууд ойлгоогүй. Үүнийг хийхийн тулд тухайн бодисын үндсийг зөв тодорхойлж, байгальд байгаа элементүүдийг ангилах шаардлагатай байв. Энэ нь зөвхөн онд боломжтой болсон 19-р сарын дунд үеүечилсэн хуулийг нээсэн зуун. Үүнийг бий болгосон түүх D.I. Менделеевийн өмнө олон жил ажилласан бөгөөд энэ төрлийн мэдлэгийг бий болгоход бүх хүн төрөлхтний олон зуун жилийн туршлага тусалсан.
Химийн шинжлэх ухааны үндэс хэзээ тавигдсан бэ?
Эртний гар урчууд төрөл бүрийн металл цутгах, хайлуулах ажилд нэлээд амжилттай байсан бөгөөд тэдгээрийн хувирлын олон нууцыг мэддэг байв. Тэд өөрсдийн мэдлэг, туршлагаа үр хойчдоо өвлүүлэн үлдээж, дундад зууныг хүртэл хэрэглэж ирсэн. Үндсэн металлыг үнэ цэнэтэй болгон хувиргах бүрэн боломжтой гэж үздэг байсан бөгөөд энэ нь 16-р зууныг хүртэл химичүүдийн гол ажил байсан юм. Үндсэндээ ийм санаа нь эртний Грекийн эрдэмтдийн философи, ид шидийн санааг агуулж байсан бөгөөд бүх бодис бие биедээ хувирч болох тодорхой "анхдагч элементүүд" -ээс бүрддэг. Энэхүү хандлага нь илт энгийн байсан ч энэ нь Үеийн хуулийг нээсэн түүхэнд чухал үүрэг гүйцэтгэсэн.

Панацея ба цагаан хандмал
Үндсэн зарчмыг хайж байхдаа алхимичид хоёр гайхалтай бодис байдаг гэдэгт бат итгэдэг байв. Тэдгээрийн нэг нь домогт философийн чулуу байсан бөгөөд үүнийг амьдралын үрэл буюу өвчин эмгэг гэж нэрлэдэг. Ийм эмчилгээ нь мөнгөн ус, хар тугалга, мөнгө болон бусад бодисыг алт болгон хувиргах аюулгүй арга төдийгүй хүний аливаа өвчнийг эдгээдэг гайхамшигт бүх нийтийн эм болж үйлчилдэг гэж үздэг байв. Цагаан хандмал гэж нэрлэгддэг өөр нэг элемент нь тийм ч үр дүнтэй биш байсан ч бусад бодисыг мөнгө болгон хувиргах чадвартай байв.
Тогтмол хуулийг нээсэн үндэслэлийг хэлэхэд алхимичдын хуримтлуулсан мэдлэгийг дурдахгүй байхын аргагүй юм. Тэд бэлгэдлийн сэтгэлгээний жишээг дүрсэлсэн. Энэхүү хагас ид шидийн шинжлэх ухааны төлөөлөгчид тодорхой зүйлийг бий болгосон химийн загварертөнц ба түүнд тохиолдож буй үйл явц нь сансрын түвшинд. Тэд бүх зүйлийн мөн чанарыг ойлгохыг хичээж, лабораторийн арга техник, тоног төхөөрөмж, химийн шилэн савны талаарх мэдээллийг маш нарийн нягт нямбай бүртгэж, хамт олон, үр хойчдоо өөрийн туршлагаа өвлүүлэн үлдээхдээ маш нягт нямбай, хичээнгүйлэн ажиллажээ.

Ангилах хэрэгцээ
Маш олон төрлийн химийн элементүүдийн талаархи ихээхэн хэмжээний мэдээлэл 19-р зуунЭнэ нь эрдэмтдийн байгалийн хэрэгцээ, тэдгээрийг системчлэх хүслийг бий болгосон нь хангалттай хуримтлагдсан байв. Гэхдээ ийм ангиллыг хийхийн тулд нэмэлт туршилтын өгөгдөл шаардлагатай байсан бөгөөд ид шидийн биш, харин бодисын бүтэц, хараахан болоогүй байгаа материйн бүтцийн суурийн мөн чанарын талаархи бодит мэдлэг шаардлагатай байв. Нэмж дурдахад, тухайн үед мэдэгдэж байсан химийн элементүүдийн атомын массын утгын талаархи мэдээлэл нь тийм ч үнэн зөв биш байсан.
Гэвч байгалийн эрдэмтдийн дунд ангилах оролдлого нь юмсын жинхэнэ мөн чанарыг ойлгохоос өмнө олон удаа хийгдсэн бөгөөд энэ нь одоо үндэс суурь болж байна. орчин үеийн шинжлэх ухаан. Мөн энэ чиглэлээр олон эрдэмтэд ажилласан. Менделеевийн үечилсэн хуулийг нээх урьдчилсан нөхцөлийг товч тайлбарлахдаа элементүүдийн ийм хослолын жишээг дурдах нь зүйтэй.
Гурвалсан
Тухайн үеийн эрдэмтэд олон төрлийн бодисуудын шинж чанар нь тэдний атомын массын хэмжээнээс хамаардаг гэж үздэг байв. Үүнийг ойлгосон Германы химич Иоганн Дёберейнер материйн үндэс болсон элементүүдийг ангилах өөрийн гэсэн системийг санал болгов. Энэ нь 1829 онд болсон. Энэхүү үйл явдал нь тухайн үеийн шинжлэх ухаанд нэлээд ноцтой ахиц дэвшил, мөн үечилсэн хуулийг нээсэн түүхэн дэх чухал үе шат байв. Доберейнер мэдэгдэж буй элементүүдийг нийгэмд нэгтгэж, тэдэнд "гурвалсан" гэсэн нэр өгсөн. Одоо байгаа системийн дагуу гаднах элементүүдийн масс нь тэдгээрийн хоорондох бүлгийн гишүүний атомын массын нийлбэрийн дундажтай тэнцүү байв.

Гурвалын хил хязгаарыг тэлэх оролдлого
Дурдсан Döbereiner системд хангалттай дутагдал байсан. Жишээлбэл, бари, стронци, кальцийн гинжин хэлхээнд бүтэц, шинж чанараараа ижил төстэй магни байгаагүй. Теллур, селен, хүхрийн нийгэмлэгт хүчилтөрөгч хангалтгүй байв. Бусад ижил төстэй бодисуудыг гурвалсан системийн дагуу ангилах боломжгүй байв.
Бусад олон химич эдгээр санааг хөгжүүлэхийг оролдсон. Ялангуяа Германы эрдэмтэн Леопольд Гмелин "хатуу" хүрээг өргөжүүлж, ангилсан элементүүдийн бүлгийг өргөжүүлж, элементүүдийн эквивалент жин ба цахилгаан сөрөг байдлын дарааллаар хуваарилахыг эрэлхийлэв. Түүний бүтэц нь зөвхөн гурвалсан төдийгүй тетрад, пентад үүсгэдэг байсан ч Германы химич үечилсэн хуулийн мөн чанарыг хэзээ ч ойлгож чадаагүй юм.
Спираль де Шанкуртуа
Бүр илүү нарийн төвөгтэй хэлхээЭлементүүдийн бүтцийг Александр де Шанкуртуа зохион бүтээсэн. Тэрээр тэдгээрийг цилиндрт эргэлдсэн хавтгай дээр байрлуулж, атомын массыг нэмэгдүүлэх дарааллаар 45 ° налуу босоо байдлаар байрлуулав. Хүлээгдэж буйгаар өгөгдсөн эзэлхүүний тэнхлэгтэй параллель шугамын дагуу геометрийн дүрс, ижил төстэй шинж чанартай бодисыг байрлуулах ёстой.

Гэвч бодит байдал дээр заримдаа огт хамааралгүй элементүүд нэг босоо чиглэлд унадаг тул хамгийн тохиромжтой ангилал бүтсэнгүй. Жишээлбэл, шүлтлэг металлын хажууд манган нь тэс өөр химийн шинж чанартай болсон. Мөн ижил "компани" нь хүхэр, хүчилтөрөгч, титан элементийг багтаасан бөгөөд энэ нь тэдэнтэй огт адилгүй байв. Гэсэн хэдий ч үүнтэй төстэй схем нь үечилсэн хуулийг нээсэн түүхэнд байр сууриа эзэлж, хувь нэмрээ оруулсан юм.
Ангилал үүсгэх бусад оролдлого
Тайлбарласан зүйлсийн дараа Жон Ньюландс өөрийн ангиллын системийг санал болгож, үүссэн цувралын найм дахь гишүүн бүр атомын массын өсөлттэй уялдуулан байрлуулсан элементүүдийн шинж чанарт ижил төстэй байдгийг тэмдэглэв. Илэрсэн хэв маягийг хөгжмийн октавын зохион байгуулалтын бүтэцтэй харьцуулах нь эрдэмтний санаанд оров. Үүний зэрэгцээ тэрээр элемент тус бүрт өөрийн серийн дугаарыг өгч, тэдгээрийг хэвтээ эгнээнд байрлуулав. Гэхдээ ийм схем дахин тохиромжгүй болж, шинжлэх ухааны хүрээлэлд маш эргэлзээтэй үнэлэгдсэн.

1964-1970 он хүртэл Химийн элементүүдийг зохион байгуулах хүснэгтийг мөн Одлинг, Мейер нар бүтээжээ. Гэхдээ ийм оролдлого дахин сул талуудтай байв. Энэ бүхэн Менделеев үечилсэн хуулийг нээхийн өмнөхөн болсон. Ангилах төгс бус оролдлого бүхий зарим бүтээлүүд бидний өнөөг хүртэл ашигладаг хүснэгтийг дэлхий нийтэд танилцуулсны дараа ч хэвлэгджээ.
Менделеевийн намтар
Оросын гайхамшигт эрдэмтэн 1834 онд Тобольск хотод гимназийн захирлын гэр бүлд төржээ. Түүнээс гадна гэрт арван зургаан ах эгч байсан. Хүүхдүүдийн хамгийн бага нь байсан Дмитрий Иванович бага наснаасаа л бусдын анхаарлыг татсангүй. Эцэг эх нь хэцүү байсан ч түүнд хамгийн сайн сайхныг өгөхийг хичээсэн илүү сайн боловсрол. Ийнхүү Менделеев эхлээд Тобольск хотод гимнастик, дараа нь нийслэлд сурган хүмүүжүүлэх дээд сургуулийг төгсөж, шинжлэх ухааныг гүн гүнзгий сонирхдог байв. Зөвхөн хими төдийгүй физик, цаг уур, геологи, технологи, багаж хэрэгсэл, нисэх онгоц гэх мэт.
Удалгүй Менделеев эрдмийн зэрэг хамгаалж, Санкт-Петербургийн их сургуульд дэд профессор болж, органик химийн сэдвээр лекц уншив. 1865 онд тэрээр "Архи, устай хослуулах тухай" сэдвээр хамтран ажиллагсаддаа докторын зэрэг хамгаалсан. Тогтмол хуулийг нээсэн жил нь 1969. Гэвч энэ амжилтын өмнө 14 жилийн шаргуу хөдөлмөр бий.

Агуу нээлтийн тухай
Алдаа, алдаа, түүнчлэн хамтран ажиллагсдынхаа эерэг туршлагыг харгалзан Дмитрий Иванович химийн элементүүдийг хамгийн тохиромжтой аргаар системчилж чадсан. Тэрээр мөн Менделеевийн үечилсэн хуулийн томъёололд дурдсан нэгдлүүд ба энгийн бодисын шинж чанар, тэдгээрийн хэлбэр нь атомын массын утгаас үечилсэн хамаарлыг анзаарсан.
Гэвч харамсалтай нь ийм дэвшилтэт санаанууд Оросын эрдэмтдийн зүрх сэтгэлд тэр даруй хариулт олж чадаагүй бөгөөд энэ шинэлэг санааг маш болгоомжтой хүлээж авсан. Гадаадын шинжлэх ухааны зүтгэлтнүүдийн дунд, ялангуяа Англи, Германд Менделеевийн хууль хамгийн хатуу эсэргүүцэгчдийг олжээ. Гэвч тун удалгүй байдал өөрчлөгдсөн. Шалтгаан нь юу байсан бэ? Оросын агуу эрдэмтний гайхалтай зориг нь хэсэг хугацааны дараа түүний шинжлэх ухааны алсын хараатай гайхалтай чадварын нотолгоо болж дэлхийд гарч ирэв.

Химийн шинэ элементүүд
Түүний бүтээсэн үелэх хууль, үелэх системийн бүтцийг нээсэн нь бодисыг системчлэхээс гадна тухайн үед үл мэдэгдэх олон элемент байгалын талаар хэд хэдэн таамаглал дэвшүүлэх боломжийг олгосон юм. Тийм ч учраас Менделеев өөрөөсөө өмнө бусад эрдэмтдийн хийж чадаагүй зүйлийг амьдралд хэрэгжүүлж чадсан юм.
Зөвхөн таван жил өнгөрч, таамаглал батлагдаж эхлэв. Францын иргэн Лекок де Бойсбодран шинэ металл нээж, түүнийг галли гэж нэрлэжээ. Түүний шинж чанар нь онолын хувьд Менделеевийн таамагласан эка-хөнгөн цагаантай маш төстэй байв. Энэ тухай мэдээд тэр үеийн шинжлэх ухааны ертөнцийн төлөөлөгчид гайхаж байв. Гэхдээ л болоо гайхалтай баримтуудогт дуусаагүй байна. Дараа нь Швед Нилссон скандиумыг нээсэн бөгөөд түүний аналог нь экабор болжээ. Мөн эка-цахиурын ихэр нь Винклерийн нээсэн германи байв. Түүнээс хойш Менделеевийн хууль үйлчилж, улам олон шинэ дэмжигчидтэй болж эхэлсэн.
Гайхалтай алсын хараатай шинэ баримтууд
Бүтээгч өөрийн санааны гоо үзэсгэлэнд маш их автсан тул тэрээр зарим таамаглал дэвшүүлэх үүрэг хүлээсэн бөгөөд үүний баталгаа нь хожим практик туршлагаар хамгийн гайхалтай батлагдсан юм. шинжлэх ухааны нээлтүүд. Жишээлбэл, Менделеев хүснэгтэд байгаа зарим бодисыг атомын массын өсөлттэй уялдуулаагүй байна. Тэрээр илүү гүнзгий утгаараа үечлэл нь зөвхөн элементүүдийн атомын жин нэмэгдэхтэй холбоотой төдийгүй өөр шалтгаанаар ажиглагдаж байгааг урьдчилан таамаглаж байв. Элементийн масс нь түүний бүтэц дэх зарим энгийн бөөмсийн хэмжээнээс хамаардаг гэж агуу эрдэмтэн таамаглаж байсан.
Ийнхүү үечилсэн хууль ямар нэгэн байдлаар шинжлэх ухааны төлөөлөгчдийг атомын бүрэлдэхүүн хэсгүүдийн талаар бодоход хүргэв. Удахгүй болох 20-р зууны эрдэмтэд - агуу нээлтүүдийн зуун нь элементүүдийн шинж чанар нь цэнэгийн хэмжээнээс хамаардаг гэдэгт олон удаа итгэлтэй байсан. атомын цөмболон түүний электрон бүрхүүлийн бүтэц.

Тогтмол хууль ба орчин үеийн байдал
Үелэх систем нь үндсэндээ өөрчлөгдөөгүй хэвээр байсан ч дараа нь олон удаа нэмэлт, өөрчлөлт оруулсан. Энэ нь инертийн хий агуулсан тэг бүлэг элементийг үүсгэсэн. Газрын ховор элементийн байршлын асуудал ч амжилттай шийдэгдсэн. Гэхдээ нэмэлтүүдийг үл харгалзан Менделеевийн үечилсэн хуулийг нээсний ач холбогдол анхны хувилбархэт үнэлэхэд нэлээд хэцүү байдаг.
Хожим нь цацраг идэвхт байдлын үзэгдлийн тусламжтайгаар ийм системчлэлийн амжилтын шалтгаан, түүнчлэн элементүүдийн шинж чанарын үечилсэн байдлыг бүрэн ойлгосон. янз бүрийн бодисууд. Удалгүй цацраг идэвхт элементүүдийн изотопууд энэ хүснэгтэд байр сууриа олсон. Олон тооны эсийн гишүүдийг ангилах үндэс нь атомын дугаар байв. Мөн 20-р зууны дунд үед цөмийн эргэн тойронд асар хурдтай хөдөлж буй электронуудын тойрог замд атомын тойрог замыг дүүргэхээс хамаарч хүснэгтэд элементүүдийн дарааллыг зөвтгөв.
Роберт Бойл 1668 онд хийсэн бүтээлдээ задрах боломжгүй химийн элементүүдийн жагсаалтыг гаргажээ. Тэр үед тэд ердөө арван тавтай байсан. Үүний зэрэгцээ эрдэмтэн түүний жагсаасан элементүүдээс бусад элементүүд байхгүй болсон гэж мэдэгдээгүй бөгөөд тэдгээрийн тоо хэмжээний тухай асуудал нээлттэй хэвээр байна.
Зуун жилийн дараа Францын химич Антуан Лавуазье эмхэтгэсэн шинэ жагсаалт-аас шинжлэх ухаанд мэдэгддэгэлементүүд. Түүний бүртгэлд 35 хүн орсон байна химийн бодис, үүний 23 нь дараа нь тэдгээр нь маш задрах боломжгүй элементүүд гэж хүлээн зөвшөөрөгдсөн.
Шинэ элементүүдийн эрэл хайгуулыг дэлхийн химич нар хийж, нэлээд амжилттай ахисан. Оросын химич Дмитрий Иванович Менделеев энэ асуудалд шийдвэрлэх үүрэг гүйцэтгэсэн: элементүүдийн атомын масс ба тэдгээрийн "шатлал" дахь байр хоорондын хамаарлын талаархи санааг тэр гаргасан. Түүний хэлснээр "бид элементүүдийн бие даасан шинж чанар ба тэдгээрийн атомын жингийн хоорондын уялдаа холбоог хайх ёстой."
Тухайн үед мэдэгдэж байсан химийн элементүүдийг харьцуулж, Менделеев асар их ажил хийснийхээ дараа эцэст нь хамаарал, бие даасан элементүүдийн хоорондох байгалийн ерөнхий холбоо, тэдгээр нь нэгдмэл байдлаар харагддаг, элемент тус бүрийн шинж чанар нь дангаараа байдаг зүйл биш гэдгийг олж мэдэв. , гэхдээ үе үе, тогтмол давтагдах үзэгдэл.
Тиймээс 1869 оны 2-р сард үүнийг томъёолсон Менделеевийн үечилсэн хууль. Мөн оны гуравдугаар сарын 6-нд Д.И. Менделеев "Элементүүдийн атомын жинтэй шинж чанаруудын хамаарал" гэсэн гарчигтай Н.А. Меншуткин Оросын химийн нийгэмлэгийн хурал дээр.
Мөн онд уг нийтлэл Германы "Zeitschrift für Chemie" сэтгүүлд, 1871 онд "Annalen der Chemie" сэтгүүлд Д.И. Менделеев өөрийн нээлтэд зориулагдсан - "Die periodische Gesetzmässigkeit der Elemente" (Химийн элементүүдийн үечилсэн загвар).
Тогтмол хүснэгт үүсгэх
Энэ санааг Менделеев нэлээд эрт бий болгосон ч гэсэн богино хугацаа, тэр дүгнэлтээ удаан хугацаанд боловсруулж чадаагүй. Түүний хувьд санаагаа тодорхой ерөнхий, хатуу, харааны систем хэлбэрээр илэрхийлэх нь чухал байв. Нэгэн удаа Д.И. Менделеев профессор А.А. Иностранцев: "Миний толгойд бүх зүйл цугларсан, гэхдээ би үүнийг хүснэгтээр илэрхийлж чадахгүй."
Намтар судлаачдын хэлснээр, энэ ярианы дараа эрдэмтэн гурван өдөр, гурван шөнө унтахгүйгээр ширээ бүтээхээр ажилласан. Тэрээр элементүүдийг нэгтгэн хүснэгт болгон зохион байгуулж болох янз бүрийн хувилбаруудыг судалж үзсэн. Үелэх систем бий болох үед бүх химийн элементүүд шинжлэх ухаанд мэдэгдээгүй байсан тул ажил нь бас төвөгтэй байв.
1869-1871 онд Менделеев шинжлэх ухааны нийгэмлэгийн дэвшүүлж, хүлээн зөвшөөрөгдсөн үечилсэн үзэл санааг үргэлжлүүлэн хөгжүүлэв. Үүний нэг алхам бол үелэх систем дэх элементийн байршлын тухай ойлголтыг бусад элементүүдийн шинж чанаруудтай харьцуулахад түүний шинж чанарын багц болгон нэвтрүүлэх явдал байв.
Энэ үндсэн дээр шил үүсгэгч ислийн өөрчлөлтийн дарааллыг судлах явцад олж авсан үр дүнд тулгуурлан Менделеев бериллий, индий, уран, зэрэг 9 элементийн атомын массын утгыг зассан. бусад.
D.I-ийн ажлын үеэр. Менделеев эмхэтгэсэн хүснэгтийнхээ хоосон нүдийг бөглөхийг эрэлхийлэв. Үүний үр дүнд 1870 онд тэрээр тухайн үед шинжлэх ухаанд үл мэдэгдэх элементүүдийг нээхийг зөгнөжээ. Менделеев атомын массыг тооцоолж, тэр үед хараахан нээгдээгүй гурван элементийн шинж чанарыг тодорхойлсон.
- "ekaaluminium" - 1875 онд нээсэн, галли гэж нэрлэгдсэн,
- "Экабора" - 1879 онд нээгдсэн, скандиум гэж нэрлэгдсэн,
- "exasilicon" - 1885 онд нээсэн, германий нэртэй.
Түүний хийсэн дараагийн таамаглал нь полони (1898 онд нээсэн), астатин (1942-1943 онд нээсэн), технециум (1937 онд нээсэн), рений (1925 онд нээсэн), Франц (1939 онд нээсэн) зэрэг өөр найман элементийг нээсэн явдал байв. .
1900 онд Дмитрий Иванович Менделеев, Уильям Рамсай нар үелэх системд тусгай, тэг бүлгийн элементүүдийг оруулах шаардлагатай гэсэн дүгнэлтэд хүрчээ. Өнөөдөр эдгээр элементүүдийг үнэт хий гэж нэрлэдэг (1962 оноос өмнө эдгээр хийг үнэт хий гэж нэрлэдэг байсан).

Тогтмол хүснэгтийг зохион байгуулах зарчим
Түүний хүснэгтэд D.I. Менделеев химийн элементүүдийг массын өсөлтийн дарааллаар эгнээнд байрлуулж, эгнээний уртыг сонгож, нэг баганын химийн элементүүд ижил төстэй химийн шинж чанартай байв.
Гели, неон, аргон, криптон, ксенон, радон зэрэг үнэт хий нь бусад элементүүдтэй урвалд орох дургүй бөгөөд химийн идэвхжил багатай тул баруун талын баганад байдаг.
Үүний эсрэгээр, хамгийн зүүн баганын элементүүд - литий, натри, кали болон бусад бодисууд нь бусад бодисуудтай хүчтэй урвалд ордог тул үйл явц нь тэсрэх аюултай байдаг. Хүснэгтийн бусад багана дахь элементүүд ижил төстэй байдлаар ажилладаг - баганын дотор эдгээр шинж чанарууд нь ижил төстэй боловч нэг баганаас нөгөөд шилжих үед өөр өөр байдаг.
Тогтмол хүснэгт нь анхны хувилбартаа байгальд одоо байгаа нөхцөл байдлыг тусгадаг. Эхлээд хүснэгтэд яагаад ийм байх ёстойг ямар ч байдлаар тайлбарлаагүй болно. Зөвхөн квант механик бий болсноор л элементүүдийн зохион байгуулалтын жинхэнэ утгыг олж мэдэв үечилсэн хүснэгт.
Уран хүртэлх химийн элементүүд (92 протон, 92 электрон агуулдаг) байгальд байдаг. 93-аас эхлэн лабораторийн нөхцөлд хиймэл элементүүд бий болсон.
Битгий алд.Бүртгүүлж, нийтлэлийн холбоосыг имэйлээр хүлээн авна уу.
Заавал судлах хичээлүүдийн нэг нь химийн хичээл байсныг сургуульд явсан хэн бүхэн санаж байгаа байх. Чи түүнд таалагдаж магадгүй, эсвэл танд таалагдахгүй байж магадгүй - энэ нь хамаагүй. Мөн энэ чиглэлээр олон мэдлэг аль хэдийн мартагдсан бөгөөд амьдралд хэрэглэгдэхгүй байх магадлалтай. Гэсэн хэдий ч хүн бүр Д.И.Менделеевийн химийн элементүүдийн хүснэгтийг санаж байгаа байх. Олон хүмүүсийн хувьд энэ нь олон өнгийн хүснэгт хэвээр үлдсэн бөгөөд дөрвөлжин бүрт тодорхой үсэг бичигдсэн бөгөөд химийн элементүүдийн нэрийг зааж өгдөг. Гэхдээ энд бид химийн талаар ярихгүй бөгөөд хэдэн зуун зүйлийг тайлбарлах болно химийн урвалболон үйл явц, гэхдээ бид үечилсэн хүснэгт хэрхэн үүссэнийг танд хэлэх болно - энэ түүх нь ямар ч хүнд, тэр дундаа сонирхолтой, хэрэгцээтэй мэдээллээр өлсөж буй бүх хүмүүст сонирхолтой байх болно.
Бага зэрэг дэвсгэр
Эрт 1668 онд Ирландын нэрт химич, физикч, теологич Роберт Бойл алхимийн тухай олон домгийг няцааж, задрах боломжгүй химийн элементүүдийг хайх хэрэгцээний талаар ярилцсан ном хэвлүүлжээ. Эрдэмтэн зөвхөн 15 элементээс бүрдсэн жагсаалтыг гаргаж өгсөн боловч илүү олон элемент байж магадгүй гэсэн санааг хүлээн зөвшөөрсөн. Энэ нь зөвхөн шинэ элементүүдийг хайх төдийгүй тэдгээрийг системчлэх эхлэл болсон юм.
Зуун жилийн дараа Францын химич Антуан Лавуазье 35 элементийг багтаасан шинэ жагсаалтыг гаргажээ. Тэдний 23 нь задрах боломжгүй болох нь тогтоогдсон. Гэвч шинэ элементүүдийн эрэл хайгуулыг дэлхий даяар эрдэмтэд үргэлжлүүлэв. БА гол үүрэгЭнэ үйл явцад Оросын нэрт химич Дмитрий Иванович Менделеев чухал үүрэг гүйцэтгэсэн бөгөөд тэрээр элементүүдийн атомын масс ба тэдгээрийн систем дэх байршил хоёрын хооронд хамаарал байж болно гэсэн таамаглалыг анх дэвшүүлсэн юм.
Химийн элементүүдийг хооронд нь харьцуулж, шаргуу хөдөлмөрлөсний ачаар Менделеев элементүүдийн хоорондын холбоог олж мэдсэн бөгөөд тэдгээр нь нэг байж болох бөгөөд тэдгээрийн шинж чанар нь энгийн зүйл биш, харин үе үе давтагдах үзэгдлийг илэрхийлдэг. Үүний үр дүнд 1869 оны 2-р сард Менделеев анхны үечилсэн хуулийг боловсруулж, 3-р сард химийн түүхч Н.А.Меншуткин Оросын Химийн Нийгэмлэгт "Элементүүдийн атомын жинтэй шинж чанаруудын хамаарал" илтгэлийг танилцуулав. Дараа нь тэр жил Германы "Zeitschrift fur Chemie" сэтгүүлд Менделеевийн бүтээл хэвлэгдсэн бол 1871 онд Германы өөр нэг "Annalen der Chemie" сэтгүүлд эрдэмтний нээлтэд зориулсан шинэ өргөн хүрээтэй нийтлэл хэвлэгджээ.
Тогтмол хүснэгт үүсгэх

1869 он гэхэд үндсэн санааг Менделеев аль хэдийн бий болгосон бөгөөд нэлээд богино хугацаанд тэрээр үүнийг юу болохыг тодорхой харуулах ямар ч эмх цэгцтэй тогтолцоонд оруулж чадаагүй юм. Хамтран ажиллагсад А.А.Иностранцевтэй ярилцахдаа тэр бүх зүйл толгойд нь бэлэн байсан ч бүгдийг нь ширээн дээр тавьж чадаагүй гэж хэлсэн. Үүний дараа Менделеевийн намтар судлаачдын хэлснээр тэрээр ширээн дээрээ шаргуу ажиллаж эхэлсэн бөгөөд энэ нь гурван өдөр унтаагүй байв. Тэд элементүүдийг хүснэгт болгон зохион байгуулах янз бүрийн аргыг туршиж үзсэн бөгөөд тэр үед шинжлэх ухаан бүх химийн элементүүдийн талаар хараахан мэдээгүй байсан тул ажил нь бас төвөгтэй байв. Гэсэн хэдий ч хүснэгтийг үүсгэсэн хэвээр байгаа бөгөөд элементүүдийг системчилсэн байв.
Менделеевийн мөрөөдлийн домог
Д.И.Менделеев өөрийн ширээний тухай мөрөөдөж байсан түүхийг олон хүн сонссон. Энэ хувилбарыг дээр дурдсан Менделеевийн хамтрагч А.А.Иностранцев шавь нараа хөгжөөж байсан хөгжилтэй түүх болгон идэвхтэй тараасан. Тэрээр Дмитрий Иванович орондоо ороод зүүдэндээ бүх химийн элементүүдийг зөв дарааллаар байрлуулсан ширээгээ тодорхой харсан гэж хэлэв. Үүний дараа оюутнууд 40°-ийн архи ч мөн адил олдсон гэж хошигнож байсан. Гэхдээ нойрны тухай түүхийн бодит урьдчилсан нөхцөл байсаар байсан: аль хэдийн дурьдсанчлан Менделеев нойргүй, амралтгүй ширээн дээр ажилладаг байсан бөгөөд Иностранцев түүнийг ядарч туйлдсан байхыг олж мэдэв. Өдрийн цагаар Менделеев бага зэрэг амрахаар шийдэж, хэсэг хугацааны дараа гэнэт сэрж, тэр даруй цаас авч, дээр нь бэлэн ширээ зурав. Гэвч эрдэмтэн өөрөө энэ түүхийг бүхэлд нь зүүдэндээ няцааж: "Би энэ тухай хорин жилийн турш бодож байсан, та нар: Би сууж байгаад гэнэт ... бэлэн болсон гэж бодож байна." Тиймээс зүүдний домог нь маш сэтгэл татам байж болох ч ширээ бүтээх нь зөвхөн шаргуу хөдөлмөрөөр л боломжтой байв.

Цаашдын ажил
1869-1871 оны хооронд Менделеев шинжлэх ухааны нийгэмлэгийн хандлагатай байсан үечилсэн байдлын санааг боловсруулсан. Энэ үйл явцын нэг чухал үе шат бол бусад элементүүдийн шинж чанаруудтай харьцуулахад түүний шинж чанаруудын нийлбэр дээр үндэслэн системийн аливаа элемент байх ёстойг ойлгох явдал байв. Үүний үндсэн дээр, мөн шил үүсгэдэг оксидын өөрчлөлтийн талаархи судалгааны үр дүнд тулгуурлан химич уран, индий, берилли болон бусад элементүүдийн атомын массын утгыг залруулж чадсан.
Мэдээжийн хэрэг, Менделеев хүснэгтэд үлдсэн хоосон нүднүүдийг аль болох хурдан дүүргэхийг хүссэн бөгөөд 1870 онд удахгүй нээгдэнэ гэж таамаглаж байсан. шинжлэх ухаанд үл мэдэгдэххимийн элементүүд, атомын масс, шинж чанарууд нь түүний тооцоолж чадсан. Эдгээрийн эхнийх нь галли (1875 онд нээсэн), скандий (1879 онд нээсэн) болон германий (1885 онд нээсэн) юм. Дараа нь таамаглал биелсээр байгаа бөгөөд полони (1898), рений (1925), технециум (1937), франций (1939), астатин (1942-1943) зэрэг өөр найман шинэ элемент нээгдэв. Дашрамд дурдахад, 1900 онд Д.И.Менделеев, Шотландын химич Уильям Рамсай нар хүснэгтэд тэг бүлгийн элементүүдийг оруулах ёстой гэсэн дүгнэлтэд хүрсэн - 1962 он хүртэл тэдгээрийг инертийн хий гэж нэрлэдэг байсан.
Тогтмол хүснэгтийн зохион байгуулалт
Д.И.Менделеевийн хүснэгтэд байгаа химийн элементүүдийг массын өсөлтийн дагуу эгнээнд байрлуулж, тэдгээрийн элементүүд ижил төстэй шинж чанартай байхаар эгнээний уртыг сонгосон. Жишээлбэл, радон, ксенон, криптон, аргон, неон, гелий зэрэг үнэт хий нь бусад элементүүдтэй урвалд ороход хэцүү бөгөөд химийн урвал багатай байдаг тул баруун талын баганад байрладаг. Мөн зүүн баганын элементүүд (кали, натри, лити гэх мэт) бусад элементүүдтэй сайн урвалд ордог бөгөөд урвалууд нь өөрөө тэсрэх шинж чанартай байдаг. Энгийнээр хэлэхэд, багана бүрийн дотор элементүүд нь нэг баганаас нөгөө баганад өөр өөр шинж чанартай байдаг. 92-р тоо хүртэлх бүх элементүүд байгальд байдаг бөгөөд 93-аас хиймэл элементүүд эхэлдэг бөгөөд үүнийг зөвхөн лабораторийн нөхцөлд л үүсгэж болно.
Анхны хувилбартаа үечилсэн системийг зөвхөн байгальд байдаг дарааллын тусгал гэж ойлгодог байсан бөгөөд яагаад бүх зүйл ийм байх ёстой талаар ямар ч тайлбар байгаагүй. Квант механик гарч ирэхэд л хүснэгт дэх элементүүдийн дарааллын жинхэнэ утга тодорхой болсон.
Бүтээлч үйл явц дахь хичээлүүд
Д.И.Менделеевийн үелэх систем бий болсон бүх түүхээс бүтээлч үйл явцын ямар сургамж авч болох талаар ярихад бид энэ чиглэлээр англи судлаачийн санааг жишээ болгон дурдаж болно. бүтээлч сэтгэлгээГрэм Уоллес, Францын эрдэмтэн Анри Пуанкаре нар. Тэднийг товчхон өгье.
Пуанкаре (1908), Грэм Уоллес (1926) нарын судалгаагаар бүтээлч сэтгэлгээний дөрвөн үндсэн үе шат байдаг.
- Бэлтгэл- үндсэн асуудлыг боловсруулах үе шат, түүнийг шийдвэрлэх анхны оролдлого;
- Инкубаци- үйл явцаас түр зуур сатаарах үе шат, гэхдээ асуудлын шийдлийг олох ажил нь далд ухамсрын түвшинд явагддаг;
- Зөн билэг– зөн совингийн шийдэл байрлах үе шат. Түүнээс гадна, энэ шийдлийг асуудалтай огт холбоогүй нөхцөл байдалд олж болно;
- Шалгалт- шийдлийг турших, хэрэгжүүлэх үе шат, энэ шийдлийг туршиж үзэх, цаашдын хөгжүүлэлт.
Бидний харж байгаагаар, Менделеев өөрийн хүснэгтийг бүтээх явцад эдгээр дөрвөн үе шатыг яг нарийн дагасан. Энэ нь хэр үр дүнтэй болохыг үр дүнгээр нь дүгнэж болно, i.e. Хүснэгтийг бий болгосноор. Үүнийг бий болгосноор зөвхөн химийн шинжлэх ухаан төдийгүй бүх хүн төрөлхтний хувьд асар том дэвшил болсон тул дээрх дөрвөн үе шатыг жижиг төслүүдийг хэрэгжүүлэх, дэлхийн төлөвлөгөөг хэрэгжүүлэхэд ашиглаж болно. Санаж байх ёстой гол зүйл бол зүүдэндээ харахыг хичнээн их хүсч, хичнээн их унтсан ч гэсэн ганц ч нээлт, асуудлыг шийдэх ганц шийдэл байхгүй. Аливаа зүйлийг амжилттай болгохын тулд химийн элементүүдийн хүснэгт үүсгэх эсвэл маркетингийн шинэ төлөвлөгөө боловсруулах эсэх нь хамаагүй, та тодорхой мэдлэг, ур чадвар эзэмшсэн байхаас гадна боломжоо чадварлаг ашиглаж, шаргуу ажиллах хэрэгтэй.
Та бүхний ажил үйлсэд амжилт, төлөвлөгөөгөө амжилттай хэрэгжүүлэхийг хүсэн ерөөе!
ОХУ-ын Боловсрол, шинжлэх ухааны яам
Тверийн захиргааны боловсролын хэлтэс
Хотын боловсролын байгууллага
"Орой (ээлж) дунд сургууль№2" Тверь
"Кругозор" оюутны эссэ бичлэгийн уралдаан
Сэдвийн хураангуй:
Дмитрий Иванович Менделеевийн үечилсэн хууль ба химийн элементүүдийн үечилсэн системийг нээсэн түүх
Тверь хотын 2-р VSOSH хотын боловсролын байгууллагын 8-р бүлгийн оюутан
Удирдагч:
дээд зэрэглэлийн химийн багш
Хотын боловсролын байгууллага VSOSH №2, Тверь
Оршил………………………………………………… ...................... ...................................3
1. Үеийн хуулийг нээн илрүүлэх урьдчилсан нөхцөл……..4
1.1. Ангилал……………………………………………………..4
1.2. Доберейнерийн гурвал ба элементүүдийн анхны системүүд…………………….4
1.3. Спираль де Шанкуртуа………………………………………………………..5
1.5.Одлинг ба Мейерийн хүснэгт…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….
2. Тогтмол хуулийн нээлт……………………9
Дүгнэлт………………………………………………………………. 16
Ашигласан материал…………………………………………………….17
Танилцуулга
Химийн элементүүдийн үелэх хууль ба үелэх систем нь орчин үеийн химийн үндэс суурь юм.
Менделеев хот, үйлдвэрүүдийг нэрлэсэн. боловсролын байгууллагууд, эрдэм шинжилгээний хүрээлэнгүүд. ОХУ-д хүндэтгэлийн алтан медалийг баталлаа - энэ нь химийн салбарт гарамгай ажилд олгогддог. Эрдэмтний нэрийг Оросын химийн нийгэмлэгт томилсон. Тверь мужид жил бүр Бүс нутгийн Менделеевийн уншлага зохион байгуулдаг. Тэр ч байтугай 101 серийн дугаартай элементийг Дмитрий Ивановичийг хүндэтгэн менделевиум гэж нэрлэжээ.
Түүний гол гавьяа нь үечилсэн хуулийг нээж, химийн элементүүдийн үечилсэн системийг бий болгосон нь дэлхийн шинжлэх ухаанд түүний нэрийг мөнхөлсөн явдал юм. Энэхүү хууль ба үечилсэн систем нь атом ба элементүүдийн тухай сургаалын цаашдын хөгжлийн үндэс нь бидний үеийн хими, физикийн үндэс юм.
Ажлын зорилго:Химийн элементүүдийн үечилсэн хууль ба үечилсэн систем үүсэх урьдчилсан нөхцөлийг судалж, Дмитрий Иванович Менделеевийн энэхүү нээлтэд оруулсан хувь нэмрийг үнэлнэ үү.
1. Үеийн хуулийг нээх урьдчилсан нөхцөл
Химийн элементүүдийн байгалийн ангилал, тэдгээрийг системчлэх үндэслэлийг эрэлхийлэх ажил Үелэх хуулийг нээхээс өмнө эхэлсэн. Үелэх хуулийг нээх үед 63 химийн элемент мэдэгдэж, тэдгээрийн нэгдлүүдийн найрлага, шинж чанарыг тодорхойлсон.
1.1 Ангилал
Шведийн нэрт химич энгийн бодис, нэгдлүүдийн шинж чанарын ялгаан дээр үндэслэн бүх элементүүдийг металл ба металл бус гэж хуваасан. Тэрээр металууд нь үндсэн исэл ба суурь, металл бустай тохирч байгааг тогтоосон хүчиллэг исэлболон хүчил.
Хүснэгт 1. Ангилал
1.2. Доберейнер гурвал ба элементүүдийн анхны системүүд
1829 онд Германы химич Иоганн Вольфганг Доберейнер элементүүдийг системчлэх анхны чухал оролдлого хийсэн. Тэрээр ижил төстэй шинж чанартай зарим элементүүдийг гурвын бүлэгт нэгтгэж болохыг анзаарсан бөгөөд үүнийг гурвалсан гэж нэрлэдэг.
Доберейнерийн гурвалсан хуулийн мөн чанар нь гурвалын дунд элементийн атомын масс нь гурвалсан хоёр туйлын элементийн атомын массын нийлбэрийн хагастай (арифметик дундаж) ойролцоо байсан явдал байв. Доберейнерийн гурвалууд нь тодорхой хэмжээгээр Менделеевийн бүлгүүдийн прототипүүд боловч эдгээр санаанууд бүхэлдээ хэт төгс бус хэвээр байна. Кальци, стронций, барийн нэг гэр бүлд магни эсвэл хүхэр, селен, теллурын гэр бүлд хүчилтөрөгч байхгүй байгаа нь ижил төстэй элементүүдийн багцыг зөвхөн гурвалсан нэгдэлд зохиомлоор хязгаарласны үр дүн юм. Энэ утгаараа Дёберейнер P, As, Sb, Bi гэсэн ижил төстэй шинж чанартай дөрвөн элементийн гурвалыг тусгаарлаж чадаагүй явдал юм. Доберейнер фосфор ба хүнцэл, сурьма, висмутын химийн шинж чанаруудын гүн аналогийг тодорхой харсан боловч өмнө нь гурвалсан эрэл хайгуулаар хязгаарлагдаж байсан тул зөв шийдлийг олж чадаагүй юм. Хагас зуун жилийн дараа Лотар Майер хэрвээ Доберейнер гурвалсан байдлаасаа түр зуур сатаарсан бол эдгээр дөрвөн элементийн ижил төстэй байдлыг нэгэн зэрэг олж харах байсан гэж хэлэх болно.
Хэдийгээр Доберейнер мэдээжийн хэрэг бүх мэдэгдэж буй элементүүдийг гурвалсан хэсгүүдэд хувааж чадаагүй ч гурвалын хууль нь атомын масс ба элементүүд болон тэдгээрийн нэгдлүүдийн шинж чанаруудын хоорондын хамаарал байгааг тодорхой харуулсан. Системчлэлийн цаашдын бүх оролдлого нь элементүүдийг атомын массын дагуу байрлуулахад үндэслэсэн байв.
1.3. Спираль де Шанкуртуа (1862)
Парисын дээд сургуулийн профессор Александр Бегуиер де Шанкуртуа тухайн үед мэдэгдэж байсан бүх химийн элементүүдийг атомын массыг нэмэгдүүлэх нэг дарааллаар байрлуулж, үүссэн цувааг цилиндрийн гадаргуу дээр суурийнх нь өнцгөөр үүссэн шугамын дагуу хэрэглэв. Суурийн хавтгайд 45 ° (гэж нэрлэгддэг дэлхийн спираль). Цилиндрийн гадаргууг задлахад цилиндрийн тэнхлэгтэй параллель босоо шугамууд дээр ижил төстэй шинж чанартай химийн элементүүд байсан нь тогтоогджээ. Тиймээс лити, натри, кали нэг босоо чиглэлд унасан; бериллий, магни, кальци; хүчилтөрөгч, хүхэр, селен, теллур гэх мэт. Де Шанкуртуа спираль сул тал нь ижил шугам дээр ижил төстэй байдаг. химийн шинж чанарЭлементүүд нь огт өөр химийн шинж чанартай элементүүд болж хувирав. Манган нь шүлтлэг металлын бүлэгт, тэдэнтэй ямар ч холбоогүй титан нь хүчилтөрөгч, хүхрийн бүлэгт орсон. Элементүүдийн шинж чанарын үечилсэн байдлын тухай санаа ингэж төрсөн боловч түүнд анхаарал хандуулаагүй бөгөөд удалгүй мартагдсан юм.
Де Шанкуртуагийн спираль үүссэний дараа удалгүй Америкийн эрдэмтэн Жон Ньюландс элементүүдийн химийн шинж чанарыг атомын масстай нь харьцуулах оролдлого хийсэн. Элементүүдийг атомын массыг нэмэгдүүлэх дарааллаар байрлуулж, Ньюландс найм дахь элемент бүрийн хооронд ижил төстэй шинж чанарууд гарч ирснийг анзаарав. Ньюландс олдсон хэв маягийг хөгжмийн хэмжүүрийн долоон интервалтай адилтган октавын хууль гэж нэрлэжээ. Хүснэгтэндээ тэрээр химийн элементүүдийг тус бүрдээ долоон элементийн босоо бүлэгт хувааж, нэгэн зэрэг олж мэдэв. жижиг өөрчлөлтзарим элементийн дараалал), ижил төстэй химийн шинж чанартай элементүүд ижил хэвтээ шугам дээр гарч ирдэг. Мэдээжийн хэрэг Жон Ньюландс атомын массыг нэмэгдүүлэх дарааллаар байрлуулсан хэд хэдэн элементүүдийг өгч, химийн элементүүдэд харгалзах атомын дугаарыг өгч, энэ дараалал ба физикийн хоорондын системчилсэн хамаарлыг анзаарсан анхны хүн юм. химийн шинж чанарэлементүүд. Ийм дарааллаар элементүүдийн шинж чанарууд давтагддаг, тэдгээрийн эквивалент жин (масс) нь 7 нэгжээр, эсвэл 7-ын үржвэрийн утгаар ялгаатай, өөрөөр хэлбэл найм дахь элемент нь шинж чанаруудыг давтдаг гэж бичжээ. хөгжмийн найм дахь ноот нь эхлээд давтагддаг шиг эхнийх нь.
Ньюландс гэрлийн элементүүдэд тохиолддог энэхүү хамаарлыг бүх нийтийн шинж чанартай болгохыг хичээсэн. Түүний хүснэгтэд ижил төстэй элементүүд нь хэвтээ эгнээнд байрладаг боловч нэг мөрөнд шинж чанараараа огт өөр элементүүд байдаг. Лондонгийн химийн нийгэмлэг түүний октавын хуулийг хайхрамжгүй хүлээн авч, Ньюландад элементүүдийг цагаан толгойн дарааллаар байрлуулж, ямар ч хэв маягийг тодорхойлохыг оролдохыг санал болгов.
1.5 Odling болон Meyer хүснэгтүүд
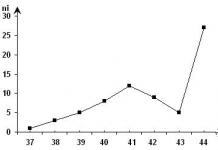
Мөн 1864 онд Германы химич Лотар Мейерийн анхны хүснэгт гарч ирэв; Үүнд 28 элемент орсон бөгөөд тэдгээрийн валентийн дагуу зургаан баганад байрлуулсан. Мейер ижил төстэй элементүүдийн цуваа дахь атомын массын тогтмол (Дёберейнерийн гурвалтай төстэй) өөрчлөлтийг онцлон тэмдэглэхийн тулд хүснэгтийн элементүүдийн тоог зориудаар хязгаарласан.
Зураг 3. Химийн элементүүдийн Мейерийн хүснэгт
1870 онд Мейер есөн босоо баганаас бүрдсэн "Элементүүдийн мөн чанар нь тэдгээрийн атомын жингийн функц" гэсэн шинэ хүснэгтийг агуулсан бүтээлээ хэвлүүлсэн. Үүнтэй төстэй элементүүд нь хүснэгтийн хэвтээ эгнээнд байрладаг; Майер зарим нүдийг хоосон орхисон. Хүснэгтэнд элементийн атомын эзэлхүүний атомын жингээс хамаарах графикийг хавсаргасан бөгөөд энэ нь тухайн нэр томьёог төгс харуулсан хөрөө хэлбэртэй хэлбэртэй байдаг. « үе үе », Тухайн үед Менделеев аль хэдийн санал болгосон.
2. Тогтмол хуулийн нээлт
Тогтмол хуулийг хэрхэн нээсэн тухай ойр дотны хүмүүсийн хэд хэдэн түүх байдаг; Эдгээр түүхийг нүдээр үзсэн гэрчүүд амаар дамжуулж, дараа нь хэвлэлд нэвтэрч, холбогдох баримтат мэдээлэл дутмаг байсан тул одоо болтол баталгаажуулах боломжгүй нэгэн төрлийн домог болсон. Санкт-Петербургийн геологийн профессорын түүх сонирхолтой. Их сургууль (), дотны найз. Тогтмол хуулийг нээсэн тэр өдрүүдэд зочилж байсан тэрээр өөрийн элементүүдийн системийг бий болгоход хэрхэн ажилласан тухай сонирхолтой өгүүлбэрүүдийг өгүүлсэн бөгөөд түүхийг нийтэлсэн хүн:
"Гавьяат профессор Александр Александрович Иностранцев надад Менделеевийн бүтээлч үйл явцыг дуусгадаг зөн совингийн талаар эелдэгээр хэлэв. хамгийн дээд зэрэгсонирхолтой зүйлс. Нэгэн удаа Физик-математикийн факультетийн нарийн бичгийн дарга байхдаа А.А.Менделеевтэй уулзахаар ирсэн бөгөөд тэрээр эрдэмтэн, дотны найзын хувьд байнга хамт байсан сүнслэг харилцаа холбоо. Тэр харав: Д.И. Гунигтай, гутарсан байдалтай ширээний ард зогсож байна.
Та юу хийж байна, Дмитрий Иванович?
Менделеев дараа нь элементүүдийн үечилсэн системд юу шингэсэн тухай ярьж эхэлсэн боловч тэр үед хууль, хүснэгт хараахан бүрдээгүй байсан: "Миний толгойд бүх зүйл нийлсэн" гэж Менделеев гашуунаар нэмж хэлэв. Үүнийг ширээн дээр байна." Хэсэг хугацааны дараа дараах зүйл тохиолдов. Менделеев гурван өдөр, гурван шөнө унтахгүйгээр ширээн дээрээ ажиллаж, оюун санааны бүтээн байгуулалтынхаа үр дүнг хүснэгтэд нэгтгэхийг оролдсон боловч түүнд хүрэх оролдлого бүтэлгүйтэв. Эцэст нь, хэт ядаргааны нөлөөгөөр Менделеев орондоо орж, тэр даруй унтжээ. "Би зүүдэндээ элементүүдийг шаардлагатай хэмжээгээр байрлуулсан ширээг харж байна. Би сэрээд тэр даруй цаасан дээр бичсэн - зөвхөн нэг газар дараа нь залруулга хийх шаардлагатай болсон."
Дараа нь элементийн ангиллыг эцэслэн гаргахдаа бие даасан элементүүдийн талаархи мэдээллийг бичсэн картуудыг хэрхэн ашигласан тухай "Химийн үндэс" номонд өгсөн өөрийн гэрчлэлийг харгалзан үзэх шаардлагатай. Элементүүдийн хоорондох үл мэдэгдэх харилцааг тодорхойлохын тулд картууд яг хэрэгтэй байсан бөгөөд эцсийн загварт огт хэрэггүй байв. Хамгийн гол нь хүснэгтийн анхны ноорогоос харахад тэдгээрийн дээр бичигдсэн элемент бүхий картууд нь бүлгүүд, эгнээний (үе) дарааллаар байршаагүй, зөвхөн бүлгүүдийн дарааллаар (үе хараахан болоогүй байсан) байрладаг. анх нээсэн). Бүлгүүдийг бие биенийхээ доор байрлуулсан бөгөөд элементүүдийн босоо багана (үе) нь бие биентэйгээ зэргэлдээ оршиж, тодорхой химийн шинж чанарууд нь үе үе байдаг нийтлэг тасралтгүй цуврал элементүүдийг бүрдүүлдэг болохыг олж тогтооход хүргэсэн бүлгүүдийг ийм байдлаар байрлуулсан. давтагдсан. Энэ нь хатуухан хэлэхэд үечилсэн хуулийн нээлт байсан юм.
Түүнээс гадна, хэрэв зөвхөн бүлгүүд төдийгүй элементүүдийн үеүүд аль хэдийн мэдэгдэж байсан бол бие даасан элементүүдийн карт ашиглах шаардлагагүй болно.
Гурав дахь түүхийг дахин өөрийнх нь хэлснээр дотны найз болох Чехийн нэрт химичээс гаралтай. Энэ түүхийг 1907 онд Браунер нийтэлсэн. түүний агуу найз нас барсны дараа; 1930 онд Чехословакийн химичүүдийн бүтээлийн цуглуулгад дахин хэвлэгдсэн. Дэлхийн 2-р дайны үед энэ түүхийг Жералд Друс Богуслав Браунерын намтарт бичсэн байдаг. Браунерын хэлснээр тэрээр химийн сурах бичиг, өөрөөр хэлбэл "Химийн үндэс" эмхэтгэл нь үечилсэн хуулийг нээж, боловсруулахад хэрхэн тусалсан талаар түүнд хэлэв.
"Би сурах бичгээ бичиж эхлэхэд надад химийн элементүүдийг хуваарилах систем хэрэгтэй гэж би мэдэрсэн, тиймээс одоо байгаа бүх системүүд нь зохиомлоор бий болгохыг хичээсэн Байгалийн систем.” Энэ зорилгоор би жижиг картон цаасан дээр элементүүдийн тэмдэг, тэдгээрийн атомын жинг бичиж, дараа нь тэдгээрийг бүлэглэж эхлэв. янз бүрийн аргаарижил төстэй байдлын дагуу. Гэхдээ би картоныг өсөн нэмэгдэж буй атомын жингийн дагуу ар араас нь байрлуулах хүртэл энэ арга надад таалагдсангүй. Би хүснэгтийн эхний мөрийг байрлуулахдаа:
H=1, Li=7, Be=9, B=11, C=12, N=14, O=16, F=19,
Дараах элементүүд нь литийн доороос эхлээд эхнийх нь доор хоёр дахь эгнээ үүсгэж болохыг би олж мэдсэн. Дараа нь би энэ шинэ эгнээнд байгааг олж мэдсэн:
Na=23, Mg=24, Al=27, Si=28, P=31, S=32, Cl=35.5
натри нь литийн бүх шинж чанарыг давтдаг; дараах элементүүдийн хувьд ижил зүйл тохиолддог. Үүнтэй ижил давталт нь тодорхой хугацааны дараа гурав дахь эгнээнд тохиолдож, бүх эгнээнд үргэлжилдэг."
Энэ бол түүний үгнээс өгүүлсэн түүх юм. Цаашид энэхүү түүхийн тайлбар, хөгжилд тэрээр “ижил төстэй элементүүдийг бүлэг болгон, атомын жин нэмэгдэхийн хэрээр элементүүдийн шинж чанар, шинж чанар нь аажмаар өөрчлөгддөг эгнээ болгон байрлуулсан нь дээр дурдсан байдаг. Түүний ширээний зүүн талд "цахилгаан эерэг" элементүүд, баруун талд нь "цахилгаан сөрөг" гэсэн үг байдаг.
Тиймээс түүний хэлсэн үгнээс өгүүлсэн түүх нь бүхэл бүтэн нээлт, байгалийн элементүүдийн системийг бий болгосон түүхэнд хамаатай биш, харин зөвхөн энэ нээлтийн эцсийн шатанд, аль хэдийн үндэслэсэн. системийг бий болгосноор тэрээр энэхүү системийн элементүүдийн суурь болох химийн бодисын үечилсэн хуулийг нээж, томъёолж чадсан. Товчхондоо, Браунерын өгүүлсэн түүх нь элементүүдийн системийн найрлагын түүхэнд хамаарахгүй, харин аль хэдийн эмхэтгэсэн системийн үндсэн дээр үечилсэн хуулийг боловсруулсан түүхэнд хамаатай юм.
Дөрөв дэх хувилбар байгаа эсэхийг 1934 онд хэвлэгдсэн сонгосон бүтээлүүдийн хоёрдугаар ботийн редакцийн дараах үгэнд оруулсан болно. мөн үечилсэн хуультай холбоотой бүтээлүүдийг агуулсан. заасан ботид "Зөвхөн нэг өгүүлэл "Comment j" ai trouve la loi periodique" намтар зүйн шинж чанартайгаар ороогүй гэж бичжээ." Зарим шалтгааны улмаас тэрээр энэ нийтлэлийг хаана нийтэлсэн холбоосыг өгөөгүй. Энэ нь мэдээжийн хэрэг асар их сонирхлыг төрүүлсэн, учир нь нэрнээс нь харахад энэ нь үечилсэн хуулийг хэрхэн нээсэн тухай бүх химичүүдийн сонирхсон асуултад эцэст нь хариулт өгөх болно гэж найдаж болох бөгөөд энэ хариултыг гуравдагч этгээдээс хүлээн авахгүй. гэсэн үг, гэхдээ энэ өгүүллийг проф. намтар зүйн шинж чанартай гэж хассан гэсэн ишлэл нь огт үндэслэлгүй мэт санагдсан тул үүнийг үечилсэн хуулийн бүтээлийн цуглуулгад оруулах ёстой байсан бөгөөд үүнээс хасагдаагүй болно. Энэхүү нийтлэлийг хайсны үр дүнд 1899 онд Францын цэвэр болон хэрэглээний химийн сэтгүүлд "Comment j" ai trouve le systeme periodique des elements гэсэн сонирхолтой гарчигтай нийтлэл хэвлэгдсэн болохыг олж мэдэв. (“Би элементүүдийн үечилсэн системийг хэрхэн олсон бэ”). Энэ нийтлэлд бичсэн тэмдэглэлд сэтгүүлийн редакторууд 1899 онд сонгогдсонтой нь холбогдуулан Д.И. Парисын Шинжлэх Ухааны Академийн гадаад корреспондент гишүүн өөрийн үечилсэн системийн талаар сэтгүүлд бичих хүсэлт гаргажээ. энэ хүсэлтийг маш их хүсэл зоригоор биелүүлж, орос хэл дээр бичсэн бүтээлээ Францын сэтгүүлд илгээв. Энэхүү бүтээлийг франц хэл рүү орчуулах ажлыг редакторууд өөрсдөө хийсэн.
Нийтлэгдсэн тексттэй хамгийн ойрын танилцах ФранцЭнэ нь зарим зүйл биш гэдгийг нийтлэл харуулж байна шинэ ажил, А яг орчуулгатүүний бичсэн "Химийн элементүүдийн үечилсэн хууль" нийтлэлээс Нэвтэрхий толь бичигБрокхаус ба Эфрон нар бөгөөд 1898 онд энэхүү толь бичгийн XXIII ботид хэвлэгдсэн. Францын сэтгүүлийн орчуулагч эсвэл редакторууд илүү их сонирхол татахын тулд "Химийн элементүүдийн үечилсэн хууль" гэсэн хэтэрхий хуурай санагдсан гарчгийг "Би хэрхэн элементүүдийн үечилсэн системийг олсон бэ" гэж өөрчилсөн нь ойлгомжтой. Үгүй бол бүх зүйл өөрчлөгдөөгүй хэвээр байсан бөгөөд би нийтлэлдээ намтарчилсан зүйл нэмээгүй.
Эдгээр нь химийн элементүүдийн үелэх систем хэрхэн нээгдсэн тухай домог, түүхүүд юм. Энэхүү агуу нээлтийн түүхтэй холбоотой шинэ материалыг нээж, судалсны үр дүнд эдгээрээс үүссэн бүх эргэлзээг арилгасан гэж үзэж болно.

Зураг 4. "Элементүүдийн системийн туршлага"
1869 оны 3-р сарын 6-нд Оросын химийн нийгэмлэгийн хурал дээр Менделеевийн эзгүйд (Менделеев Тверь муж дахь бяслагны үйлдвэрт байсан бөгөөд магадгүй Москва муж дахь "Боблово" эдлэн газартаа зогссон байж магадгүй) мессеж. Тэр үечилсэн хуулийг нээсэн тухай сэтгүүлийнхээ дараагийн дугаарт (“Оросын химийн нийгэмлэгийн сэтгүүл”) нийтлэлд хүлээн авсан.
1871 онд "Химийн элементүүдийн үечилсэн хууль" хэмээх сүүлчийн өгүүлэлдээ Менделеев Үелэх хуулийн дараах томъёоллыг өгсөн: "Элементүүдийн шинж чанар, тиймээс тэдгээрийн бүрдүүлдэг энгийн ба нийлмэл биетүүдийн шинж чанарууд нь үе үе хамааралтай байдаг. атомын жин."
Үүний зэрэгцээ Менделеев өөрийн үелэх системд сонгодог болсон хэлбэрийг (богино хувилбар гэж нэрлэдэг) өгсөн. Өмнөх хүмүүсээс ялгаатай нь Менделеев хүснэгтийг эмхэтгэж, атомын жингийн тоон утгуудад эргэлзээгүй хэв маяг байгааг онцлон тэмдэглэсэн төдийгүй эдгээр хэв маягийг нэрлэхээр шийджээ.нийтлэг хууль

байгаль. Атомын масс нь элементийн шинж чанарыг тодорхойлдог гэсэн таамаглалд үндэслэн тэрээр зарим элементийн хүлээн зөвшөөрөгдсөн атомын жинг өөрчилж, одоог хүртэл нээгдээгүй элементүүдийн шинж чанарыг нарийвчлан тайлбарлах үүрэг хүлээсэн.
Зураг 5. Химийн элементүүдийн үечилсэн систем Д.И.Менделеев олон жилийн турш Үеийн хуулийг хүлээн зөвшөөрөхийн төлөө тэмцсэн; Менделеевийн таамаглаж байсан элементүүдийг олж илрүүлсний дараа л түүний санаанууд хүлээн зөвшөөрөгдсөн: галлиум (Пол Лекок де Бойсбодран, 1875), скандий (Ларс Нилссон, 1879), германиум (Клеменс Винклер, 1886) - эка-хөнгөн цагаан ба эка- - цахиур. 1880-аад оны дунд үеэс Үеийн хуулийг эцэст нь нэг хууль гэж хүлээн зөвшөөрсөнонолын үндэс
хими.
Дүгнэлт Тогтмол хууль тоглосонасар том үүрэг бусдын химийн хөгжилд. Бүх элементүүд болон тэдгээрийн физик, химийн шинж чанаруудын хоорондын харилцан хамаарлыг олж мэдсэн. Энэ нь байгалийн шинжлэх ухаанд асар их ач холбогдолтой шинжлэх ухаан, философийн асуудлыг тавьсан: энэ харилцан уялдааг тайлбарлах ёстой. Үелэх хуулийг нээсний дараа бүх элементийн атомыг нэг зарчмын дагуу барьж байгуулах, тэдгээрийн бүтэц нь элементүүдийн шинж чанарын үечилсэн байдлыг тусгах ёстой гэдэг нь тодорхой болсон. Ийнхүү үечилсэн хууль нь атом-молекулын шинжлэх ухааны хувьслын чухал холбоос болж, атомын бүтцийн онолыг хөгжүүлэхэд чухал нөлөө үзүүлсэн. Тэрээр мөн "химийн элемент" хэмээх орчин үеийн ойлголтыг боловсруулах, энгийн ба нарийн төвөгтэй бодисын талаархи санаа бодлыг тодруулахад хувь нэмэр оруулсан. Үүнд атомын физикийн дэвшил цөмийн эрчим хүчхиймэл элементүүдийг нэгтгэх нь зөвхөн Үеийн хуулийн ачаар боломжтой болсон.
“Шинэ онол, гайхалтай ерөнхий дүгнэлт гарч ирээд үхнэ. Шинэ санаанууд бидний аль хэдийн хоцрогдсон атом, электрон тухай ойлголтыг орлох болно. Хамгийн агуу нээлтүүдТуршилтууд нь өнгөрсөн үеийг хүчингүй болгож, өнөөдөр гайхалтай шинэлэг, өргөн цар хүрээг нээх болно - энэ бүхэн ирж, алга болно, гэхдээ Менделеевийн үечилсэн хууль үргэлж оршин тогтнож, эрэл хайгуулыг удирдан чиглүүлэх болно.
Лавлагаа
2. . Химийн үндэс. - Т. 2. – М. – Л.: Госхимизат, 1947. - 389 х.
3. . Химийн чиглэлээр сонгогдсон лекцүүд. - М .: Илүү өндөр. сургууль, 1968 он. - 224 секунд.
4. . Тогтмол хуулийг нээсэн түүхийн талаархи шинэ материалууд. - М.–Л.: Хэвлэлийн газар Акад. ЗХУ, 1950 он. - 145 секунд.
5. . Философийн шинжилгээЭхний ээлжийн хууль дээр ажилладаг (). - М .: Хэвлэлийн газар Акад. ЗХУ, 1959 он. - 294 с.
6. . Философи дахь шинэ бүтээл ба шинэ бүтээлийн философи. - Т.2. - М.: Шинжлэх ухаан ба сургууль, 1922.- P.88.