ශතවර්ෂ ගණනාවකට පෙර, පෘථිවියේ ඕනෑම ද්රව්යයක් අන්වීක්ෂීය අංශු වලින් සමන්විත වන බව මිනිසුන් තේරුම් ගත්හ. යම් කාලයක් ගත වූ අතර, මෙම අංශු සැබවින්ම පවතින බව විද්යාඥයින් ඔප්පු කළහ. ඒවා පරමාණු ලෙස හැඳින්විණි. සාමාන්යයෙන් පරමාණු වලට වෙන වෙනම පැවතිය නොහැකි අතර ඒවා කණ්ඩායම් වලට ඒකාබද්ධ වේ. මෙම කණ්ඩායම් අණු ලෙස හැඳින්වේ.
"අණු" යන නම පැමිණෙන්නේ ලතින් වචනය මවුල වලින් වන අතර එහි තේරුම බර, අවහිර කිරීම, තොග සහ කුඩා උපසර්ගය - කුලා ය. මීට පෙර, මෙම යෙදුම වෙනුවට, "corpuscle" යන වචනය භාවිතා කරන ලදී, වචනාර්ථයෙන් "කුඩා ශරීරය" යන්නයි. අණුවක් යනු කුමක්දැයි සොයා බැලීම සඳහා, අපි හැරෙමු පැහැදිලි කිරීමේ ශබ්දකෝෂ. Ushakov ගේ ශබ්දකෝෂය පවසන්නේ මෙය ස්වයංක්රීයව පැවතිය හැකි කුඩාම අංශුව වන අතර එයට අයත් වන ද්රව්යයේ සියලුම ගුණාංග ඇති බවයි. අණු සහ පරමාණු අප වටා ඇති අතර, අපට ඒවා ස්පර්ශ කළ නොහැකි වුවද, අපට සැබවින්ම පෙනෙන්නේ ඒවායේ යෝධ පොකුරු පමණි.
ජලය සමඟ උදාහරණයක්
අණුවක් යනු කුමක්දැයි පැහැදිලි කිරීමට හොඳම ක්රමය වන්නේ වතුර වීදුරුවක උදාහරණය භාවිතා කිරීමයි. ඔබ එයින් අඩක් වත් කළහොත්, ඉතිරි ජලයෙහි රසය, වර්ණය සහ සංයුතිය වෙනස් නොවේ. වෙනස් දෙයක් බලාපොරොත්තු වීම අමුතු දෙයක් වනු ඇත. ඔබ නැවත අඩක් දැමුවහොත්, ප්රමාණය අඩු වනු ඇත, නමුත් ගුණාංග නැවත එලෙසම පවතිනු ඇත. මේ විදියට ඉදිරියට ගියොත් අපි අවසන් වෙන්නේ පුංචි බිංදුවක්. එය තවමත් පයිප්පයකින් බෙදිය හැකි නමුත්, මෙම ක්රියාවලිය දින නියමයක් නොමැතිව දිගටම කරගෙන යා නොහැක.

අවසානයේදී, ඔබ කුඩා අංශුවකින් අවසන් වනු ඇත, ඉතිරිය තවදුරටත් ජලය නොවේ. අණුවක් යනු කුමක්ද සහ එය කෙතරම් කුඩාද යන්න පිළිබඳ අදහසක් ලබා ගැනීමට, එක් ජල බිංදුවක අණු කීයක් තිබේදැයි අනුමාන කිරීමට උත්සාහ කරන්න. ඔබ සිතන්නේ කෙසේද? බිලියන? බිලියන සියයක්? ඇත්ත වශයෙන්ම, ඔවුන්ගෙන් sextillion සියයක් පමණ ඇත. මෙය එකකට පසුව බිංදු විසිතුනක් ඇති සංඛ්යාවකි. එවැනි විශාලත්වය සිතීම දුෂ්කර ය, එබැවින් අපි සැසඳීමක් භාවිතා කරමු: ඇපල් ගෙඩිය මෙන් බොහෝ වාර ගණනක් විශාල ඇපල් ගෙඩියක ප්රමාණය කුඩා වේ, එබැවින් එය බලවත්ම දෘශ්ය අන්වීක්ෂයකින් පවා දැකිය නොහැක.
සහ පරමාණු
අප දැනටමත් දන්නා පරිදි, සියලුම අන්වීක්ෂීය අංශු, අනෙක් අතට, පරමාණු වලින් සමන්විත වේ. ඒවායේ අංකය අනුව, මධ්යම පරමාණුවල කක්ෂ සහ බන්ධන වර්ගය අනුව, අණු වල ජ්යාමිතික හැඩය වෙනස් විය හැක. උදාහරණයක් ලෙස, මිනිස් DNA සර්පිලාකාර හැඩයෙන් ඇඹරී ඇති අතර, සාමාන්ය මේස ලුණු වල කුඩාම අංශුව මේ ආකාරයෙන් පෙනේ: යම් ආකාරයකින් අණුවකින් පරමාණු කිහිපයක් ඉවතට ගතහොත්, එහි විනාශය සිදුවනු ඇත. ඒ අතරම, අන්තිමයා කොතැනකවත් නොයනු ඇත, නමුත් තවත් ක්ෂුද්ර අංශු කොටසක් බවට පත්වනු ඇත.
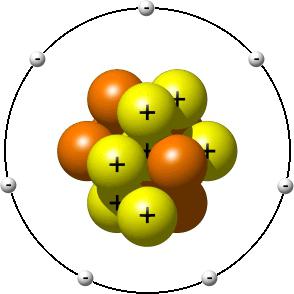
අපි අණුවක් යනු කුමක්දැයි සොයා ගත් පසු, අපි පරමාණුව වෙත යමු. එහි ව්යුහය ග්රහලෝක පද්ධතියකට බෙහෙවින් සමාන ය: මධ්යයේ නියුට්රෝන සහ ධන ආරෝපිත ප්රෝටෝන සහිත න්යෂ්ටියක් ඇති අතර ඉලෙක්ට්රෝන එය වටා විවිධ කක්ෂවල භ්රමණය වේ. සාමාන්යයෙන්, පරමාණුව විද්යුත් වශයෙන් මධ්යස්ථ වේ. වෙනත් වචන වලින් කිවහොත්, ඉලෙක්ට්රෝන ගණන ප්රෝටෝන ගණනට සමාන වේ.
අපගේ ලිපිය ප්රයෝජනවත් යැයි අපි බලාපොරොත්තු වෙමු, දැන් ඔබට අණුවක් සහ පරමාණුවක් යනු කුමක්ද, ඒවා ව්යුහගත වන්නේ කෙසේද සහ ඒවා වෙනස් වන්නේ කෙසේද යන්න පිළිබඳ ප්රශ්න නොමැත.
පරමාණු වෙනස් වන්නේ කෙසේද?

පරිවර්තනය, "පරමාණු" යන්නෙන් අදහස් වන්නේ බෙදිය නොහැකි බවයි. එය එසේ නම් කර ඇත්තේ දිගු කලක් එය පදාර්ථයේ කුඩාම කොටස ලෙස සැලකූ බැවිනි. නමුත් විද්යාවේ තවත් වර්ධනයක් පෙන්නුම් කළේ මෙය එසේ නොවන බවයි. එබැවින්, පරමාණුවක් සෑදී ඇත්තේ කුමක්ද සහ විවිධ මූලද්රව්යවල පරමාණු වෙනස් වන්නේ කෙසේදැයි සොයා බලමු.
පරමාණුක ව්යුහය
අද විද්යාව රසායනික මූලද්රව්ය වර්ග 126ක් දනී. සාමාන්ය සැලැස්මඒවායේ පරමාණු වල ව්යුහය සමාන වේ. සෑම එකක්ම ඉලෙක්ට්රෝන කක්ෂගත වන ප්රෝටෝන සහ නියුට්රෝන න්යෂ්ටියක් ඇත. ඉලෙක්ට්රෝන යනු සෘණ ආරෝපිත අංශු වේ. ඒවා න්යෂ්ටිය වටා භ්රමණය වන විට ඒවා සෑදේ ඉලෙක්ට්රෝන වලාකුළු.
ප්රෝටෝන ධන ආරෝපිත අංශු වේ. විවේකයේදී, පරමාණුවක එකම ප්රෝටෝන සහ ඉලෙක්ට්රෝන සංඛ්යාවක් අඩංගු වේ රසායනික මූලද්රව්යයවිදුලි ආරෝපණයක් නොමැත. කෙසේ වෙතත්, ප්රතික්රියා අතරතුර, එය වෙනත් මූලද්රව්යවලට ඉලෙක්ට්රෝන ලබා දී ධන ආරෝපිත අංශුවක් බවට පත් විය හැකිය, නැතහොත් ඒවා ඉවතට ගෙන සෘණ ආරෝපිත අංශුවක් බවට පත් විය හැකිය. නියුට්රෝන කිසිදු ආරෝපණයක් ගෙන නොයන නමුත් ඒවා මූලද්රව්යයේ ස්කන්ධයට බලපායි. ප්රෝටෝන සහ නියුට්රෝන සඳහා ඒකාබද්ධ නාමයක් සොයා ගන්නා ලදී - නියුක්ලියෝන.
විවිධ මූලද්රව්යවල පරමාණු
විවිධ මූලද්රව්යවල පරමාණු න්යෂ්ටියේ ඇති ප්රෝටෝන සංඛ්යාවෙන් එකිනෙකට වෙනස් වේ. ඉලෙක්ට්රෝන ගණන වෙනස් විය හැකි නමුත් ප්රෝටෝන ගණන කිසිවිටෙකත් වෙනස් නොවේ. මූලද්රව්යයේ පරමාණුක ක්රමාංකය මගින් න්යෂ්ටියේ කොපමණ ප්රෝටෝන අඩංගු වේද යන්න සොයා ගත හැක ආවර්තිතා වගුවමෙන්ඩලීව්. හයිඩ්රජන් (අංක 1) හි ඉලෙක්ට්රෝන 1 ක් සහ ප්රෝටෝන 1 ක් විවේකයේ, ලිතියම් ඇත  (අංක 3) - ඉලෙක්ට්රෝන 3 ක් සහ ප්රෝටෝන 3 ක්, කාබන් (අංක 6) - ඉලෙක්ට්රෝන 6 ක් සහ ප්රෝටෝන 6 ක්.
(අංක 3) - ඉලෙක්ට්රෝන 3 ක් සහ ප්රෝටෝන 3 ක්, කාබන් (අංක 6) - ඉලෙක්ට්රෝන 6 ක් සහ ප්රෝටෝන 6 ක්.
විවිධ පරමාණුවල විවිධ ප්රෝටෝන සංඛ්යා ඇති බැවින් ඒවායේ ස්කන්ධයන්ද වෙනස් වේ. මූලද්රව්යයක ස්කන්ධය ප්රධාන වශයෙන් සෑදී ඇත්තේ ප්රෝටෝන සහ නියුට්රෝන මගිනි, මන්ද ඉලෙක්ට්රෝනවල බර නොසැලකිය හැකි බැවිනි. නමුත් න්යෂ්ටියේ ඇති විවිධ නියුට්රෝන සංඛ්යා නිසා එකම මූලද්රව්යයේ පරමාණුවලට පවා විවිධ බර තිබිය හැක. නියුට්රෝන සංඛ්යාව ප්රෝටෝන සංඛ්යාවෙන් වෙනස් වන පරමාණු සමස්ථානික ලෙස හැඳින්වේ. නිදසුනක් ලෙස, ස්වභාවධර්මයේ කාබන් පරමාණු C12 (ප්රෝටෝන 6 ක් සහ නියුට්රෝන 6 ක්), C13 (ප්රෝටෝන 6 ක් සහ නියුට්රෝන 7 ක්) සහ 2 සිට 16 දක්වා නියුට්රෝන අන්තර්ගතයක් සහිත අනෙකුත් ප්රභේද ඇත.
Atom thing (Garg et al 2014); මූලද්රව්ය යනු දෙය වර්ගයකි.
පරමාණුවක් යනු ප්රෝටෝන, නියුට්රෝන සහ ඉලෙක්ට්රෝන වල එකතුවකි. උදාසීන තත්වයේ එක් හුදකලා පරමාණුවකට සමහර ප්රෝටෝන, සමාන ඉලෙක්ට්රෝන සංඛ්යාවක් සහ සමහර නියුට්රෝන ඇත (සැහැල්ලු මූලද්රව්ය සඳහා ප්රෝටෝන වලට සමාන සංඛ්යාවක්, බර මූලද්රව්ය සඳහා 50% වැඩි). පරමාණුවක ඇති නියුට්රෝන හෝ ප්රෝටෝන සංඛ්යාව වෙනස් වන්නේ ඔබ අංශු ත්වරණකාරකවල ලබා ගන්නා වැනි විකිරණශීලී ක්රියාවලීන් හෝ ඉතා ඉහළ ශක්ති අන්තර්ක්රියාවල ප්රතිඵලයක් ලෙස පමණි. සහ මම කියන්නේ ඇත්තටමඅධි ශක්තිය: ඩයිනමයිට් කූරු පුපුරවා හැරීම ගැන ඔබ සිතුවද, ප්රෝටෝන සහ නියුට්රෝන සමඟ අවුල් කිරීමට එය ප්රමාණවත් ශක්තියක් නොවේ. රසායන විද්යාව ඇති වන්නේ පරමාණු එකතු වී ඉලෙක්ට්රෝන හුවමාරු කරන විට හෝ ඉලෙක්ට්රෝන එකිනෙක ලබා දෙන විටය. රසායනික ප්රතික්රියාසෑම විටම සිදු වන අතර ඒවායින් බොහොමයක් සඳහා වැඩි ශක්තියක් අවශ්ය නොවේ: ඉලෙක්ට්රෝන පරමාණුවකින් පරමාණුවට ගෙනයාම බොහෝ විට ඉතා සරල ය.
ඉතින්, පරමාණුවක රසායනය ඉලෙක්ට්රෝන ගණන මත රඳා පවතින අතර හුදකලා පරමාණුවක ඇති ඉලෙක්ට්රෝන ගණන කෙලින්ම ප්රෝටෝන ගණන මත රඳා පවතී. ඉලෙක්ට්රෝන පරමාණු වලින් එකතු කිරීම සහ ඉවත් කිරීම ඉතා පහසුයි (ඔබේ හිසකෙස් මත බැලූනයක් අතුල්ලන්න: ස්ථිතික විදුලිය- ඔබ ඔබේ හිසකෙස් අතර ඉලෙක්ට්රෝන මාරු කර ඇත බැලූනය), එබැවින් අපි පරමාණු ඒවායේ ඇති ප්රෝටෝන ගණන අනුව වර්ගීකරණය කරමු. නියුට්රෝන එතරම් අදාළ නොවේ: මම ඒවා ගැන අවසානයේ කතා කරමි.
එබැවින් මූලද්රව්යය පරමාණුවක් තීරණය වන්නේ ප්රෝටෝන ගණනෙනි. සියලුම හයිඩ්රජන් පරමාණුවලට එක් ප්රෝටෝනයක් ඇති අතර එක් ප්රෝටෝනයක් සහිත සියලුම පරමාණු හයිඩ්රජන් වේ. ප්රෝටෝන දෙකක් හීලියම්, තුනක් ලිතියම්, දාහත ක්ලෝරීන්, 79 රන් ය, යනාදී මූලද්රව්යයක පිරිසිදු නියැදියක මේ ආකාරයේ පරමාණු පමණක් අඩංගු වේ: නිදසුනක් ලෙස, පිරිසිදු යකඩ නියැදියක අඩංගු වන්නේ ප්රෝටෝන 26ක් සහිත පරමාණු පමණි. අනෙක් අතට, ජලය මූලද්රව්යයක් නොවේ: ජල අණුවක් හයිඩ්රජන් පරමාණු දෙකකින් (එක් ප්රෝටෝනයක් බැගින්) ඔක්සිජන් පරමාණුවක් (ප්රෝටෝන අටක්) සමඟ ඉලෙක්ට්රෝන බෙදා ගනී.
දැන්, මූලද්රව්යයක් "සරල ස්වරූපයකට බෙදිය නොහැක" සහ පරමාණු "සරල ආකාරයක්" නොවන්නේ මන්ද යන්නෙන් අදහස් කරන්නේ කුමක්ද? යකඩ පරමාණුව නිසා ඒවා සරල ස්වරූපයක් නොවේ - යකඩ: එය එකම හැඩය, එය සරල නොවේ. මේ විදියට හිතන්න. මම ඔබට පිරිසිදු යකඩ කැබැල්ලක් ලබා දෙන්නේ නම්, ඔබට කළ හැක්කේ එය කුඩා යකඩ කැබලිවලට කැඩීම හෝ මල බැඳීමට ඉඩ දීම වැනි සංකීර්ණ ද්රව්යයක් බවට පත් කිරීමයි. - මලකඩ සෑදෙන්නේ යකඩ හා ඔක්සිජන් වලින්. ඔබට සෑදිය හැකි කුඩාම යකඩ කැබැල්ල තනි යකඩ පරමාණුවකි, නමුත් එය තවමත් ඇදහිය නොහැකි තරම් කුඩා යකඩ කැබැල්ලකි. ඔබට තනි තනි යකඩ පරමාණු ඉක්මවා යකඩ කැබැල්ලක් කැඩීමට අවශ්ය නම්, ඔබට භාවිතා කිරීමට අවශ්ය වනු ඇත න්යෂ්ටික ප්රතික්රියාකාරකයහෝ අංශු ත්වරණයක් හෝ එවැනි දෙයක්, පසුව අවසානයේ ඔබ පරමාණුවල ප්රෝටෝන ගණන වෙනස් කරන නිසා ඔබට යකඩ නොවන දෙයක් ලබා ගත හැකිය.
අපි මෙය ජලයට සමාන කරමු. මම ඔබට පිරිසිදු ජලය බාල්දියක් ලබා දෙන්නේ නම්, යකඩ කැබැල්ලක් මෙන්, ඔබට එය කුඩා හා කුඩා සාම්පලවලට බෙදිය හැකිය, අවසානයේ එක් ජල අණුවක් සමඟ අවසන් වේ. නමුත් ඔබට වෙනත් දෙයක් කළ හැකිය: ඔබ ජලය හරහා විදුලිය ගමන් කරන්නේ නම්, එය පිරිසිදු හයිඩ්රජන් බවට බෙදී යයි පිරිසිදු ඔක්සිජන්. මේවා "සරල" ද්රව්ය වන්නේ සෑම එකක්ම සෑදී ඇත්තේ එක් මූලද්රව්යයක පරමාණු වලින් වන අතර ජලයට මූලද්රව්ය දෙකක පරමාණු ඇත.
නියුට්රෝන ගැන කුමක් කිව හැකිද? හොඳයි, රසායන විද්යා දෘෂ්ටිකෝණයකින්, ඔවුන් බොහෝ දේ නොකරන අතර එකම ප්රෝටෝන සංඛ්යාවක් ඇති නමුත් විවිධ නියුට්රෝන සංඛ්යා ඇති පරමාණු සමාන සංඛ්යාවක් ඇති පරමාණුවලට වඩා බොහෝ සමාන වේ (උදාහරණයක් ලෙස ඒවාට අවශ්යයෙන්ම එකම රසායන විද්යාව ඇත). නියුට්රෝන, නමුත් විවිධ ප්රෝටෝන සංඛ්යා. ප්රෝටෝන සංඛ්යාව අනුව වර්ගීකරණය කිරීම වඩාත් තර්කානුකූලයි, මෙය ඉලෙක්ට්රෝන ගණන තීරණය කරන අතර රසායන විද්යාව තීරණය කරයි.
ඔබ නියුට්රෝන සංඛ්යාව අනුව පරමාණු වර්ග කිරීමට උත්සාහ කළා යැයි සිතමු, බොහෝ ආගන් පරමාණු (ප්රෝටෝන 18) ට නියුට්රෝන 22 ක් ඇත, නමුත් සමහර ක්ලෝරීන් පරමාණු (ප්රෝටෝන 17) සහ පොටෑසියම් පරමාණු (ප්රෝටෝන 19) ද 22 ක් ඇත. නියුට්රෝන. ඔබ බොහෝ විට දන්නා පරිදි, ආගන්, ක්ලෝරීන් සහ පොටෑසියම් එකිනෙකට සම්පූර්ණයෙන්ම වෙනස් වේ. අනෙක් අතට, නියුට්රෝන 22ක් සහිත පොටෑසියම් පරමාණු නියුට්රෝන 21ක් ඇති වඩාත් සුලබ ආකාරයේ පොටෑසියම් පරමාණුවලට බොහෝ දුරට සමානව හැසිරේ.
"පරමාණු" සහ "අණු" යන සංකල්ප අතර වෙනස කුමක්ද? සහ හොඳම පිළිතුර ලැබුණා
සන්රයිස් වෙතින් පිළිතුර[විශේෂඥ]
පරමාණුවක් කුඩා වේ, එක් අණුවක පරමාණු කිහිපයක් තිබිය හැක (උදාහරණ - හයිඩ්රජන් පරමාණු 2ක් සහ එක් ඔක්සිජන් පරමාණුවක් = ජල අණුවක්)
වෙතින් පිළිතුරු ඩයනා මාමිනා[ගුරු]
අණුවක් සෑදී ඇත්තේ පරමාණු වලිනි.
වෙතින් පිළිතුරු නැත[ගුරු]
හැර පොදු ස්ථාන, උපතින් ද.
වෙතින් පිළිතුරු වාතය[නවකයා]
පරමාණුවක් යනු න්යෂ්ටියකින් සහ ඉලෙක්ට්රෝන වලින් සමන්විත අන්තර්ක්රියා කරන මූලද්රව්යවල විද්යුත් උදාසීන පද්ධතියකි. , සහ අණුවක් යනු පරමාණු 2ක් හෝ වැඩි ගණනකින් සමන්විත සංයෝගයකි
වෙතින් පිළිතුරු Durchlaucht Furst[ගුරු]
පරමාණුවක් (පුරාණ ග්රීක ἄτομος - බෙදිය නොහැකි) යනු රසායනික මූලද්රව්යයක කුඩාම කොටස වන අතර එය එහි ගුණාංග දරන්නා වේ. පරමාණුවක් පරමාණුක න්යෂ්ටියකින් සහ අවට ඉලෙක්ට්රෝන වලාකුළකින් සමන්විත වේ. පරමාණුවක න්යෂ්ටිය ධන ආරෝපිත ප්රෝටෝන සහ විද්යුත් උදාසීන නියුට්රෝන වලින් සමන්විත වන අතර එය වටා ඇති වලාකුළ සෘණ ආරෝපිත ඉලෙක්ට්රෝන වලින් සමන්විත වේ. න්යෂ්ටියේ ඇති ප්රෝටෝන සංඛ්යාව ඉලෙක්ට්රෝන ගණන සමඟ සමපාත වන්නේ නම්, සමස්තයක් ලෙස පරමාණුව විද්යුත් වශයෙන් උදාසීන වේ. එසේ නොමැති නම්, එය යම් ධන හෝ ඍණ ආරෝපණයක් ඇති අතර එය අයනයක් ලෙස හැඳින්වේ. න්යෂ්ටියේ ඇති ප්රෝටෝන සහ නියුට්රෝන සංඛ්යාව අනුව පරමාණු වර්ගීකරණය කර ඇත: ප්රෝටෝන සංඛ්යාව මගින් පරමාණුව යම් රසායනික මූලද්රව්යයකට අයත් වේද යන්න තීරණය කරයි, සහ නියුට්රෝන ගණන මෙම මූලද්රව්යයේ සමස්ථානිකය තීරණය කරයි.
පරමාණු විවිධ වර්ගවිවිධ ප්රමාණවලින්, අන්තර් පරමාණුක බන්ධන මගින් සම්බන්ධ වී, අණු සාදයි.
පදාර්ථයේ කුඩාම වෙන් කළ නොහැකි කොටස ලෙස පරමාණුව පිළිබඳ සංකල්පය මුලින්ම සකස් කරන ලද්දේ පුරාණ ඉන්දියානු සහ පුරාණ ග්රීක දාර්ශනිකයන්(බලන්න: පරමාණුවාදය). XVII දී සහ XVIII සියවස්සමහර ද්රව්ය තවදුරටත් ඒවායේ සංඝටක මූලද්රව්යවලට බෙදිය නොහැකි බව පෙන්නුම් කරමින් මෙම අදහස පර්යේෂණාත්මකව තහවුරු කිරීමට රසායන විද්යාඥයින්ට හැකි විය. රසායනික ක්රම. කෙසේ වෙතත්, තුළ XIX අග- 20 වන ශතවර්ෂයේ ආරම්භයේ දී, භෞතික විද්යාඥයින් උප පරමාණුක අංශු සහ පරමාණුවේ සංයුක්ත ව්යුහය සොයා ගත් අතර, පරමාණුව සැබවින්ම "බෙදිය නොහැකි" නොවන බව පැහැදිලි විය.
අණු (නව ලතින් අණු, ලතින් මවුල වලින් කුඩා - ස්කන්ධය) යනු එහි රසායනික ගුණාංග රැගෙන යන ද්රව්යයක කුඩාම අංශුවයි.
අණුවක් පරමාණු දෙකකින් හෝ වැඩි ගණනකින් සමන්විත වන අතර එය සංඝටක ගණන මගින් සංලක්ෂිත වේ පරමාණුක න්යෂ්ටිසහ ඉලෙක්ට්රෝන, මෙන්ම යම් ව්යුහයක්.
සාමාන්යයෙන් උපකල්පනය කරනු ලබන්නේ අණු මධ්යස්ථ (විද්යුත් ආරෝපණයක් නොපවතියි) සහ යුගල නොකළ ඉලෙක්ට්රෝන රැගෙන නොයන බවයි (සියලු සංයුජතා සංතෘප්ත වේ); ආරෝපිත අණු අයන ලෙස හැඳින්වේ, ඒකීයතාවයෙන් වෙනස් බහුත්වයක් සහිත අණු (එනම්, යුගල නොකළ ඉලෙක්ට්රෝන සහ අසංතෘප්ත සංයුජතා සහිත) රැඩිකල් ලෙස හැඳින්වේ.
පරමාණු සිය ගණනක් හෝ දහස් ගණනක් මගින් සෑදෙන අණු සාර්ව අණු ලෙස හැඳින්වේ. අණු වල ව්යුහාත්මක ලක්ෂණ තීරණය කරයි භෞතික ගුණාංගමෙම අණු වලින් සමන්විත ද්රව්යය.
වෙතින් පිළිතුරු මාරියම් අබ්දුල්ලා[නවකයා]
පරමාණුවලට විද්යුත් ආරෝපණයක් ද ඇති අතර, අණුව මධ්යස්ථ වේ
වෙතින් පිළිතුරු මුර්වට් කසිමොව්[නවකයා]
පරමාණුවක් යනු අණුවක් සෑදී ඇති දෙයයි
පරිවර්තනය, "පරමාණු" යන්නෙන් අදහස් වන්නේ බෙදිය නොහැකි බවයි. එය එසේ නම් කර ඇත්තේ දිගු කලක් එය පදාර්ථයේ කුඩාම කොටස ලෙස සැලකූ බැවිනි. නමුත් විද්යාවේ තවත් වර්ධනයක් පෙන්නුම් කළේ මෙය එසේ නොවන බවයි. එබැවින්, පරමාණුවක් සෑදී ඇත්තේ කුමක්ද සහ විවිධ මූලද්රව්යවල පරමාණු වෙනස් වන්නේ කෙසේදැයි සොයා බලමු.
පරමාණුක ව්යුහය
අද විද්යාව රසායනික මූලද්රව්ය වර්ග 126ක් දනී. ඔවුන්ගේ පරමාණු වල සාමාන්ය ව්යුහය සමාන වේ. සෑම එකක්ම ඉලෙක්ට්රෝන කක්ෂගත වන ප්රෝටෝන සහ නියුට්රෝන න්යෂ්ටියක් ඇත. ඉලෙක්ට්රෝන යනු සෘණ ආරෝපිත අංශු වේ. ඒවා න්යෂ්ටිය වටා භ්රමණය වන විට ඉලෙක්ට්රෝන වලාවක් සෑදේ.
ප්රෝටෝන ධන ආරෝපිත අංශු වේ. විවේකයේදී, පරමාණුවක එකම ප්රෝටෝන සහ ඉලෙක්ට්රෝන සංඛ්යාවක් අඩංගු වේ, එබැවින් එවැනි රසායනික මූලද්රව්යයකට විද්යුත් ආරෝපණයක් නොමැත. කෙසේ වෙතත්, ප්රතික්රියා අතරතුර, එය වෙනත් මූලද්රව්යවලට ඉලෙක්ට්රෝන ලබා දී ධන ආරෝපිත අංශුවක් බවට පත් විය හැකිය, නැතහොත් ඒවා ඉවතට ගෙන සෘණ ආරෝපිත අංශුවක් බවට පත් විය හැකිය. නියුට්රෝන කිසිදු ආරෝපණයක් ගෙන නොයන නමුත් ඒවා මූලද්රව්යයේ ස්කන්ධයට බලපායි. ප්රෝටෝන සහ නියුට්රෝන - නියුක්ලියෝන සඳහා ඒකාබද්ධ නාමයක් සොයා ගන්නා ලදී.
විවිධ මූලද්රව්යවල පරමාණු
විවිධ මූලද්රව්යවල පරමාණු න්යෂ්ටියේ ඇති ප්රෝටෝන සංඛ්යාවෙන් එකිනෙකට වෙනස් වේ. ඉලෙක්ට්රෝන ගණන වෙනස් විය හැකි නමුත් ප්රෝටෝන ගණන කිසිවිටෙකත් වෙනස් නොවේ. න්යෂ්ටිය තුළ ප්රෝටෝන කීයක් අඩංගු වේද යන්න මෙන්ඩලීව්ගේ ආවර්තිතා වගුවේ ඇති මූලද්රව්යයේ අනුක්රමික අංකය මගින් තීරණය කළ හැක. හයිඩ්රජන් (අංක 1) හි ඉලෙක්ට්රෝන 1 ක් සහ ප්රෝටෝන 1 ක් විවේකයේදී, ලිතියම් ඇත  (අංක 3) - ඉලෙක්ට්රෝන 3 ක් සහ ප්රෝටෝන 3 ක්, කාබන් (අංක 6) - ඉලෙක්ට්රෝන 6 ක් සහ ප්රෝටෝන 6 ක්.
(අංක 3) - ඉලෙක්ට්රෝන 3 ක් සහ ප්රෝටෝන 3 ක්, කාබන් (අංක 6) - ඉලෙක්ට්රෝන 6 ක් සහ ප්රෝටෝන 6 ක්.
විවිධ පරමාණුවල විවිධ ප්රෝටෝන සංඛ්යා ඇති බැවින් ඒවායේ ස්කන්ධයන්ද වෙනස් වේ. මූලද්රව්යයක ස්කන්ධය ප්රධාන වශයෙන් සෑදී ඇත්තේ ප්රෝටෝන සහ නියුට්රෝන මගිනි, මන්ද ඉලෙක්ට්රෝනවල බර නොසැලකිය හැකි බැවිනි. නමුත් න්යෂ්ටියේ ඇති විවිධ නියුට්රෝන සංඛ්යා නිසා එකම මූලද්රව්යයේ පරමාණුවලට පවා විවිධ බර තිබිය හැක. නියුට්රෝන සංඛ්යාව ප්රෝටෝන සංඛ්යාවෙන් වෙනස් වන පරමාණු සමස්ථානික ලෙස හැඳින්වේ. නිදසුනක් ලෙස, ස්වභාවධර්මයේ කාබන් පරමාණු C12 (ප්රෝටෝන 6 ක් සහ නියුට්රෝන 6 ක්), C13 (ප්රෝටෝන 6 ක් සහ නියුට්රෝන 7 ක්) සහ 2 සිට 16 දක්වා නියුට්රෝන අන්තර්ගතයක් සහිත අනෙකුත් ප්රභේද ඇත.
අවධානය, අද පමණක්!
වෙනත්
විදේශීය වචනය"ඇල්ෆා" රුසියානු භාෂාවෙන් තදින් මුල් බැස ඇති අතර විවිධ සංයෝජනවල දක්නට ලැබේ. ගැන...
ඇත්ත වශයෙන්ම, අප සෑම කෙනෙකුටම, වඩාත් පොදු අර්ථයෙන්, මූලද්රව්යයක් යනු කුමක්ද යන්න පිළිබඳ හොඳ අදහසක් ඇත. මූලද්රව්යයක් යනු සංරචකයකි ...
"හරය" යන වචනයේ තේරුම බෝලයක් මෙන් හැඩැති යමක හරයයි. කෙසේ වෙතත්, මෙම සංකල්පයේ අර්ථය වෙනස් විය හැකිය, ...
අප සෑම කෙනෙකුම, අවම වශයෙන් එක් වරක්වත්, බොහෝ තරු වලින් වැසී ඇති සුන්දර රාත්රී අහස අගය කළෙමු. ඔබ කවදා හෝ කල්පනා කර තිබේද...
Large Hadron Collider හි නිර්වචනය නම්: LHC යනු ආරෝපිත අංශු ත්වරණකාරකයක් වන අතර, එය නිර්මාණය කර ඇත්තේ...
ඉලෙක්ට්රෝනය වේ මූලික අංශුව, සෘණ විදුලි ආරෝපණයක් ඇති. එය -1 ට සමාන වේ. ඉලෙක්ට්රෝනය ඇතුල් වෙනවා...
ඇතුළත ගලා යන අදෘශ්යමාන බලවේගයක් ඇත ජීව විද්යාත්මක වස්තූන්සහ අජීවී පරිසරය. මෙම බලවේගය හැඳින්වෙන්නේ ...
භෞතික විද්යාවේ සහ රසායන විද්යාවේ විවිධ නියමයන්, න්යායන් සහ නියමයන් ගැන බොහෝ අය හොඳින් දැන නොසිටිති. සහ සමහර, සමහර විට ...
විවිධ වර්ග අතර ප්රතික්රියා රසායනික ද්රව්යසහ මූලද්රව්ය රසායන විද්යාවේ අධ්යයනයේ ප්රධාන විෂයයන්ගෙන් එකකි.…
පදාර්ථය පිළිබඳ සංකල්පය එකවර විද්යාවන් කිහිපයක් අධ්යයනය කරයි. කරුණු දෙකකින් ද්රව්ය යනු කුමක්ද යන ප්රශ්නය අපි විශ්ලේෂණය කරන්නෙමු ...
පාසැලේ රසායන විද්යා පාඩම් වලදී, විවිධ ගැටළු විසඳන ආකාරය ඔවුන් ඔබට උගන්වයි, ඒවා අතර ජනප්රිය ගණනය කිරීමේ ගැටළු වේ.
විදුලි ආරෝපණය - භෞතික ප්රමාණය, එය විද්යුත් චුම්භකයට සහභාගී වීමට ශරීරයට ඇති හැකියාව තීරණය කරයි ...
ඔක්සිකරණ තත්ත්වය යනු අණුවක ඇති පරමාණුවක කොන්දේසි සහිත ආරෝපණයයි, ඉලෙක්ට්රෝන සම්පූර්ණයෙන් පිළිගැනීමේ ප්රතිඵලයක් ලෙස පරමාණුව එය ලබා ගනී, එහි...