Binárna látka chlorid meďnatý (monochlorid), ktorého vzorec je CuCl, je soľ kyseliny chlorovodíkovej. Je to prášok, zvyčajne bielej alebo zelenej farby, veľmi zle rozpustný vo vode. Zelenkastý odtieň monochloridových kryštálov je spôsobený prítomnosťou nečistôt dvojmocnej látky nazývanej chlorid meďnatý ii.
Túto zlúčeninu prvýkrát získal veľký chemik Robert Boyle. Táto udalosť sa stala už dávno a vedec na jej získanie použil jednoduchý kov, meď a dvojmocnosť. Potom v roku 1799 Joseph Proust izoloval kryštály dichloridu z monochloridu. Táto reakcia bola procesom postupného zahrievania roztoku, v dôsledku čoho chlorid meďnatý stratil časť svojho chlóru, asi polovicu svojej prítomnosti. Separácia dichloridu od monochloridu sa uskutočnila bežným premývaním.
Chlorid meďnatý je biely kryštalická látka, ktorý mení tvar pri teplote 408 °C kryštálovú mriežku. Keďže sa táto zlúčenina topí aj vrie prakticky bez rozkladu, jej chemický vzorec sa niekedy píše ako Cu2Cl2. Monochlorid je však rovnako ako iné zlúčeniny medi toxický.
Zlúčenina chloridu meďnatého, ktorej vzorec je napísaný ako CuCl2, vyzerá ako tmavohnedé klinovité monokryštály. Pri interakcii aj s veľmi malým množstvom vody kryštály zlúčeniny menia farbu: z tmavohnedej sa postupne mení na zelenkastú a potom na modrú. Je zaujímavé, že ak do takéhoto vodného roztoku pridáte veľmi málo, kryštály sa vrátia do jedného z medzistavov – zozelenajú.
Teplota topenia látky je 537 °C a pri teplote 954 - 1032 °C vrie. Zlúčenina je rozpustná v látkach, ako je voda, alkohol a amoniak. Jeho hustota je 3,054 g/cm3. Pri konštantnom riedení roztoku a udržiavaní teploty na 25 °C je molárna elektrická vodivosť látky 265,9 cm2/mol.
Chlorid meďnatý sa získava pôsobením chlóru na meď, ako aj uskutočňovaním reakčnej reakcie (II) s Priemyselná výroba je založená na pražení zmesí sulfidov medi s chloridom sodným. V tomto prípade musí byť počas reakcie zabezpečená teplota 550 – 600 °C, v dôsledku čoho okrem uvažovanej látky môže byť plynné skupenstvo zložky ako HCl, sírové plyny a zlúčeniny arzénu. Sú známe priemyselné odvetvia, kde sa chlorid meďnatý vyrába iniciáciou výmennej reakcie medzi síranom meďnatým a BaCl2.
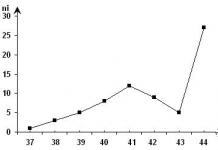
Pri teplote 993 °C sa látka rozkladá na CuCl a Cl2, jej rozpustnosť vo vodných roztokoch je charakterizovaná:
Po rozpustení vo vodnom roztoku pri teplote 25 stupňov sa 77,4 gramov chloridu meďnatého úplne rozpustí v 100 gramoch vody;
Keď teplota roztoku dosiahne 100 °C, rozpustí sa v ňom už 120 gramov látky. V oboch prípadoch sa predpokladá, že hustota CuCl2 bola rovnaká.
Chlorid meďnatý je široko používaný ako chemický katalyzátor, zložka pyrotechnických zmesí pri výrobe rôznych minerálnych farbív. Ako analyzátor spalín pomáha vypočítať koncentráciu spalín a hladinu oxidu uhličitého. Dichlorid sa tiež používa ako nosič kyslíka pre rôznych štádiách chemická výroba, takáto technológia je bežná napríklad pri výrobe organických farbív.
Chlorid meďnatý je napriek svojej nerozpustnej rozpustnosti schopný tvoriť množstvo kryštalických hydrátov. V tomto prípade má koncentrovaný roztok látky schopnosť pridávať oxid dusnatý, ktorý je tiež široko používaný pri výrobe liekov a v chemickom priemysle.
Všeobecné informácie o hydrolýze chloridu meďnatého
DEFINÍCIA
Chlorid meďnatý– priemerná soľ tvorená slabou zásadou – hydroxidom meďnatým (Cu(OH) 2) a silná kyselina– chlorovodíková (chlórovodík) (HCl). Vzorec - CuCl2.
Predstavuje kryštály žltohnedej (tmavohnedej) farby; vo forme kryštalických hydrátov - zelená. Molová hmotnosť – 134 g/mol.
Ryža. 1. Chlorid meďný. Vzhľad.
Hydrolýza chloridu meďnatého
Hydrolyzuje na katióne. Charakter prostredia je kyslý. Teoreticky je možný druhý stupeň. Rovnica hydrolýzy je nasledovná:
Prvá etapa:
CuCl2 ↔ Cu 2+ + 2Cl - (disociácia soli);
Cu 2+ + HOH ↔ CuOH + + H + (hydrolýza katiónom);
Cu2+ + 2Cl - + HOH ↔ CuOH + + 2Cl - + H + (iónová rovnica);
CuCl 2 + H 2 O ↔ Cu(OH)Cl +HCl (molekulárna rovnica).
Druhá etapa:
Cu(OH)Cl ↔ CuOH + + Cl - (disociácia soli);
CuOH + + HOH ↔ Cu(OH) 2 ↓ + H + (hydrolýza katiónom);
CuOH + + Cl - + HOH ↔ Cu(OH) 2 ↓ + Cl - + H + (iónová rovnica);
Cu(OH)Cl + H 2 O ↔ Cu(OH) 2 ↓ + HCl (molekulárna rovnica).
Príklady riešenia problémov
PRÍKLAD 1
PRÍKLAD 2
| Cvičenie | Napíšte rovnicu pre elektrolýzu roztoku chloridu meďnatého. Aké množstvo látky sa uvoľní na katóde, ak sa 5 g chloridu meďnatého podrobí elektrolýze? |
| Riešenie | Napíšme disociačnú rovnicu pre chlorid meďnatý vo vodnom roztoku: CuCl 2 ↔ Cu 2+ +2Cl - . Napíšme konvenčne schému elektrolýzy: (-) Katóda: Cu2+, H20. (+) Anóda: Cl-, H20. Cu 2+ +2e → Cu o; 2Cl - -2e -> Cl2. Potom bude rovnica elektrolýzy pre vodný roztok chloridu meďnatého vyzerať takto: CuCl2 = Cu + Cl2. Vypočítajme množstvo chloridu meďnatého (II) pomocou údajov uvedených v probléme ( molárnej hmotnosti– 134 g/mol): a(CuCI2) = m(CuCI2)/M(CuCI2) = 5/134 = 0,04 mol. Podľa reakčnej rovnice υ(CuCl2) = υ(Cu) = 0,04 mol. Potom vypočítame hmotnosť medi uvoľnenej na katóde (mólová hmotnosť – 64 g/mol): m(Cu) = a(Cu) x M(Cu) = 0,04 x 64 = 2,56 g. |
| Odpoveď | Hmotnosť medi uvoľnenej na katóde je 2,56 g. |
§1. Chemické vlastnosti jednoduchá látka(st. ok. = 0).
a) Vzťah ku kyslíku.
Na rozdiel od svojich susedov podskupiny - striebra a zlata - meď reaguje priamo s kyslíkom. Meď vykazuje nevýznamnú aktivitu voči kyslíku, ale vo vlhkom vzduchu postupne oxiduje a pokryje sa zelenkastým filmom pozostávajúcim zo zásaditých uhličitanov medi:
V suchom vzduchu prebieha oxidácia veľmi pomaly a na povrchu medi sa tvorí tenká vrstva oxidu medi:
Navonok sa meď nemení, pretože oxid meďnatý (I), rovnako ako samotná meď, je ružový. Navyše, vrstva oxidu je taká tenká, že prepúšťa svetlo, t.j. presvitá. Meď inak oxiduje pri zahriatí, napríklad pri 600-800 0 C. V prvých sekundách prebieha oxidácia na oxid meďnatý (I), ktorý sa z povrchu mení na čierny oxid meďnatý (II). Vytvorí sa dvojvrstvový oxidový povlak.
Tvorba Q (Cu20) = 84935 kJ.

Obrázok 2. Štruktúra filmu oxidu medi.
b) Interakcia s vodou.
Kovy podskupiny medi sú na konci elektrochemickej napäťovej série za vodíkovým iónom. Preto tieto kovy nedokážu vytesniť vodík z vody. Zároveň vodík a iné kovy môžu vytesňovať kovy podskupiny medi z roztokov ich solí, napríklad:
Táto reakcia je redoxná, pretože elektróny sa prenášajú:
Molekulárny vodík vytláča kovy podskupiny medi s veľkými ťažkosťami. Vysvetľuje to skutočnosť, že väzba medzi atómami vodíka je silná a na jej prerušenie sa vynakladá veľa energie. Reakcia prebieha iba s atómami vodíka.
V neprítomnosti kyslíka meď prakticky neinteraguje s vodou. V prítomnosti kyslíka meď pomaly reaguje s vodou a pokryje sa zeleným filmom hydroxidu meďnatého a zásaditého uhličitanu:
c) Interakcia s kyselinami.
Meď, ktorá je v sérii napätia po vodíku, ho nevytláča z kyselín. Preto kyselina chlorovodíková a zriedená kyselina sírová nemajú žiadny vplyv na meď.
Avšak v prítomnosti kyslíka sa meď rozpúšťa v týchto kyselinách za vzniku zodpovedajúcich solí:
Jedinou výnimkou je kyselina jodovodíková, ktorá reaguje s meďou za uvoľnenia vodíka a vytvára veľmi stabilný meďnatý (I) komplex:
2 Cu + 3 Ahoj → 2 H[ Cul 2 ] + H 2
Meď tiež reaguje s oxidačnými kyselinami, napríklad kyselinou dusičnou:
Cu + 4HNO 3( konc. .) → Cu(NO 3 ) 2 +2 NIE 2 +2H 2 O
3Cu + 8HNO 3( riedenie .) → 3Cu(č 3 ) 2 +2NO+4H 2 O
A tiež s koncentrovanou studenou kyselinou sírovou:
Cu+H 2 SO 4 (konc.) → CuO + SO 2 +H 2 O
S horúcou koncentrovanou kyselinou sírovou :
Cu+2H 2 SO 4( konc. ., horúce ) → CuSO 4 + SO 2 + 2H 2 O
S bezvodou kyselinou sírovou pri teplote 200 0 C vzniká síran meďnatý:
2Cu + 2H 2 SO 4( bezvodý .) 200 °C → Cu 2 SO 4 ↓+SO 2 + 2H 2 O
d) Vzťah k halogénom a niektorým iným nekovom.
Tvorba Q (CuCl) = 134300 kJ
Tvorba Q (CuCl2) = 111700 kJ
Meď dobre reaguje s halogénmi a vytvára dva typy halogenidov: CuX a CuX 2 .. Pri vystavení halogénom pri izbovej teplote nedochádza k viditeľným zmenám, ale najskôr sa na povrchu vytvorí vrstva adsorbovaných molekúl a potom tenká vrstva halogenidov . Pri zahrievaní prebieha reakcia s meďou veľmi búrlivo. Medený drôt alebo fóliu nahrejeme a horúce spustíme do nádoby s chlórom - v blízkosti medi sa objavia hnedé pary pozostávajúce z chloridu meďnatého CuCl 2 s prímesou chloridu meďnatého CuCl. Reakcia prebieha spontánne v dôsledku uvoľneného tepla. Monivalentné halogenidy medi sa získavajú reakciou kovovej medi s roztokom halogenidu meďného, napríklad:
V tomto prípade sa monochlorid vyzráža z roztoku vo forme bielej zrazeniny na povrchu medi.
Meď tiež pomerne ľahko reaguje so sírou a selénom pri zahrievaní (300-400 °C):
2 Cu + S → Cu 2 S
2Cu +Se→Cu 2 Se
Ale meď nereaguje s vodíkom, uhlíkom a dusíkom ani pri vysoké teploty.
e) Interakcia s oxidmi nekovov
Pri zahrievaní môže meď vytláčať jednoduché látky z niektorých oxidov nekovov (napríklad oxid síry (IV) a oxidy dusíka (II, IV)), čím sa vytvorí termodynamicky stabilnejší oxid medi (II):
4Cu+SO 2 600-800 °C →2CuO + Cu 2 S
4Cu+2NO 2 500-600 °C →4CuO + N 2
2 Cu+2 NIE 500-600° C →2 CuO + N 2
§2. Chemické vlastnosti jednomocnej medi (št. ok. = +1)
Vo vodných roztokoch je ión Cu + veľmi nestabilný a disproporcionálny:
Cu + ↔ Cu 0 + Cu 2+
Meď v oxidačnom stave (+1) sa však môže stabilizovať v zlúčeninách s veľmi nízkou rozpustnosťou alebo komplexáciou.
a) oxid meďnatý (ja) Cu 2 O
Amfotérny oxid. Hnedo-červená kryštalická látka. V prírode sa vyskytuje ako minerál cuprit. Môže sa umelo získať zahrievaním roztoku medenej (II) soli s alkáliou a nejakým silným redukčným činidlom, napríklad formaldehydom alebo glukózou. Oxid meďný nereaguje s vodou. Oxid meďný sa prevedie do roztoku s koncentrovanou kyselinou chlorovodíkovou za vzniku chloridového komplexu:
Cu 2 O+4 HCl→2 H[ CuCl2]+ H 2 O
Rozpustné aj v koncentrovanom roztoku amoniaku a amónnych solí:
Cu 2 0+2NH 4 + →2 +
V zriedenej kyseline sírovej sa disproporcionuje na dvojmocnú meď a kovovú meď:
Cu 2 O+H 2 SO 4 (zriedený) →CuSO 4 + Cu 0 ↓+H 2 O
Oxid meďnatý tiež vstupuje do nasledujúcich reakcií vo vodných roztokoch:
1. Pomaly oxidovaný kyslíkom na hydroxid meďnatý:
2 Cu 2 O+4 H 2 O+ O 2 →4 Cu(OH) 2 ↓
2. Reaguje so zriedenými halogenovodíkovými kyselinami za vzniku zodpovedajúcich halogenidov medi:
Cu 2 O+2 HГ→2CuГ↓ +H 2 O(G=Cl, Br, J)
3. Redukované na kovovú meď pomocou typických redukčných činidiel, napríklad hydrosiričitanu sodného v koncentrovanom roztoku:
2 Cu 2 O+2 NaSO 3 →4 Cu↓+ Na 2 SO 4 + H 2 SO 4
Oxid meďný sa redukuje na kov meď v nasledujúcich reakciách:
1. Pri zahriatí na 1800 °C (rozklad):
2 Cu 2 O - 1800 °C C →2 Cu + O 2
2. Pri zahrievaní v prúde vodíka, oxidu uhoľnatého, hliníka a iných typických redukčných činidiel:
Cu 2 O+H 2 - >250 °C →2Cu +H 2 O
Cu 2 O+CO - 250-300 °C →2Cu +CO 2
3 Cu 2 O + 2 Al - 1000° C →6 Cu + Al 2 O 3
Pri vysokých teplotách tiež oxid meďnatý reaguje:
1. S amoniakom (tvorí sa nitrid meďnatý)
3 Cu 2 O + 2 N.H. 3 - 250° C →2 Cu 3 N + 3 H 2 O
2. S oxidmi alkalických kovov:
Cu 2 O+M 2 O- 600-800 °C →2 MCuO (M= Li, Na, K)
V tomto prípade sa tvoria medené (I) kupráty.
Oxid meďný výrazne reaguje s alkáliami:
Cu 2 O+2 NaOH (konc.) + H 2 O↔2 Na[ Cu(OH) 2 ]
b) hydroxid meďnatý (ja) CuOH
Hydroxid meďný tvorí žltú látku a je nerozpustný vo vode.
Pri zahrievaní alebo varení sa ľahko rozkladá:
2 CuOH → Cu 2 O + H 2 O
c) HalogenidyCuF, CuSl, CuBrACuJ
Všetky tieto zlúčeniny sú biele kryštalické látky, slabo rozpustné vo vode, ale vysoko rozpustné v nadbytku NH 3, kyanidových iónov, tiosíranových iónov a iných silných komplexotvorných činidiel. Jód tvorí iba zlúčeninu Cu +1 J. V plynnom stave vznikajú cykly typu (CuГ) 3. Reverzibilne rozpustné v zodpovedajúcich halogenovodíkových kyselinách:
CuG + HG ↔H[ CuG 2 ] (Г=Cl, Br, J)
Chlorid a bromid meďný sú na vlhkom vzduchu nestabilné a postupne sa premieňajú na zásadité meďnaté soli:
4 CuG +2H 2 O + O 2 →4 Cu(OH)G (G=Cl, Br)
d) Ostatné zlúčeniny medi (ja)
1. Octan meďný (CH 3 COOCu) je zlúčenina medi, ktorá sa javí ako bezfarebné kryštály. Vo vode pomaly hydrolyzuje na Cu 2 O, na vzduchu sa oxiduje na octan meďnatý; CH 3 COOCu sa získava redukciou (CH 3 COO) 2 Cu vodíkom alebo meďou, sublimáciou (CH 3 COO) 2 Cu vo vákuu alebo interakciou (NH 3 OH)SO 4 s (CH 3 COO) 2 Cu v roztoku v prítomnosti H3COONH3. Látka je toxická.
2. Acetylid meďný – červenohnedé, niekedy čierne kryštály. Keď sú kryštály suché, pri údere alebo zahrievaní vybuchnú. Stabilný za mokra. Keď dôjde k detonácii v neprítomnosti kyslíka, nevznikajú žiadne plynné látky. Pod vplyvom kyselín sa rozkladá. Vzniká ako zrazenina pri prechode acetylénu do amoniakových roztokov solí medi (I):
S 2 H 2 +2[ Cu(N.H. 3 ) 2 ](OH) → Cu 2 C 2 ↓ +2 H 2 O+2 N.H. 3
Táto reakcia sa používa na kvalitatívnu detekciu acetylénu.
3. Nitrid medi - anorganická zlúčenina so vzorcom Cu 3 N, tmavozelené kryštály.
Pri zahrievaní sa rozkladá:
2 Cu 3 N - 300° C →6 Cu + N 2
Prudko reaguje s kyselinami:
2 Cu 3 N +6 HCl - 300° C →3 Cu↓ +3 CuCl 2 +2 N.H. 3
§3. Chemické vlastnosti dvojmocnej medi (st. ok. = +2)
Meď má najstabilnejší oxidačný stav a je pre ňu najcharakteristickejšia.
a) oxid meďnatý (II) CuO
CuO je hlavný oxid dvojmocnej medi. Kryštály sú čiernej farby, za normálnych podmienok celkom stabilné a prakticky nerozpustné vo vode. V prírode sa vyskytuje ako čierny minerál tenorit (melakonit). Oxid meďnatý (II) reaguje s kyselinami za vzniku zodpovedajúcich solí medi (II) a vody:
CuO + 2 HNO 3 → Cu(NIE 3 ) 2 + H 2 O
Keď sa CuO taví s alkáliami, tvoria sa medené (II) kupráty:
CuO+2 KOH- t ° → K 2 CuO 2 + H 2 O
Pri zahriatí na 1100 °C sa rozkladá:
4CuO- t ° →2 Cu 2 O + O 2
b) Hydroxid meďnatý (II).Cu(OH) 2
Hydroxid meďnatý je modrá amorfná alebo kryštalická látka, prakticky nerozpustná vo vode. Pri zahriatí na 70-90 °C sa Cu(OH)2 prášok alebo jeho vodné suspenzie rozkladajú na CuO a H2O:
Cu(OH) 2 → CuO + H 2 O
Je to amfotérny hydroxid. Reaguje s kyselinami za vzniku vody a zodpovedajúcej soli medi:
Nereaguje so zriedenými roztokmi alkálií, ale rozpúšťa sa v koncentrovaných roztokoch a vytvára svetlomodré tetrahydroxycupráty (II):
Hydroxid meďnatý tvorí zásadité soli so slabými kyselinami. Veľmi ľahko sa rozpúšťa v prebytku amoniaku za vzniku medeného amoniaku:
Cu(OH) 2 +4NH 4 OH → (OH) 2 +4H 2 O
Amoniak medi má intenzívnu modrofialovú farbu, preto sa používa v analytickej chémii na stanovenie malých množstiev iónov Cu 2+ v roztoku.
c) Soli medi (II)
Jednoduché soli medi (II) sú známe pre väčšinu aniónov, okrem kyanidu a jodidu, ktoré pri interakcii s katiónom Cu 2+ tvoria kovalentné zlúčeniny medi (I), ktoré sú nerozpustné vo vode.
Soli medi (+2) sú rozpustné hlavne vo vode. Modrá farba ich roztokov je spojená s tvorbou iónu 2+. Často kryštalizujú ako hydráty. Z vodného roztoku chloridu meďnatého pod 15 °C teda kryštalizuje tetrahydrát, pri 15-26 °C - trihydrát, nad 26 °C - dihydrát. Vo vodných roztokoch sú meďnaté soli mierne hydrolyzované a často sa z nich vyzrážajú zásadité soli.
1. Pentahydrát síranu meďnatého (síran meďnatý)
Najväčší praktický význam má CuSO 4 * 5H 2 O, nazývaný síran meďnatý. Suchá soľ má modrú farbu, ale pri miernom zahriatí (200 0 C) stráca kryštalizačnú vodu. Bezvodá soľ je biela. Pri ďalšom zahrievaní na 700 0 C sa mení na oxid meďnatý, pričom stráca oxid sírový:
CuSO 4 -- t ° → CuO+ SO 3
Síran meďnatý sa pripravuje rozpustením medi v koncentrovanej kyseline sírovej. Táto reakcia je opísaná v časti "Chemické vlastnosti jednoduchej látky." Síran meďnatý sa používa pri elektrolytickej výrobe medi, v poľnohospodárstve na kontrolu škodcov a chorôb rastlín a na výrobu iných zlúčenín medi.
2. Dihydrát chloridu meďnatého.
Sú to tmavozelené kryštály, ľahko rozpustné vo vode. Koncentrované roztoky chloridu meďnatého sú zelené a zriedené roztoky sú modré. To sa vysvetľuje tvorbou komplexu zeleného chloridu:
Cu 2+ +4 Cl - →[ CuCl 4 ] 2-
A jeho ďalšie ničenie a vznik modrého aqua komplexu.
3. Trihydrát dusičnanu meďnatého.
Modrá kryštalická látka. Získava sa rozpustením medi v kyseline dusičnej. Pri zahrievaní kryštály najskôr strácajú vodu, potom sa rozkladajú s uvoľňovaním kyslíka a oxidu dusičitého a menia sa na oxid meďnatý (II):
2 Cu (č 3 ) 2 -- t° →2CuO+4NO 2 +O 2
4. Hydroxomeďnatý (II) uhličitan.
Uhličitany medi sú nestabilné a v praxi sa takmer nepoužívajú. Určitý význam pre výrobu medi má len zásaditý uhličitan meďnatý Cu 2 (OH) 2 CO 3, ktorý sa v prírode vyskytuje vo forme minerálu malachitu. Pri zahrievaní sa ľahko rozkladá a uvoľňuje vodu, oxid uhoľnatý (IV) a oxid meďnatý (II):
Cu 2 (OH) 2 CO 3 -- t° →2CuO+H 2 O+CO 2
§4. Chemické vlastnosti trojmocnej medi (st. ok. = +3)
Tento oxidačný stav je najmenej stabilný pre meď a zlúčeniny medi (III) sú preto skôr výnimkou ako „pravidlom“. Niektoré trojmocné zlúčeniny medi však existujú.
a) Oxid meďnatý Cu 2 O 3
Ide o kryštalickú látku tmavo granátovej farby. Nerozpúšťa sa vo vode.
Získava sa oxidáciou hydroxidu meďnatého peroxodisíranom draselným v alkalickom prostredí pri záporných teplotách:
2 Cu (OH) 2 +K 2 S 2 O 8 +2 KOH -- -20 °C → Cu 2 O 3 ↓+2 tis 2 SO 4 +3H 2 O
Táto látka sa rozkladá pri teplote 400 0 C:
Cu 2 O 3 -- t ° →2 CuO+ O 2
Oxid meďnatý je silné oxidačné činidlo. Pri reakcii s chlorovodíkom sa chlór redukuje na voľný chlór:
Cu 2 O 3 +6 HCl-- t ° →2 CuCl 2 + Cl 2 +3 H 2 O
b) Mednatany (C)
Sú to čierne alebo modré látky, vo vode nestále, diamagnetické, anión je stuha štvorcov (dsp 2). Vzniká interakciou hydroxidu meďnatého a chlórnanu alkalického kovu v alkalickom prostredí:
2 Cu(OH) 2 + MClO + 2 NaOH→2 milCuO 3 + NaCl +3 H 2 O (M= Na- Čs)
c) hexafluorocuprát draselný (III)
Zelená látka, paramagnetická. Oktaedrická štruktúra sp 3 d 2. Komplex fluoridu meďnatého CuF 3, ktorý sa vo voľnom stave rozkladá pri -60 0 C. Vzniká zahrievaním zmesi chloridov draslíka a medi vo fluórovej atmosfére:
3KCl + CuCl + 3F 2 → K 3 + 2Cl 2
Rozkladá vodu za vzniku voľného fluóru.
§5. Zlúčeniny medi v oxidačnom stave (+4)
Veda zatiaľ pozná iba jedinú látku, kde je meď v oxidačnom stave +4, je to hexafluorocuprát cézny (IV) - Cs 2 Cu +4 F 6 - oranžová kryštalická látka, stabilná v sklenených ampulkách pri 0 0 C. Reaguje nasilu vodou. Získava sa fluoridáciou s vysoký krvný tlak a teplota zmesi chloridov cézia a medi:
CuCl 2 +2CsCl +3F 2 -- t ° r → Čs 2 CuF 6 +2Cl 2
Základné informácie:
| Ochranné, zabraňujúce prenikaniu spór húb a patogénov do vedúcich tkanív |
| Korónové žlté telo (bezvodé) až modrozelené kryštály (dihydrát) |
Vydanie:
chlorid meďnatý: správanie v životnom prostredí
| Indikátor | Význam | Vysvetlenie | ||
| Rozpustnosť vo vode pri 20 o C (mg/l) | 757000 Q4 High||||
| Rozpustnosť v organických rozpúšťadlách pri 20 o C (mg/l) | 680 000 Q4 - Metanol -||||
| Teplota topenia (o C) | - - -||||
| Bod varu (o C) | - - -||||
| Teplota rozkladu (o C) | - - -||||
| Bod vzplanutia (o C) | - - -||||
| Rozdeľovací koeficient v systéme oktanol/voda pri pH 7, 20 o C | P: ----||||
| Špecifická hmotnosť (g/ml) / Špecifická hmotnosť | 3.39 Q3 -||||
| Disociačná konštanta (pKa) pri 25 °C | - - -||||
| Poznámka: | ||||
| Tlak pár pri 25 o C (MPa) | 1,00 X 10 -10 Q1 Nie je prchavý||||
| Henryho konštanta pri 25 o C (Pa*m 3 /mol) | - - -||||
| Henryho konštanta pri 20 o C (bezrozmerná) | 7,29 X 10-21 vypočítané Nie je prchavý||||
| Doba rozpadu v pôde (dni) | DT50 (typické) - - -||||
| - | ||||
| Vodná fotolýza DT50 (dni) pri pH 7 | Význam: ----||||
| - | ||||
| Vodná hydrolýza DT50 (dni) pri 20 °C a pH 7 | Význam: ----||||
| - | ||||
| Depozícia vody DT50 (dni) | - - -||||
| Len vodná fáza DT50 (dni) | - - -||||
| Index potenciálneho vylúhovania GUS | - - -||||
| Index zvýšenia koncentrácie v SCI podzemnej vody (µg/l) pri aplikačnej dávke 1 kg/ha (l/ha) | Význam: ----||||
| - | ||||
| Potenciál pre index transportu viazaného na častice | - - -||||
| Koc - koeficient rozdelenia organického uhlíka (ml/g) | - - -||||
| Stabilita pH: | ||||
| Poznámka: | ||||
| Freundlichova adsorpčná izoterma | Kf: -- | -|||
| - | ||||
| Maximálna absorpcia UV žiarenia (l/(mol*cm)) | - - -||||
chlorid meďnatý: ekotoxicita
| Indikátor | Význam | Zdroj / Kvalitatívne ukazovatele / Iné informácie | Vysvetlenie | |
| Biokoncentračný faktor | BCF: -- | -|||
| Bioakumulačný potenciál | - - -||||
| LD50 (mg/kg) | 140 V3 Krysa Stredná||||
| Cicavce - Krátkodobá potrava NOEL | (mg/kg): -- | -|||
| Vtáky – akútne LD50 (mg/kg) | - - -||||
| Vtáky – akútna toxicita (CK50/LD50) | - - -||||
| Ryby – akútne 96 hodín CK50 (mg/l) | 0,24 F4 Pstruh dúhový Stredne||||
| Ryby – chronická 21-dňová NOEC (mg/l) | - - -||||
| Vodné bezstavovce – akútne 48 hodín EC50 (mg/l) | - - -||||
| Vodné bezstavovce – chronická 21-dňová NOEC (mg/l) | - - -||||
| Vodné kôrovce – akútne 96 hodín CK50 (mg/l) | 0,134 F3 Krevety Mysis Stredne||||
| Spodné mikroorganizmy - akútne 96 hodín CK50 (mg/l) | 0,043 F4 Komár Chironomus Vysoká||||
| NOEC, statické, voda (mg/l) | - - -||||
| Bentické mikroorganizmy - Chronická 28-dňová NOEC, Sediment (mg/kg) | - - -||||
| Vodné rastliny - akútne 7 dní EC50, biomasa (mg/l) | - - -||||
| Riasy – akútne 72 hodín EC50, rast (mg/l) | 0,55 H1 Neznámy druh Stredný||||
| Riasy - chronická 96 hodinová NOEC, rast (mg/l) | - - -||||
| Včely – akútne 48 hodín LD50 (µg/jednotlivec) | - - -||||
| Pôdne červy – akútne 14-dňové CK50 (mg/kg) | - - -||||
| Pôdne červy - Chronická 14-dňová maximálna neaktívna koncentrácia látky, reprodukcia (mg/kg) | 15 A4 Dážďovka, ako Cu, 8 týždňov Mierne||||
| Iné článkonožce (1) | LR50 (g/ha): - - -||||
| Iné článkonožce (2) | LR50 (g/ha): - - -||||
| Pôdne mikroorganizmy | - - -||||
| Dostupné údaje o mezosvete (mezokozme) | NOEAEC mg/l: - - -||||
chlorid meďnatý: ľudské zdravie
Kľúčové ukazovatele:
| Indikátor | Význam | Zdroj / Kvalitatívne ukazovatele / Iné informácie | Vysvetlenie | |
| Cicavce – akútne orálne LD50 (mg/kg) | 140 V3 Krysa Stredná||||
| Cicavce - Dermálne LD50 (mg/kg telesnej hmotnosti) | - - -||||
| Cicavce - Inhalácia | ||||
MEĎ A JEJ ZLÚČENINY
LEKCIA NA 11. HODINE PRÍRODOVED
Na zvýšenie kognitívnej aktivity a samostatnosti žiakov využívame vyučovacie hodiny kolektívne štúdium materiál. Na takýchto hodinách dostane každý žiak (alebo dvojica žiakov) úlohu, o splnení ktorej musí referovať na tej istej hodine a jeho hlásenie si ostatní žiaci triedy zapisujú do zošitov a je súčasťou obsahu. vzdelávací materiál lekciu. Každý študent prispieva k učeniu triedy o danej téme.
Počas vyučovacej hodiny sa režim práce žiakov mení z intraaktívneho (režim, v ktorom sú informačné toky uzavreté vo vnútri žiakov, typický pre samostatnú prácu) na interaktívny (režim, v ktorom sú informačné toky obojsmerné, t.j. informačné toky z oboch strán). študent a študent, dochádza k výmene informácií). Učiteľ v tomto prípade vystupuje ako organizátor procesu, opravuje a dopĺňa informácie poskytnuté žiakmi.
Lekcie pre kolektívne štúdium materiálu pozostávajú z nasledujúcich etáp:
1. fáza – inštalácia, v ktorej učiteľ vysvetľuje ciele a program práce na vyučovacej hodine (do 7 minút);
2. etapa – samostatná práca žiakov podľa pokynov (do 15 minút);
3. fáza – výmena informácií a zhrnutie hodiny (zaberie všetok zostávajúci čas).
Lekcia „Meď a jej zlúčeniny“ je určená pre triedy s hĺbkové štúdium chémia (4 hodiny chémie týždenne), ktorá prebieha počas dvoch akademických hodín, lekcia aktualizuje vedomosti študentov o nasledujúcich témach: „Všeobecné vlastnosti kovov", "Vzťah ku kovom koncentrovanej kyseliny sírovej, kyseliny dusičnej", " Kvalitatívne reakcie o aldehydoch a viacsýtnych alkoholoch“, „Oxidácia nas jednosýtne alkoholy oxid meďnatý", "Komplexné zlúčeniny".
Pred vyučovacou hodinou žiaci dostávajú domáce úlohy: zopakujte uvedené témy. Predbežná príprava učiteľa na vyučovaciu hodinu pozostáva z vypracovania inštruktážnych kariet pre študentov a prípravy súprav na laboratórne experimenty.
PRIEBEH HODINY
Fáza inštalácie
Učiteľ pózuje žiakom cieľ lekcie: na základe doterajších poznatkov o vlastnostiach látok predpovedať, prakticky potvrdiť, zhrnúť informácie o medi a jej zlúčeninách.
Študenti tvoria elektronický vzorec atóm medi, zistite, aké oxidačné stavy môže vykazovať meď v zlúčeninách, aké vlastnosti budú mať (redoxné, acidobázické) zlúčeniny medi.
V zošitoch žiakov sa objaví tabuľka.
Vlastnosti medi a jej zlúčenín
| Kovové | Cu 2 O – zásaditý oxid | CuO – zásaditý oxid |
| Redukčné činidlo | CuOH je nestabilná zásada | Cu(OH) 2 – nerozpustná zásada |
| CuCl – nerozpustná soľ | CuSO 4 – rozpustná soľ | |
| Majú redoxnú dualitu | Oxidačné činidlá |
Etapa samostatná práca
Na potvrdenie a doplnenie predpokladov žiaci vykonávajú laboratórne pokusy podľa pokynov a zapisujú si rovnice uskutočnených reakcií.
Návod na samostatnú prácu vo dvojiciach
1. Medený drôt zohrejte v plameni. Všimnite si, ako sa zmenila jeho farba. Vložte horúci kalcinovaný medený drôt etanol. Všimnite si zmenu jeho farby. Opakujte tieto manipulácie 2-3 krát.
Skontrolujte, či sa zápach etanolu zmenil.2. Napíšte dve reakčné rovnice zodpovedajúce uskutočneným transformáciám. Aké vlastnosti medi a jej oxidu potvrdzujú tieto reakcie?
Pridajte kyselinu chlorovodíkovú k oxidu meďnému.3. čo pozoruješ? Napíšte reakčné rovnice, pričom vezmite do úvahy, že chlorid meďný je nerozpustná zlúčenina. Aké vlastnosti medi(I) potvrdzujú tieto reakcie?
a) Granule zinku vložte do roztoku síranu meďnatého. Ak reakcia neprebehne, zahrejte roztok. b) Pridajte 1 ml kyseliny sírovej do oxidu meďnatého a zohrejte.4. čo pozoruješ? Napíšte reakčné rovnice.
Aké vlastnosti zlúčenín medi potvrdzujú tieto reakcie?
Vložte prúžok univerzálneho indikátora do roztoku síranu meďnatého.
Vysvetlite výsledok. Napíšte iónovú rovnicu pre hydrolýzu v kroku I. Pridajte roztok síranu medového do roztoku uhličitanu sodného.čo pozoruješ? Zapíšte si to5.
reakčná rovnica
spoločná hydrolýza v molekulárnej a iónovej forme.
Aké zmeny nastali? Napíšte reakčné rovnice. Aké vlastnosti zlúčenín medi dokazujú tieto reakcie?6. Pridajte roztok jodidu draselného k síranu meďnatému.
čo pozoruješ? Napíšte rovnicu reakcie.7. Akú vlastnosť medi(II) táto reakcia dokazuje?
Vložte malý kúsok medeného drôtu do skúmavky s 1 ml koncentrovanej kyseliny dusičnej. Skúmavku uzavrite zátkou.
čo pozoruješ? (Vezmite skúmavku pod ťah.) Napíšte rovnicu reakcie.
Nalejte kyselinu chlorovodíkovú do inej skúmavky a vložte do nej malý kúsok medeného drôtu.8. čo pozoruješ? Vysvetlite svoje pozorovania. Aké vlastnosti medi potvrdzujú tieto reakcie?
Nadbytok hydroxidu sodného sa pridá k síranu meďnatému.9. čo pozoruješ? Vysvetlite svoje pozorovania. Aké vlastnosti medi potvrdzujú tieto reakcie?
reakčná rovnica
čo pozoruješ? Výslednú zrazeninu zahrejte. čo sa stalo? Napíšte reakčné rovnice. Aké vlastnosti zlúčenín medi potvrdzujú tieto reakcie?
K výslednej zrazenine pridajte roztok glycerínu.10. čo pozoruješ? Vysvetlite svoje pozorovania. Aké vlastnosti medi potvrdzujú tieto reakcie?
reakčná rovnica
Aké zmeny nastali? Napíšte reakčné rovnice. Aké vlastnosti zlúčenín medi dokazujú tieto reakcie?
K výslednej zrazenine pridajte roztok glukózy a zahrievajte. čo sa stalo? Napíšte rovnicu reakcie s použitím glukózy ako všeobecný vzorecaldehydy
11. Akú vlastnosť zlúčeniny medi dokazuje táto reakcia?
Pridajte k síranu meďnatému: a) roztok amoniaku; b) roztok fosforečnanu sodného.
čo pozoruješ? Napíšte reakčné rovnice.
Aké vlastnosti zlúčenín medi dokazujú tieto reakcie? Etapa výmeny informácií a sumarizácie Učiteľ kladie otázku týkajúcu sa vlastností konkrétnej látky. Žiaci, ktorí vykonali príslušné pokusy, podajú správu o vykonanom pokuse a zapíšu reakčné rovnice na tabuľu. Potom učiteľ a žiaci doplnia informácie o
chemické vlastnosti
1. ah látky, ktoré nebolo možné potvrdiť reakciami v školskom laboratóriu.
Postup pri diskusii o chemických vlastnostiach zlúčenín medi
Ako reaguje meď s kyselinami, s akými ďalšími látkami môže meď reagovať?
Reakčné rovnice pre meď sú napísané pomocou:
Koncentrovaná a zriedená kyselina dusičná:
Cu + 4HN03 (konc.) = Cu(N03)2 + 2N02 + 2H20,
3Cu + 8HN03 (zriedený) = 3Cu(N03)2 + 2NO + 4H20;
Koncentrovaná kyselina sírová:
Cu + 2H2S04 (konc.) = CuS04 + S02 + 2H20;
Kyslík:
2Cu + 02 = 2CuO; Cu + Cl2 = CuCl2;
Kyselina chlorovodíková
v prítomnosti kyslíka:
2Cu + 4HCl + 02 = 2CuCl2 + 2H20;
2. Chlorid železitý:
Pozornosť sa venuje základným vlastnostiam, schopnosti vytvárať komplexy a redoxnej dualite. Rovnice pre reakcie oxidu meďného s sú napísané:
Kyselina chlorovodíková, kým sa nevytvorí CuCl:
Cu20 + 2HCl = 2CuCl + H20;
Nadbytok HCl:
CuCl + HCl = H;
Redukčné a oxidačné reakcie Cu 2 O:
Cu20 + H2 = 2Cu + H20,
2Cu20 + 02 = 4CuO;
Disproporcia pri zahrievaní:
Cu2O = Cu + CuO,
2CuCl = Cu + CuCl2.
3. Aké vlastnosti má oxid meďnatý?
Pozornosť sa upriamuje na hlavné a oxidačné vlastnosti. Reakčné rovnice pre oxid meďnatý sú napísané:
Kyselina:
CuO + 2H+ = Cu2+ + H20;
Etanol:
C2H5OH + CuO = CH3CHO + Cu + H20;
vodík:
CuO + H2 = Cu + H20;
hliník:
3CuO + 2Al = 3Cu + Al203.
4. Aké vlastnosti má hydroxid meďnatý?
Pozornosť sa upriamuje na oxidačné, zásadité vlastnosti, schopnosť vytvárať komplexy s organickými a anorganické zlúčeniny. Reakčné rovnice sú napísané pomocou:
Aldehyd:
RCHO + 2Cu(OH)2 = RCOOH + Cu20 + 2H20;
Kyselina:
Cu(OH)2 + 2H+ = Cu2+ + 2H20;
Amoniak:
Cu(OH)2 + 4NH3 = (OH)2;
Glycerín:

Rovnica rozkladovej reakcie:
Cu(OH)2 = CuO + H20.
5. Aké vlastnosti vykazujú medené (II) soli?
Pozornosť sa venuje reakciám iónovej výmeny, hydrolýzy, oxidačných vlastností a tvorby komplexov. Rovnice pre reakcie síranu meďnatého s:
Hydroxid sodný:
Cu2+ + 2OH – = Cu(OH)2;
Fosforečnan sodný:
3Cu2+ + 2= Cu3(P04)2;
Cu2+ + Zn = Cu + Zn2+;
Jodid draselný:
2CuS04 + 4KI = 2CuI + I2 + 2K2S04;
Amoniak:
Cu2+ + 4NH3 = 2+;
a reakčné rovnice:
Hydrolýza:
Cu2+ + HOH = CuOH + + H+;
Spoločná hydrolýza s uhličitanom sodným za vzniku malachitu:
2Cu2+ + 2 + H20 = (CuOH)2C03 + C02.
Okrem toho môžete študentom povedať o interakcii oxidu meďnatého a hydroxidu s alkáliami, čo dokazuje ich amfotérny charakter:
Cu(OH)2 + 2NaOH (konc.) = Na2,
Cu + Cl2 = CuCl2,
Cu + HgCl2 = CuCl2 + Hg,
2Cu + 4HCl + 02 = 2CuCl2 + 2H20,
CuO + 2HCl = CuCl2 + H20,
Cu(OH)2 + 2HCl = CuCl2 + 2H20,
CuBr2 + Cl2 = CuCl2 + Br2,
(CuOH)2C03 + 4HCl = 2CuCl2 + 3H20 + C02,
2CuCl + Cl2 = 2CuCl2,
2CuCl = CuCl2 + Cu,
CuS04 + BaCl2 = CuCl2 + BaS04.)
Cvičenie 3. Vytvorte reťazce transformácií zodpovedajúce nasledujúcim schémam a vykonajte ich:

Úloha 1.
Na zliatinu medi a hliníka sa pôsobilo najskôr prebytkom alkálií a potom prebytkom zriedenej kyseliny dusičnej.
.
(Odpoveď Vypočítajte hmotnostné podiely kovov v zliatine, ak je známe, že objemy plynov uvoľnených pri oboch reakciách (za rovnakých podmienok) sú rovnaké
. Hmotnostný podiel medi – 84%) Úloha 2.
(Keď sa kalcinovalo 6,05 g kryštalického hydrátu dusičnanu meďnatého, získali sa 2 g zvyšku. Určte vzorec pôvodnej soli. Odpoveď.
Cu(N03)23H20.) Úloha 3. Medená platňa s hmotnosťou 13,2 g sa ponorila do 300 g roztoku dusičnanu železitého s hmotnostný zlomok soľ 0,112. Keď to vytiahli, ukázalo sa, že hmotnostný zlomok
(Keď sa kalcinovalo 6,05 g kryštalického hydrátu dusičnanu meďnatého, získali sa 2 g zvyšku. Určte vzorec pôvodnej soli. dusičnan železitý sa rovnal hmotnostnému zlomku vytvorenej medenej soli. Určte hmotnosť platne po jej vybratí z roztoku.
10 rokov) Domáce úlohy.
Naučte sa látku napísanú v zošite. Urobte reťazec transformácií zlúčenín medi obsahujúci aspoň desať reakcií a vykonajte ho.
1. LITERATÚRA Puzakov S.A., Popkov V.A. Príručka o chémii pre uchádzačov o štúdium na univerzitách. programy. Otázky, cvičenia, úlohy. Vzorové skúšobné papiere. M.: absolventská škola
2. , 1999, 575 s. Kuzmenko N.E., Eremin V.V.