Реакции между разного рода химическими веществами и элементами являются одним из главных предметов изучения в химии. Чтобы понять, как составить уравнение реакции и использовать их в своих целях необходимо достаточно глубокое понимание всех закономерностей при взаимодействии веществ, а также процессов с химическими реакциями.
Составление уравнений
Одним из способов выражения химической реакции является – химическое уравнение. В нем записывается формула исходного вещества и продукта, коэффициенты, которые показывают, какое количество молекул имеет каждое вещество. Все известные химические реакции разделяются на четыре типа: замещение, соединение, обмен и разложение. Среди них выделяют: окислительно-восстановительные, экзогенные, ионные, обратимые, необратимые и т.д.
Подробнее о том, как составлять уравнения химических реакций:
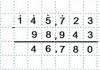
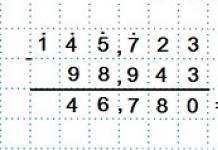
- Необходимо определить, название веществ, взаимодействующих между собой в реакции. Пишем их в левой части нашего уравнения. В качестве примера рассмотрим химическую реакцию, которая образовалась между серной кислотой и алюминием. Реагенты располагаем слева: H2SO4+Al. Далее пишем знак «равно». В химии вы можете повстречать знак «стрелочка», которая указывает вправо, или же направленные противоположно две стрелки, они означают «обратимость». Результат взаимодействия металла и кислоты – соль и водород. Полученные после реакции продукты запиши после знака «равно», то есть справа. H2SO4+Al= H2+ Al2(SO4)3. Итак, у нас видна схема реакции.
- Для составления химического уравнения обязательно нужно найти коэффициенты. Вернемся к предыдущей схеме. Посмотрим на левую ее часть. В составе серной кислоты содержатся атомы водорода, кислорода и серы, в примерном соотношении 2:4:1. В правой части – 3 атома серы и 12 атомов кислорода в соли. Два атома водорода содержится в молекуле газа. В левой части соотношение этих элементов составляет2:3:12
- Для уравнивания количества атомов кислорода и серы, которые в составе сульфата алюминия (III), необходимо поставить перед кислотой в левую часть уравнения коэффициент 3. Теперь у нас в левой части имеется 6 атомов водорода. Для того чтобы сравнять количество элементов водорода, нужно поставить 3 перед водородом в правой части уравнения.
- Теперь осталось лишь уравнять количество алюминия. Поскольку в состав соли входит два атома металла, то в левой части перед алюминием выставляем коэффициент 2. В итоге, мы получим уравнение реакции этой схемы: 2Al+3H2SO4=Al2(SO4)3+3H2
Поняв основные принципы как составить уравнение реакции химических веществ, в дальнейшем не вызовет особого труда записать любую, даже самую экзотическую, с точки зрения химии, реакцию.
2.4. Схемы и уравнения химических реакций
При химических реакциях одни вещества превращаются в другие. Вспомним известную нам реакцию серы с кислородом. И в ней из одних веществ (исходных веществ или реагентов ) образуются другие (конечные вещества или продукты реакции ).
Для записи и передачи информации о химических реакциях используются схемы и уравнения реакций .
Схема реакции показывает, какие вещества вступают в реакцию и какие образуются в результате реакции. И в схемах, и в уравнениях реакций вещества обозначаются их формулами.
Схема горения серы записывается так: S 8 + O 2 SO 2 .
Это означает, что при взаимодействии серы с кислородом протекает химическая реакция, в результате которой образуется диоксид серы (сернистый газ). Все вещества здесь молекулярные, поэтому при записи схемы использованы молекулярные формулы этих веществ. То же относится и к схеме другой реакции – реакции горения белого фосфора:
P 4 + O 2 P 4 O 10 .
При нагревании до 900 o С карбоната кальция (мела, известняка) протекает химическая реакция: карбонат кальция превращается в оксид кальция (негашеную известь) и диоксид углерода (углекислый газ) по схеме:
CaCO 3 CaO + CO 2 .
Для указания на то, что процесс происходит при нагревании, схему (и уравнение) обычно дополняют знаком " t" , а то, что углекислый газ при этом улетучивается, обозначают стрелкой, направленной вверх:
CaCO 3 CaO + CO 2 .
Карбонат кальция и оксид кальция – вещества немолекулярные, поэтому в схеме использованы их простейшие формулы, отражающие состав их формульных единиц. Для молекулярного вещества – углекислого газа – использована молекулярная формула.
Рассмотрим схему реакции, протекающей при
взаимодействия пентахлорида фосфора с водой:
PCl 5 +H 2 O H 3 PO 4
+ HCl.
Из схемы видно, что при этом образуется фосфорная
кислота и хлороводород.
Иногда для передачи информации о химической реакции бывает достаточно и краткой схемы этой реакции, например:
S 8 SO 2 ; P 4 P 4 O 10 ; CaCO 3 CaO.
Естественно, что краткой схеме может соответствовать и несколько разных реакций.
Для любой химической реакции справедлив один
из важнейших законов химии:
При протекании химических реакций атомы не
появляются, не исчезают и не превращаются друг в
друга.
При записи уравнений химических реакций, кроме формул веществ, используются коэффициенты. Как и в алгебре, коэффициент "1" в уравнении химической реакции не ставится, но подразумевается. Рассмотренные нами реакции описываются следующими уравнениями:
1S 8 + 8O 2 = 8SO 2 , или S 8 + 8O 2
= 8SO 2 ;
1P 4 + 5O 2 = 1P 4 O 10 , или P 4 + 5O 2
= P 4 O 10 ;
1CaCO 3 = 1CaO + 1CO 2 , или CaCO 3 = CaO + CO 2 ;
1PCl 5 + 4H 2 O = 1H 3 PO 4 + 5HCl, или PCI 5
+ 4H 2 O = H 3 PO 4 + 5HCI.
Знак равенства между правой и левой частью уравнения означает, что число атомов каждого элемента, входящих в состав исходных веществ, равно числу атомов этого элемента, входящих в продукты реакциии .
Коэффициенты в уравнении химической реакции показывают отношение между числом реагирующих и числом образующихся молекул (для немолекулярных веществ – числом формульных единиц) соответствующих веществ. Так, для реакции, протекающей при взаимодействии пентахлорида фосфора с водой
и так далее (всего 6 пропорций).Обычно отдельный
коэффициент в уравнении реакции не имеет
никакого смысла, но в некоторых случаях может
означать число молекул или формульных единиц
данного вещества.Примеры информации, даваемой
схемами и уравнениями реакций.
1-й пример. Реакция горения метана в кислороде
(или на воздухе):
СН 4 + O 2 CO 2 + H 2 O
(схема),
СН 4 + 2O 2 = CO 2 + 2Н 2 О
(уравнение).
Схема химической реакции показывает, что (1) в реакции, протекающей между метаном и кислородом, образуются углекислый газ и вода.
Уравнение реакции добавляет, что (2) число молекул метана, вступившего в реакцию, относится к числу молекул вступившего в реакцию кислорода, как 1 к 2, и так далее, то есть:
Кроме того, уравнение показывает, что одна молекула метана реагирует с двумя молекулами кислорода, при этом образуется одна молекула углекислого газа и две молекулы воды.
2-й пример. Восстановление железа водородом из
его оксида:
Fe 2 O 3 + H 2 Fe + H 2 O
(схема),
Fe 2 O 3 + 3H 2 = 2Fe + 3H 2 О
(уравнение).
Схема химической реакции показывает, что (1) при взаимодействии оксида железа(Fe 2 O 3) с водородом (которое происходит при нагревании) образуются железо и вода.
Уравнение добавляет к этому, что (2) число формульных единиц оксида железа, вступившего в реакцию, относится к числу вступивших в реакцию молекул водорода, как 1 к 3, и так далее. То есть:
Кроме того уравнение показывает, что одна формульная единица оксида железа реагирует с тремя молекулами водорода, при этом образуется два атома железа и три молекулы воды.
Как вы узнаете в дальнейшем, уравнения реакций дают нам и другую количественную информацию.
| Карбонат кальция – CaCO 3 .
Бесцветное немолекулярное вещество,
нерастворимое в воде. Такие широко известные
горные породы, как мрамор и известняк, состоят в
основном из карбоната кальция. Мел, которым вы
пишете на доске, – тоже карбонат кальция: многие
морские организмы (радиолярии и др.) строят свои
панцири из этого вещества; за длительное время на
дне океана формируются залежи мела,
представляющего собой огромные слои
спрессованных панцирей этих организмов. Карбонат кальция не обладает способностью плавиться – при нагревании он разлагается. Горные породы, образуемые карбонатом кальция, используются в строительстве в качестве отделочных материалов, строительного камня, а также для производства негашеной извести (CaO). В металлургии карбонат кальция в виде известняка добавляют в руду для лучшего образования шлаков. |
РЕАГЕНТЫ,
ПРОДУКТЫ РЕАКЦИИ, СХЕМЫ И УРАВНЕНИЯ РЕАКЦИЙ,
КОЭФФИЦИЕНТЫ В УРАВНЕНИЯХ РЕАКЦИЙ
1.Запишите уравнения, соответствующие следующим
схемам реакций:
а) Na+ Cl 2 NaCl; б) CuO + Al Al 2 O 3 + Сu;
в) N 2 O N 2 + O 2 ; г)NaOH
+ H 2 SO 4 Na 2 SO 4 +
H 2 O.
2.Какую информацию передают составленными вами
уравнениями реакций (среди приведенных веществ
молекулярными являются Cl 2 , N 2 О, N 2 ,
O 2 , H 2 SO 4 и H 2 O; остальные –
немолекулярные).
2.5. Первоначальные сведения о классификации чистых химических веществ
Вы уже познакомились в той или иной степени
примерно с пятьюдесятью индивидуальными
(чистыми) химическими веществами. Всего же науке
известно несколько миллионов таких веществ.
Чтобы не утонуть в этом " море" веществ, их
необходимо систематизировать и прежде всего
классифицировать – классифицировать более
подробно, чем мы делали это в параграфе 1.4 (рис. 1.3).
Вещества отличаются друг от друга своими
свойствами, а свойства веществ определяются
составом и строением. Поэтому важнейшие
признаки, по которым классифицируют вещества –
состав, строение и свойства.
По составу, а точнее, по числу входящих в их
состав элементов, вещества делятся на простые и
сложные (это вы уже знаете). Сложных веществ в
сотни тысяч раз больше, чем простых, поэтому
среди них выделяют бинарные вещества (бинарные
соединения).
Схема этой классификации приведена на рисунке
2.1.
Признаком, по которому проводят дальнейшую
классификацию веществ, являются их свойства.
Начнем с простых веществ.
По физическим свойствам простые вещества
делятся на металлы
и неметаллы
.
Характерные физические свойства металлов:
1) высокая электропроводность (способность
хорошо проводить электрический ток),
2) высокая теплопроводность (способность хорошо
проводить теплоту),
3) высокая пластичность (ковкость, изгибаемость,
вытягиваемость).

Кроме того все металлы обладают " металлическим" блеском. Но следует помнить, что таким блеском обладают не только металлы, но и часть неметаллов, и даже некоторые сложные вещества. Блестит кристаллический кремний, одна из полиморфных модификаций мышьяка, теллур, а это всё – неметаллы. Из сложных веществ – пирит FeS 2 , халькопирит CuFeS 2 и некоторые другие.
Основой систематизации химических элементов, простых веществ и соединений служит ЕСТЕСТВЕННАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ, открытая в 1869 году выдающимся русским химиком Дмитрием Ивановичем Менделеевым (1834 –1907) и названная им " периодической системой" . Усовершенствованная многими поколениями ученых, эта система продолжает называться " периодической" , хотя это и не совсем правильно. Графически система химических элементов выражается в виде таблицы элементов (рис. 2.2); со строением этой таблицы вы подробно познакомитесь, изучая главу 6. Пока же посмотрим, где в таблице элементов расположены элементы, образующие неметаллы , а где – элементы, образующие металлы . Оказывается, элементы, образующие неметаллы, группируются в правом верхнем углу таблицы элементов. Все остальные элементы – элементы, образующие металлы. Причину этого вы узнаете, изучив строение атомов и химические связи.

При комнатной температуре металлы – твердые
вещества (исключение – ртуть, ее температура
плавления – 39 o С).
В отличие от металлов, неметаллы не обладают
каким-либо определенным набором характерных
физических характеристик. Даже агрегатное
состояние у них может быть разным. При комнатной
температуре газообразныдвенадцать простых
веществ (Н 2 , Не, N 2 , O 2 , O 3 , F 2 ,
Nе, Cl 2 , Аr, Кr, Хе, Rn), жидкость одна (Br 2), а
твердых веществ – более десяти (В, С (алмаз) ,
С (графит) , Si, P 4 , S 8 , As, Se, Те, I 2
и др.). По своим химическим свойствам большинство
металлов сильно отличается от большинства
неметаллов, но резкой границы между ними нет.
Многие простые вещества при определенных
условиях могут вступать в реакции друг с другом,
например:
2H 2 + O 2 = 2H 2 O; 2Na + Cl 2 = 2NaCl; 2Ca + O 2 = 2CaO.
В результате таких реакций образуются бинарные соединения.
В принципе, в состав бинарного соединения могут входить любые элементы (кроме гелия и неона). Но часто один из этих элементов – кислород, водород или один из галогенов (фтор, хлор, бром или йод). Такие вещества называются кислородными соединениями , водородными соединениями или галогенидами . Примеры бинарных соединений: CaO, Al 2 O 3 , КН, HCl, АlI 3 , СаС 2 .
Примеры кислородных соединений:
H 2 O
(вода), H 2 O 2 (пероксид водорода), Na 2 O
(оксид натрия), Na 2 O 2 (пероксид натрия),
СО 2 (диоксид углерода), OF 2 (фторид
кислорода). Большинство кислородных соединений
является оксидами
. Чем оксиды отличаются от
остальных кислородных соединений, вы узнаете
позже.
Примеры оксидов:
Li 2 O – оксид лития, CO 2 – диоксид
углерода, CaO – оксид кальция, SiO 2 – диоксид
кремния, Al 2 O 3 – оксид алюминия, Н 2 О
– вода,
MnO 2 – диоксид марганца, SO 3 –триоксид
серы.
Примеры водородных соединений:
NаН –
гидрид натрия, H 2 O – вода, КН – гидрид калия,
НСl – хлороводород, СаH 2 – гидрид кальция,
NH 3 – аммиак, BaH 2 – гидрид бария, CH 4
– метан.
Примеры галогенидов:
CaF 2 –
фторид кальция, BF 3 – трифторид бора, NaCl
– хлорид натрия,PCl 5 – пентахлорид фосфора,
КВr – бромид калия, НВr – бромоводород, AlI 3 –
йодид алюминия, HI – йодоводород.
Примеры названий бинарных соединений приведены
в таблице 6.
Таблица 6. Примеры названий бинарных соединений.
Обратите внимание, что все эти названия содержат суффикс -ид . Таким способом можно назвать любое бинарное соединение, кроме бинарных соединений элементов, образующих металлы (интерметаллических соединений ). Вместе с тем, некоторые бинарные соединения имеют свои традиционные названия (вода, аммиак, хлороводород, метан и некоторые другие).
Среди бинарных соединений на Земле чаще всего встречаются оксиды. Это вызвано тем, что каждый второй атом в земной коре (в атмосфере, гидросфере и литосфере) – атом кислорода. А среди оксидов самое распространенное вещество – вода. Одна из причин этого в том, что водород – также один из самых распространенных элементов в земной коре.
Теперь – о более сложных соединениях. Пусть в состав соединения входят три элемента. Таких соединений очень много. Какие из них наиболее важные? Конечно, кислородсодержащие соединения. И прежде всего, те, в состав которых входит водород. Важность этих соединений вызвана еще и тем, что в результате химических реакций между оксидами и водой получаются как раз такие вещества, например:
СаО + H 2 O = Ca(OH) 2 ; P 4 O 10 + 6H 2 O
= 4H 3 PO 4 ;
Li 2 O + H 2 O = 2LiOH; SO 3 + H 2 O = H 2 SO 4 .
Образующиеся в результате этих реакций вещества называются гидроксидами . Название происходит от сочетания слов " гидрат оксида" , то есть соединение оксида с водой.

Существует много гидроксидов, в том числе и такие, которые не образуются при непосредственном взаимодействии оксида с водой, например: H 2 SiO 3 , Al(OH) 3 , Cu(OH) 2 и другие. Эти вещества тоже называются гидроксидами потому, что при нагревании они разлагаются на оксид и воду.
Вообще-то почти все гидроксиды при нагревании
разлагаются, образуя соответствующий оксид и
воду, например:
Cu(OH) 2 = CuO + H 2 O при 100 o С;
Сa(OH) 2 = CaO +H 2 O при 500 o С;
H 2 SO 4 = SO 3 + H 2 O при 450 o С;
2Аl(ОН) 3 = Al 2 O 3 + 3H 2 O при 200 o С;
H 2 SiO 3 = SiO 2 + H 2 O ниже 100 o С.
Но такие гидроксиды, как, например, NaОН и КОН, не
разлагаются даже при нагревании до 1500 o С.
Примеры названий некоторых гидроксидов приведены в таблице 7 .
Название |
Название |
||
| NаОН | Гидроксид натрия | H 2 SO 4 | Серная кислота |
| КОН | Гидроксид калия | H 2 SO 3 | Сернистая кислота |
| Ca(OH) 2 | Гидроксид кальция | HNO 3 | Азотная кислота |
| Ba(OH) 2 | Гидроксид бария | HNO 2 | Азотистая кислота |
| Аl(ОН) 3 | Гидроксид алюминия | H 3 PO 4 | Фосфорная кислота |
| Cu(OH) 2 | Гидроксид меди | H 2 CO 3 | Угольная кислота |
| Zn(OH) 2 | Гидроксид цинка | H 2 SiO 3 | Кремниевая кислота |
Обратите внимание, что в левой половине таблицы собраны гидроксиды элементов, образующих металлы (название начинается со слова " гидроксид "), а в правой – гидроксиды элементов, образующих неметаллы (название содержит слово " кислота "). Разная форма названий связана с тем, что эти гидроксиды очен ь сильно отличаются по своим химическим свойствам. Например, их растворы по-разному изменяют окраску веществ, называемых индикаторами (точнее, кислотно -основными индикаторами ). Такими веществами-индикаторами являются красители, содержащиеся в чернике, малине, черной смородине, краснокочанной капусте и даже в чае. В лаборатории в качестве индикаторов обычно используют лакмус (природный краситель), метилоранж и фенолфталеин (оба синтетические). Так, лакмус в растворах, содержащих кислоты, окрашивается в красный цвет, а в растворах, содержащих растворимые гидроксиды металлов (щелочи ) – в синий. Цвета других индикаторов приведены в приложении 3. Кислоты имеют кислый вкус, но пробовать их нельзя ни в коем случае, так как большинство из них ядовиты, или обладают обжигающим действием.
Из гидроксидов, приведенных в таблице 6, щелочами являются NaOH, КОН и Ba(OH) 2 . Малорастворимый Са(ОН) 2 тоже меняет окраску индикаторов. Из приведенных в этой же таблице кислот не меняет окраску индикаторов только кремниевая кислота, в частности потому, что она, в отличие от остальных кислот, нерастворима в воде.
Между собой кислоты, как правило, не реагируют,
а с гидроксидами металлов вступают в реакции,
например:
H 2 SO 4 + 2КОН = К 2 SО 4 + H 2 О;
2HNO 3 + Ва(ОН) 2 = Ва(NO 3) 2 + 2H 2 O;
Н 3 РО 4 + 3NаОН = Nа 3 РО 4 + 3Н 2 О.
Кроме воды продуктами этих реакций являются соли – сложные вещества еще одного важнейшего класса. В результате реакции ни кислоты, ни щелочи в растворе не остается, и раствор становится нейтральным , поэтому такие реакции называют реакциями нейтрализации .
Обратите внимание на суффиксы в названиях солей, приведенных в таблице 8.
Таблица 8.Соли и их названия
Название |
Название |
||
| К 2 SO 3 | Сульфит калия | Na 2 CO 3 | Карбонат натрия |
| CaSO 4 | Сульфат кальция | МgСО 3 | Карбонат магния |
| Al 2 (SO 4) 3 | Сульфат алюминия | K 2 SiO 3 | Силикат калия |
| Ba(NO 2) 2 | Нитрит бария | K 3 PO 4 | Фосфат калия |
| Ba(NO 3) 2 | Нитрат бария | Ca 3 (PO 4) 2 | Фосфат кал ьция |
Некоторые гидроксиды из всех остальных гидроксидов реагируют только с кислотами. Такие гидроксиды называются основаниями. Те же гидроксиды, которые реагируют и с кислотами, и с ос нованиями (щелочами), называются амфотерными гидроксидами. Основаниям соответствуют основные оксиды , кислотам – кислотные оксиды, а амфотерным гидроксидам – амфотерные оксиды. Примеры различных по своему химическому поведению оксидов приведены в таблице 9.
Таблица 9.Примеры основных, амфотерных и кислотных оксидов, а также соответствующие им гидроксидов.
Основные |
Амфотерные |
Кислотные |
|||
Гидроксиды |
Гидроксиды |
Гидроксиды |
|||
*)Приведена идеализированная формула
гидроксида
**)Существует только в водном растворе
Соли образуются не только при реакциях кислот с
основаниями, но и при взаимодействии металлов с
кислотами:
Mg + H 2 SO 4 = MgSO 4 + H 2 O,
2Al + 6HCl = 2AlCl 3 + 3H 2 ,
а также при взаимодействии основных оксидов с
кислотными оксидами Li 2 O + CO 2 = Li 2 СО 3 ,
основных оксидов с кислотами FeO + H 2 SO 4 =
FeSO 4 + Н 2 О
и кислотных оксидов с основаниями SO 2 + 2NаОН =
Na 2 SO 3 + H 2 O.
В аналогичные реакции вступают также амфотерные
оксиды и гидроксиды.
А теперь вернемся к знакомому вам делению
веществ на молекулярные и немолекулярные, то
есть к классификации их по типу строения. Как
распределяются молекулярные и немолекулярные
вещества по различным классам сложных веществ,
показано в таблице 10.
Таблица 10. Тип строения некоторых сложных веществ
Класс соединений |
Молекулярное строение |
Немолекулярное строение |
Основные и амфотерные оксиды |
||
Кислотные оксиды |
CO 2 , N 2 O 3 , N 2 O 5 , P 4 O 10 , SO 2 , SO 3 |
B 2 O 3 , SiO 2 , CrO 3 |
Основные и амфотерные гидроксиды |
||
Кислотные гидроксиды (кислоты) |
H 3 BO 3 , H 2 CO 3 , HNO 2 , HNO 3 , H 3 PO 4 , H 2 SO 3 , H 2 SO 4 |
|
CH 4 , NH 3 , H 2 O, H 2 S, HF, HCl |
||
Галогениды |
BF 3 , SiCl 4 , CBr 4 , C 2 I 6 , NCl 3 |
NaF, КС1, СаBr 2 , MgI 2 , BaF 2 |
Как видите, химические вещества – очень разные, разные по составу, по своим физическим характеристикам, разные по химическим свойствам. Но ответить на вопросы, почему данное вещество имеет такой состав, почему оно обладает такими характеристиками, почему оно реагирует именно с этими веществами и как оно с ними реагирует, вы пока не можете. Вспомните, что свойства вещества определяются его составом и строением. Поэтому для ответа на эти вопросы нужно прежде всего изучить, как вещества устроены, то есть – строение вещества.
| Диоксид углерода – CO 2
,
или углекислый газ. Молекулярное вещество,
кислотный оксид. Несмотря на то, что его объемная
доля в земной атмосфере всего 0,03 – 0,04 %,
углекислый газ – один из существеннейших
компонентов воздуха, и его роль в нашей жизни
трудно переоценить. Он непосредственно
участвует в двух важнейших природных процессах:
дыхании и фотосинтезе. Например, за один час
взрослый человек выдыхает около 20 литров
углекислого газа. Повышение его содержания
губительно для человека и животных: при объемной
доле 0,2 – 0,15 % человек теряет сознание.
Атмосферный СО 2 предохраняет нашу планету
от переохлаждения, так как способен удерживать
тепловое излучение, исходящее от поверхности
Земли, но его избыток может вызвать так
называемый " парниковый эффект" . Твердый СО 2
– " сухой лед" – используется для
охлаждения: например, куски льда у продавщицы
мороженого есть не что иное, как " сухой лед" Оксид кальция – CaO , или негашеная (жженая) известь – основный оксид белого цвета, гигроскопичен (поглощает влагу). Это вещество энергично реагирует с водой, образуя "гашеную известь" – гидроксид кальция. Получают этот оксид обжигом различных горных пород, образованных карбонатом кальция, отсюда и название "жженая известь". При попадании на кожу вызывает ожоги. Особенно опасно попадание его в глаза. Гидроксид кальция – Ca(OH) 2 , или гашеная известь, – основание белого цвета, малорастворимое в воде. Получают его так называемым гашением – добавлением воды к оксиду кальция. В реакции выделяется так много тепла, что реакционная смесь вскипает. Гашеную известь используют в строительстве как связующий материал и как сырье для изготовления белого силикатного кирпича, а также в производстве минеральных удобрений. |
ЕСТЕСТВЕННАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ, МЕТАЛЛЫ, НЕМЕТАЛЛЫ, БИНАРНЫЕ СОЕДИНЕНИЯ, КИСЛОРОДНЫЕ СОЕДИНЕНИЯ, ВОДОРОДНЫЕ СОЕДИНЕНИЯ, ГАЛОГЕНИДЫ, ГИДРИДЫ, ОКСИДЫ, ГИДРОКСИДЫ, КИСЛОТЫ, ОСНОВАНИЯ, СОЛИ, ЩЕЛОЧИ, АМФОТЕРНЫЕ ГИДРОКСИДЫ, ИНДИКАТОРЫ, РЕАКЦИЯ НЕЙТРАЛИЗАЦИИ, ОСНОВНЫЕ ОКСИДЫ, КИСЛОТНЫЕ ОКСИДЫ, АМФОТЕРНЫЕ ОКСИДЫ а) Fe(OH) 2 ; б) Pb(OH) 2 ; в) Fe(ОН) 3 ; г) Сr(ОН) 3 .
7.Составьте уравнения реакций по следующим
схемам реакций:
Li 2 O + P 4 O 1 0 Li 3 PO 4 ;
MnSO 4 + NаОН M n(OH) 2 + Na 2 SO 4 ;
Fe 3 O 4 + Al Al 2 O 3
+ Fe; La 2 (SO 4) 3 + KOH La(OH) 3 + K 2 SO 4 ;
Fe 2 O 3 + Mg MgO + Fe;
Ag NO 3 + NaO H Ag 2 O
+NaNO 3 + H 2 O.
К каким классам относятся исходные и конечные
вещества этих реакций?
1. Взаимодействие растворов кислот и оснований с
индикаторами.
2. Химические свойства кислот и оснований.
3. Химические свойства металлов.
4. Химические свойства оксидов.
Достаточно часто школьникам и студентам приходится составлять т. н. ионные уравнения реакций. В частности, именно этой теме посвящена задача 31, предлагаемая на ЕГЭ по химии. В данной статье мы подробно обсудим алгоритм написания кратких и полных ионных уравнений, разберем много примеров разного уровня сложности.
Зачем нужны ионные уравнения
Напомню, что при растворении многих веществ в воде (и не только в воде!) происходит процесс диссоциации - вещества распадаются на ионы. Например, молекулы HCl в водной среде диссоциируют на катионы водорода (H + , точнее, H 3 O +) и анионы хлора (Cl -). Бромид натрия (NaBr) находится в водном растворе не в виде молекул, а в виде гидратированных ионов Na + и Br - (кстати, в твердом бромиде натрия тоже присутствуют ионы).
Записывая "обычные" (молекулярные) уравнения, мы не учитываем, что в реакцию вступают не молекулы, а ионы. Вот, например, как выглядит уравнение реакции между соляной кислотой и гидроксидом натрия:
HCl + NaOH = NaCl + H 2 O. (1)
Разумеется, эта схема не совсем верно описывает процесс. Как мы уже сказали, в водном растворе практически нет молекул HCl, а есть ионы H + и Cl - . Так же обстоят дела и с NaOH. Правильнее было бы записать следующее:
H + + Cl - + Na + + OH - = Na + + Cl - + H 2 O. (2)
Это и есть полное ионное уравнение . Вместо "виртуальных" молекул мы видим частицы, которые реально присутствуют в растворе (катионы и анионы). Не будем пока останавливаться на вопросе, почему H 2 O мы записали в молекулярной форме. Чуть позже это будет объяснено. Как видите, нет ничего сложного: мы заменили молекулы ионами, которые образуются при их диссоциации.
Впрочем, даже полное ионное уравнение не является безупречным. Действительно, присмотритесь повнимательнее: и в левой, и в правой частях уравнения (2) присутствуют одинаковые частицы - катионы Na + и анионы Cl - . В процессе реакции эти ионы не изменяются. Зачем тогда они вообще нужны? Уберем их и получим краткое ионное уравнение:
H + + OH - = H 2 O. (3)
Как видите, все сводится к взаимодействию ионов H + и OH - c образованием воды (реакция нейтрализации).
Все, полное и краткое ионные уравнения записаны. Если бы мы решали задачу 31 на ЕГЭ по химии, то получили бы за нее максимальную оценку - 2 балла.
Итак, еще раз о терминологии:
- HCl + NaOH = NaCl + H 2 O - молекулярное уравнение ("обычное" уравнения, схематично отражающее суть реакции);
- H + + Cl - + Na + + OH - = Na + + Cl - + H 2 O - полное ионное уравнение (видны реальные частицы, находящиеся в растворе);
- H + + OH - = H 2 O - краткое ионное уравнение (мы убрали весь "мусор" - частицы, которые не участвуют в процессе).
Алгоритм написания ионных уравнений
- Составляем молекулярное уравнение реакции.
- Все частицы, диссоциирующие в растворе в ощутимой степени, записываем в виде ионов; вещества, не склонные к диссоциации, оставляем "в виде молекул".
- Убираем из двух частей уравнения т. н. ионы-наблюдатели, т. е. частицы, которые не участвуют в процессе.
- Проверяем коэффициенты и получаем окончательный ответ - краткое ионное уравнение.
Пример 1 . Составьте полное и краткое ионные уравнения, описывающие взаимодействие водных растворов хлорида бария и сульфата натрия.
Решение . Будем действовать в соответствии с предложенным алгоритмом. Составим сначала молекулярное уравнение. Хлорид бария и сульфат натрия - это две соли. Заглянем в раздел справочника "Свойства неорганических соединений" . Видим, что соли могут взаимодействовать друг с другом, если в ходе реакции образуется осадок. Проверим:
Упражнение 2 . Дополните уравнения следующих реакций:
- KOH + H 2 SO 4 =
- H 3 PO 4 + Na 2 O=
- Ba(OH) 2 + CO 2 =
- NaOH + CuBr 2 =
- K 2 S + Hg(NO 3) 2 =
- Zn + FeCl 2 =
Упражнение 3 . Напишите молекулярные уравнения реакций (в водном растворе) между: а) карбонатом натрия и азотной кислотой, б) хлоридом никеля (II) и гидроксидом натрия, в) ортофосфорной кислотой и гидроксидом кальция, г) нитратом серебра и хлоридом калия, д) оксидом фосфора (V) и гидроксидом калия.
Искренне надеюсь, что у вас не возникло проблем с выполнением этих трех заданий. Если это не так, необходимо вернуться к теме "Химические свойства основных классов неорганических соединений".
Как превратить молекулярное уравнение в полное ионное уравнение
Начинается самое интересное. Мы должны понять, какие вещества следует записывать в виде ионов, а какие - оставить в "молекулярной форме". Придется запомнить следующее.
В виде ионов записывают:
- растворимые соли (подчеркиваю, только соли хорошо растворимые в воде);
- щелочи (напомню, что щелочами называют растворимые в воде основания, но не NH 4 OH);
- сильные кислоты (H 2 SO 4 , HNO 3 , HCl, HBr, HI, HClO 4 , HClO 3 , H 2 SeO 4 , ...).
Как видите, запомнить этот список совсем несложно: в него входят сильные кислоты и основания и все растворимые соли. Кстати, особо бдительным юным химикам, которых может возмутить тот факт, что сильные электролиты (нерастворимые соли) не вошли в этот перечень, могу сообщить следующее: НЕвключение нерастворимых солей в данный список вовсе не отвергает того, что они являются сильными электролитами.
Все остальные вещества должны присутствовать в ионных уравнениях в виде молекул. Тем требовательным читателям, которых не устраивает расплывчатый термин "все остальные вещества", и которые, следуя примеру героя известного фильма, требуют "огласить полный список" даю следующую информацию.
В виде молекул записывают:
- все нерастворимые соли;
- все слабые основания (включая нерастворимые гидроксиды, NH 4 OH и сходные с ним вещества);
- все слабые кислоты (H 2 СO 3 , HNO 2 , H 2 S, H 2 SiO 3 , HCN, HClO, практически все органические кислоты...);
- вообще, все слабые электролиты (включая воду!!!);
- оксиды (всех типов);
- все газообразные соединения (в частности, H 2 , CO 2 , SO 2 , H 2 S, CO);
- простые вещества (металлы и неметаллы);
- практически все органические соединения (исключение - растворимые в воде соли органических кислот).
Уф-ф, кажется, я ничего не забыл! Хотя проще, по-моему, все же запомнить список N 1. Из принципиально важного в списке N 2 еще раз отмечу воду.
Давайте тренироваться!
Пример 2 . Составьте полное ионное уравнение, описывающие взаимодействие гидроксида меди (II) и соляной кислоты.
Решение . Начнем, естественно, с молекулярного уравнения. Гидроксид меди (II) - нерастворимое основание. Все нерастворимые основания реагируют с сильными кислотами с образованием соли и воды:
Cu(OH) 2 + 2HCl = CuCl 2 + 2H 2 O.
А теперь выясняем, какие вещества записывать в виде ионов, а какие - в виде молекул. Нам помогут приведенные выше списки. Гидроксид меди (II) - нерастворимое основание (см. таблицу растворимости), слабый электролит. Нерастворимые основания записывают в молекулярной форме. HCl - сильная кислота, в растворе практически полностью диссоциирует на ионы. CuCl 2 - растворимая соль. Записываем в ионной форме. Вода - только в виде молекул! Получаем полное ионное уравнение:
Сu(OH) 2 + 2H + + 2Cl - = Cu 2+ + 2Cl - + 2H 2 O.
Пример 3 . Составьте полное ионное уравнение реакции диоксида углерода с водным раствором NaOH.
Решение . Диоксид углерода - типичный кислотный оксид, NaOH - щелочь. При взаимодействии кислотных оксидов с водными растворами щелочей образуются соль и вода. Составляем молекулярное уравнение реакции (не забывайте, кстати, о коэффициентах):
CO 2 + 2NaOH = Na 2 CO 3 + H 2 O.
CO 2 - оксид, газообразное соединение; сохраняем молекулярную форму. NaOH - сильное основание (щелочь); записываем в виде ионов. Na 2 CO 3 - растворимая соль; пишем в виде ионов. Вода - слабый электролит, практически не диссоциирует; оставляем в молекулярной форме. Получаем следующее:
СO 2 + 2Na + + 2OH - = Na 2+ + CO 3 2- + H 2 O.
Пример 4 . Сульфид натрия в водном растворе реагирует с хлоридом цинка с образованием осадка. Составьте полное ионное уравнение данной реакции.
Решение . Сульфид натрия и хлорид цинка - это соли. При взаимодействии этих солей выпадает осадок сульфида цинка:
Na 2 S + ZnCl 2 = ZnS↓ + 2NaCl.
Я сразу запишу полное ионное уравнение, а вы самостоятельно проанализируете его:
2Na + + S 2- + Zn 2+ + 2Cl - = ZnS↓ + 2Na + + 2Cl - .
Предлагаю вам несколько заданий для самостоятельной работы и небольшой тест.
Упражнение 4 . Составьте молекулярные и полные ионные уравнения следующих реакций:
- NaOH + HNO 3 =
- H 2 SO 4 + MgO =
- Ca(NO 3) 2 + Na 3 PO 4 =
- CoBr 2 + Ca(OH) 2 =
Упражнение 5 . Напишите полные ионные уравнения, описывающие взаимодействие: а) оксида азота (V) с водным раствором гидроксида бария, б) раствора гидроксида цезия с иодоводородной кислотой, в) водных растворов сульфата меди и сульфида калия, г) гидроксида кальция и водного раствора нитрата железа (III).
Поговорим о том, как составить химическое уравнение, ведь именно они являются основными элементами данной дисциплины. Благодаря глубокому осознанию всех закономерностей взаимодействий и веществ, можно управлять ими, применять их в различных сферах деятельности.
Теоретические особенности
Составление химических уравнений - важный и ответственный этап, рассматриваемый в восьмом классе общеобразовательных школ. Что должно предшествовать данному этапу? Прежде чем педагог расскажет своим воспитанникам о том, как составить химическое уравнение, важно познакомить школьников с термином «валентность», научить их определять данную величину у металлов и неметаллов, пользуясь таблицей элементов Менделеева.

Составление бинарных формул по валентности
Для того чтобы понять, как составить химическое уравнение по валентности, для начала нужно научиться составлять формулы соединений, состоящих из двух элементов, пользуясь валентностью. Предлагаем алгоритм, который поможет справиться с поставленной задачей. Например, необходимо составить формулу оксида натрия.
Сначала важно учесть, что тот химический элемент, который в названии упоминается последним, в формуле должен располагаться на первом месте. В нашем случае первым будет записываться в формуле натрий, вторым кислород. Напомним, что оксидами называют бинарные соединения, в которых последним (вторым) элементом обязательно должен быть кислород со степенью окисления -2 (валентностью 2). Далее по таблице Менделеева необходимо определить валентности каждого из двух элементов. Для этого используем определенные правила.
Так как натрий - металл, который располагается в главной подгруппе 1 группы, его валентность является неизменной величиной, она равна I.
Кислород - это неметалл, поскольку в оксиде он стоит последним, для определения его валентности мы из восьми (число групп) вычитаем 6 (группу, в которой находится кислород), получаем, что валентность кислорода равна II.
Между определенными валентностями находим наименьшее общее кратное, затем делим его на валентность каждого из элементов, получаем их индексы. Записываем готовую формулу Na 2 O.

Инструкция по составлению уравнения
А теперь подробнее поговорим о том, как составить химическое уравнение. Сначала рассмотрим теоретические моменты, затем перейдем к конкретным примерам. Итак, составление химических уравнений предполагает определенный порядок действий.
- 1-й этап. Прочитав предложенное задание, необходимо определить, какие именно химические вещества должны присутствовать в левой части уравнения. Между исходными компонентами ставится знак «+».
- 2-й этап. После знака равенства необходимо составить формулу продукта реакции. При выполнении подобных действий потребуется алгоритм составления формул бинарных соединений, рассмотренный нами выше.
- 3-й этап. Проверяем количество атомов каждого элемента до и после химического взаимодействия, в случае необходимости ставим дополнительные коэффициенты перед формулами.

Пример реакции горения
Попробуем разобраться в том, как составить химическое уравнение горения магния, пользуясь алгоритмом. В левой части уравнения записываем через сумму магний и кислород. Не забываем о том, что кислород является двухатомной молекулой, поэтому у него необходимо поставить индекс 2. После знака равенства составляем формулу получаемого после реакции продукта. Им будет в котором первым записан магний, а вторым в формуле поставим кислород. Далее по таблице химических элементов определяем валентности. Магний, находящийся во 2 группе (главной подгруппе), имеет постоянную валентность II, у кислорода путем вычитания 8 - 6 также получаем валентность II.
Запись процесса будет иметь вид: Mg+O 2 =MgO.
Для того чтобы уравнение соответствовало закону сохранения массы веществ, необходимо расставить коэффициенты. Сначала проверяем количество кислорода до реакции, после завершения процесса. Так как было 2 атома кислорода, а образовался всего один, в правой части перед формулой оксида магния необходимо добавить коэффициент 2. Далее считаем число атомов магния до и после процесса. В результате взаимодействия получилось 2 магния, следовательно, в левой части перед простым веществом магнием также необходим коэффициент 2.
Итоговый вид реакции: 2Mg+O 2 =2MgO.
Пример реакции замещения
Любой конспект по химии содержит описание разных видов взаимодействий.
В отличие от соединения, в замещении и в левой, и в правой части уравнения будет два вещества. Допустим, необходимо написать реакцию взаимодействия между цинком и Алгоритм написания используем стандартный. Сначала в левой части через сумму пишем цинк и соляную кислоту, в правой части составляем формулы получаемых продуктов реакции. Так как в электрохимическом ряду напряжений металлов цинк располагается до водорода, в данном процессе он вытесняет из кислоты молекулярный водород, образует хлорид цинка. В результате получаем следующую запись: Zn+HCL=ZnCl 2 +H 2 .
Теперь переходим к уравниванию количества атомов каждого элемента. Так как в левой части хлора был один атом, а после взаимодействия их стало два, перед формулой соляной кислоты необходимо поставить коэффициент 2.
В итоге получаем готовое уравнение реакции, соответствующее закону сохранения массы веществ: Zn+2HCL=ZnCl 2 +H 2 .

Заключение
Типичный конспект по химии обязательно содержит несколько химических превращений. Ни один раздел этой науки не ограничивается простым словесным описанием превращений, процессов растворения, выпаривания, обязательно все подтверждается уравнениями. Специфика химии заключается в том, что с все процессы, которые происходят между разными неорганическими либо органическими веществами, можно описать с помощью коэффициентов, индексов.
Чем еще отличается от других наук химия? Химические уравнения помогают не только описывать происходящие превращения, но и проводить по ним количественные вычисления, благодаря которым можно осуществлять лабораторное и промышленное получение разных веществ.