Еще много веков назад люди догадывались, что любое вещество на земле состоит из микроскопических частиц. Прошло какое-то время, и ученые доказали, что эти частицы действительно существуют. Их назвали атомами. Обычно атомы не могут существовать отдельно и объединяются в группы. Эти группы и называются молекулами.
Само название "молекула" происходит от латинского слова moles, означающего тяжесть, глыбу, громаду, и уменьшительного суффикса - cula. Раньше вместо этого термина употреблялось слово «корпускула», дословно означающее «маленькое тело». Для того чтобы выяснить, что такое молекула, обратимся к толковым словарям. В словаре Ушакова говорится, что это мельчайшая частица, которая может существовать автономно и обладает всеми свойствами вещества, к которому она относится. Молекулы и атомы окружают нас повсюду, и хоть их нельзя пощупать, все, что мы видим, на самом деле - это их гигантские скопления.
Пример с водой
Лучше всего объяснить, что такое молекула, можно на примере стакана с водой. Если отлить из него половину, то вкус, цвет и состав оставшейся воды не изменится. Было бы странно ожидать чего-то другого. Если снова отлить половину, количество уменьшится, но свойства опять останутся теми же. Продолжая в том же духе, мы в итоге получим маленькую капельку. Ее еще можно поделить пипеткой, но до бесконечности продолжать этот процесс не получится.

В конечном счете получится мельчайшая частица, остаток от деления которой водой уже не будет. Для того чтобы представить себе, что такое молекула и насколько она мала, попробуйте угадать, сколько молекул находится в одной капельке воды. Как вы думаете? Миллиард? Сто миллиардов? На самом деле их там примерно сто секстильонов. Это число, у которого после единицы идет двадцать три нуля. Такую величину сложно себе представить, поэтому воспользуемся сравнением: размер одной меньше крупного яблока во столько раз, во сколько само яблоко меньше Поэтому ее нельзя увидеть даже в самый мощный оптический микроскоп.
и атомов
Как мы уже знаем, все микроскопические частицы в свою очередь состоят из атомов. В зависимости от их количества, орбит центральных атомов и типа связей геометрическая форма молекул может быть различной. К примеру, человеческая ДНК закручена в форме спирали, а мельчайшая частица обычной поваренной соли имеет вид Если у молекулы каким-то образом забрать несколько атомов, произойдет ее разрушение. При этом последние никуда не денутся, а войдут в состав другой микрочастицы.
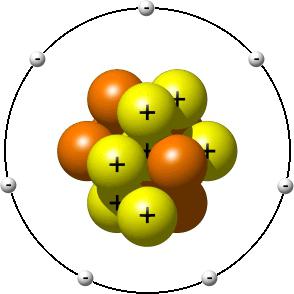
После того как мы разобрались, что такое молекула, перейдем к атому. Его структура очень напоминает планетарную систему: в центре находится ядро с нейтронами и положительно заряженными протонами, а вокруг на разных орбитах вращаются электроны. В целом атом электронейтрален. Другими словами, число электронов равно числу протонов.
Надеемся, наша статья оказалась полезной, и теперь у вас больше нет вопросов о том, что такое молекула и атом, как они устроены и чем отличаются.
Чем отличаются атомы?

В переводе «атом» означает неделимый. Назван он так потому, что долгое время его считали наименьшей частью вещества. Но дальнейшее развитие науки показало, что это не так. Итак, давайте разберемся, из чего состоит атом и чем отличаются атомы различных элементов.
Строение атома
На сегодняшний день науке известно 126 видов химических элементов. Общий план строения их атомов одинаков. Каждый из них имеет ядро, состоящее из протонов и нейтронов, вокруг которого вращаются электроны. Электроны - это негативно заряженные частицы. При их вращении вокруг ядра образуется электронное облако.
Протоны - это позитивно заряженные частицы. В состоянии покоя в атоме содержится одинаковое количество протонов и электронов, поэтому такой химический элемент не имеет электрического заряда. Однако, в процессе реакций он может отдавать электрон другим элементам, превращаясь в позитивно заряженную частицу, или забирать их, становясь отрицательно заряженной частицей. Нейтроны никакого заряда не несут, но влияют на массу элемента. Для протонов и нейтронов придумано объединяющее название - нуклоны.
Атомы различных элементов
Атомы различных элементов отличаются друг от друга количеством протонов в ядре. Количество электронов может меняться, а протонов - никогда. Сколько протонов содержится в ядре, можно узнать по порядковому номеру элемента в периодической системе Менделеева. У водорода (№1) в состоянии покоя 1 электрон и 1 протон, у лития  (№3) - 3 электрона и 3 протона, у углерода (№6) - 6 электронов и 6 протонов.
(№3) - 3 электрона и 3 протона, у углерода (№6) - 6 электронов и 6 протонов.
Поскольку количество протонов у различных атомов разное, массы у них тоже отличаются. Масса элемента в основном формируется протонами и нейтронами, ведь вес электронов ничтожно мал. Но даже у атомов одного и того же элемента вес может отличаться из-за разного количества нейтронов в ядре. Атомы, у которых количество нейтронов отличается от количества протонов, называют изотопами. Например, в природе существуют атомы углерода С12 (6 протонов и 6 нейтронов), С13 (6 протонов и 7 нейтронов) и другие разновидности с содержанием нейтронов от 2 до 16.
Атом вещь (Garg и др 2014.); элемент - это тип вещи.
Атом представляет собой набор протонов, нейтронов и электронов. Один изолированный атом в нейтральном состоянии имеет некоторое количество протонов, такое же количество электронов и некоторое число нейтронов (примерно столько же, сколько протонов для более легких элементов, что примерно на 50% больше, для более тяжелых элементов). Число нейтронов или протонов в атоме изменяется только в результате радиоактивных процессов или очень высокоэнергетических взаимодействий, таких как вы получаете в ускорителях частиц. И я имею в виду действительно высокая энергия: даже если вы думаете о раздувании палочек динамита, это не достаточно энергии, чтобы начать возиться с протонами и нейтронами. Химия происходит, когда атомы объединяются и обмениваются электронами или дают электроны друг другу. Химические реакции происходят все время, и многие из них не нуждаются в большой энергии: перемещение электронов с атома на атом часто очень просто.
Итак, химия атома зависит от числа электронов, а число электронов в изолированном атоме напрямую зависит от числа протонов. Электроны настолько легко добавлять и удалять из атомов (просто натереть воздушный шар на волосы: статическое электричество - это то, что вы переводили электроны между вашими волосами и воздушным шаром), поэтому мы классифицируем атомы в соответствии с количеством протонов в них. Нейтроны не так актуальны: я расскажу о них в конце.
Таким образом, элемент атома определяется числом протонов. Все атомы водорода имеют один протон, и все атомы с одним протоном являются водородом. Два протона - это гелий, три - литий, семнадцать - хлор, 79 - золото и т. Д. Чистый образец элемента содержит только атомы такого типа: например, чистый образец железа содержит только атомы с 26 протонами. С другой стороны, вода не является элементом: молекула воды состоит из двух атомов водорода (по одному протону), разделяющих электроны с атомом кислорода (восемь протонов).
Теперь, что значит утверждать, что элемент «нельзя разбить на более простую форму» и почему атомы не являются «более простой формой»? Ну, они не более простая форма, потому что атом железа - железо: это та же форма, что не проще. Подумайте об этом так. Если я дам вам кусок чистого железа, все, что вы можете сделать, это разбить его на более мелкие куски железа или сделать его более сложным веществом, например, разрешив ему ржавчину. - ржавчина образована из железа и кислорода. Самый маленький возможный кусок железа, который вы могли бы сделать, - это единственный атом железа, но это все еще просто невероятно крошечный кусок железа. Если бы вы хотели сломать кусок железа за пределы отдельных атомов железа, вам нужно будет использовать ядерный реактор или ускоритель частиц или что-то в этом роде, а затем, наконец, вы сможете получить то, что не было железом, потому что вы бы изменили количество протонов в атомах.
Давайте сравним это с водой. Если я дам вам ведро с чистой водой, то, подобно куску железа, вы можете разделить его на более мелкие и мелкие образцы, в конечном итоге получив единственную молекулу воды. Но вы можете сделать что-то еще: если вы пропускаете электричество через воду, он расщепляется на чистый водород и чистый кислород. Это «более простые» вещества, потому что каждый состоит из атомов только одного элемента, тогда как вода имеет атомы двух элементов.
Что относительно нейтронов? Ну, с точки зрения химии, они не делают много, а атомы с таким же числом протонов, но с различным числом нейтронов, гораздо более похожи (они имеют, по существу, одну и ту же химию, например), чем атомы, имеющие одинаковые число нейтронов, но различное количество протонов. Гораздо более целесообразно классифицировать по числу протонов, поскольку это определяет количество электронов и определяет химию.
Предположим, вы попытались классифицировать атомы в соответствии с количеством нейтронов.Наилучшим образом, большинство атомов аргона (18 протонов) имеют 22 нейтрона, но некоторые атомы хлора (17 протонов) и приличная доля атомов калия (19 протонов) также имеют 22 нейтрона. Как вы, наверное, знаете, аргон, хлор и калий абсолютно ничем не похожи друг на друга. С другой стороны, атомы калия с 22 нейтронами ведут себя почти одинаково с наиболее распространенным видом атомов калия, которые имеют 21 нейтрон.
Чем отличаются понятия "атом" и "молекула"? и получил лучший ответ
Ответ от Sunrise[эксперт]
атом меньше, в одной молекуле может быть несколько атомов (пример - 2 атома водорода и один атом кислорода= молекула воды)
Ответ от Диана Мамина
[гуру]
Молекула состоит из атомов.
Ответ от НЕТ
[гуру]
Кроме общих мест, ещё и родом.
Ответ от Воздушная
[новичек]
атом, это электронейтральная система взаимодействубщих элементов, состоящая из ядра и электронов. , а молекула - это соединение, состоящее из 2х или более атомов
Ответ от Durchlaucht Furst
[гуру]
А́том (др. -греч. ἄτομος - неделимый) - наименьшая часть химического элемента, являющаяся носителем его свойств. Атом состоит из атомного ядра и окружающего его электронного облака. Ядро атома состоит из положительно заряженных протонов и электрически нейтральных нейтронов, а окружающее его облако состоит из отрицательно заряженных электронов. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. Атомы классифицируются по количеству протонов и нейтронов в ядре: количество протонов определяет принадлежность атома некоторому химическому элементу, а число нейтронов - изотопу этого элемента.
Атомы различного вида в различных количествах, связанные межатомными связями, образуют молекулы.
Понятие об атоме как о наименьшей неделимой части материи было впервые сформулировано древнеиндийскими и древнегреческими философами (см. : атомизм). В XVII и XVIII веках химикам удалось экспериментально подтвердить эту идею, показав, что некоторые вещества не могут быть подвергнуты дальнейшему расщеплению на составляющие элементы с помощью химических методов. Однако в конце XIX - начале XX века физиками были открыты субатомные частицы и составная структура атома, и стало ясно, что атом в действительности не является «неделимым».
Моле́кула (новолатинское molecula, уменьшительное от лат. moles - масса) - наименьшая частица вещества, несущая его химические свойства.
Молекула состоит из двух или более атомов, характеризуется количеством входящих в неё атомных ядер и электронов, а также определённой структурой.
Обычно подразумевается, что молекулы нейтральны (не несут электрических зарядов) и не несут неспаренных электронов (все валентности насыщены) ; заряженные молекулы называют ионами, молекулы с мультиплетностью, отличной от единицы (т. е. с неспаренными электронами и ненасыщенными валентностями) - радикалами.
Молекулы, образованные сотнями или тысячами атомов, называются макромолекулами. Особенности строения молекул определяют физические свойства вещества, состоящего из этих молекул.
Ответ от Мариям Абдулла
[новичек]
еще у атомов электрический заряд, тогда как молекула нейтральна
Ответ от Мурват Казымов
[новичек]
атом это то из чего состоит молекула
В переводе «атом» означает неделимый. Назван он так потому, что долгое время его считали наименьшей частью вещества. Но дальнейшее развитие науки показало, что это не так. Итак, давайте разберемся, из чего состоит атом и чем отличаются атомы различных элементов.
Строение атома
На сегодняшний день науке известно 126 видов химических элементов. Общий план строения их атомов одинаков. Каждый из них имеет ядро, состоящее из протонов и нейтронов, вокруг которого вращаются электроны. Электроны - это негативно заряженные частицы. При их вращении вокруг ядра образуется электронное облако.
Протоны - это позитивно заряженные частицы. В состоянии покоя в атоме содержится одинаковое количество протонов и электронов, поэтому такой химический элемент не имеет электрического заряда. Однако, в процессе реакций он может отдавать электрон другим элементам, превращаясь в позитивно заряженную частицу, или забирать их, становясь отрицательно заряженной частицей. Нейтроны никакого заряда не несут, но влияют на массу элемента. Для протонов и нейтронов придумано объединяющее название - нуклоны.
Атомы различных элементов
Атомы различных элементов отличаются друг от друга количеством протонов в ядре. Количество электронов может меняться, а протонов - никогда. Сколько протонов содержится в ядре, можно узнать по порядковому номеру элемента в периодической системе Менделеева. У водорода (№1) в состоянии покоя 1 электрон и 1 протон, у лития  (№3) - 3 электрона и 3 протона, у углерода (№6) - 6 электронов и 6 протонов.
(№3) - 3 электрона и 3 протона, у углерода (№6) - 6 электронов и 6 протонов.
Поскольку количество протонов у различных атомов разное, массы у них тоже отличаются. Масса элемента в основном формируется протонами и нейтронами, ведь вес электронов ничтожно мал. Но даже у атомов одного и того же элемента вес может отличаться из-за разного количества нейтронов в ядре. Атомы, у которых количество нейтронов отличается от количества протонов, называют изотопами. Например, в природе существуют атомы углерода С12 (6 протонов и 6 нейтронов), С13 (6 протонов и 7 нейтронов) и другие разновидности с содержанием нейтронов от 2 до 16.
Внимание, только СЕГОДНЯ!
ДРУГОЕ
Иностранное слово «альфа» прочно прижилось в русском языке и встречается в самых разных сочетаниях. О том,…
Безусловно, каждый из нас в самом общем смысле хорошо представляет, что такое элемент. Элемент - это составная часть…
Слово "ядро" означает сердцевину чего-либо, имеющую форму шара. Однако значения у данного понятия могут быть разными, в…
Каждый из нас хоть раз, но любовался прекрасным ночным небом, усыпанным множеством звёзд. Не задумывались ли вы о том,…
Определение большого адронного коллайдера звучит так: БАК является ускорителем заряженных частиц, и создан он с целью…
Электрон - это элементарная частица, которая имеет отрицательный электрический заряд. Он равен -1. Электрон входит в…
Существует невидимая сила, которая протекает внутри биологических объектов и неживой среды. Эта сила называется…
Не так много людей хорошо разбираются в различных терминах, теориях и законах физики и химии. А некоторые, может быть,…
Реакции между разного рода химическими веществами и элементами являются одним из главных предметов изучения в химии.…
Понятие вещества изучается сразу несколькими науками. Вопрос о том, какие есть вещества, мы разберём с двух точек…
На уроках химии в школе учат решать различные задачи, популярными среди которых являются задачи на вычисление…
Электрический заряд – физическая величина, которая определяет способность тела принимать участие в электромагнитных…
Степень окисления – это условный заряд атома в молекуле, он получает атом в результате полного принятия электронов, его…