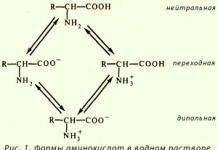
Тема урока: Сложные эфиры. Состав. Номенклатура. Свойства. Применение.
Цели урока :
Рассмотреть состав и строение простейших сложных эфиров, сущность реакции этерификации.
Создать условия для развития умений самостоятельно приобретать знания, используя различные
источники информации.
Способствовать: 1. формированию опыта творческой деятельности, опыта делового общения.
2. развитию творческого мышления, памяти, внимания, наблюдательности.
Продолжить формировать умения учащихся самостоятельно анализировать, корректировать и
оценивать знания;
Важнейшая задача учителя состоит в том, чтобы поддерживать и направлять учащихся, не давать готовые знания, а учит добывать их из различных источников.
Тип урока : Урок изучения нового материала с элементами исследования и использованием презентации по данной теме.
Форма организации познавательной деятельности : работа в группах с использованием ИКТ.
На столе учителя: мыло разных видов, духи, лаки, цветы (герань, фиалки), свежие фрукты: лимон, апельсин, мандарин, масло бергамота, лаванды и др.
Эпиграф урока :
В аромате есть убедительность, которая сильнее слов, очевидности, чувства и воли. Убедительность аромата неопровержима, необорима, она входит в нас подобно тому, как входит в наши лёгкие воздух, которым мы дышим, она наполняет, заполняет нас до отказа. Против неё нет средства. Патрик Зюскинд. «Парфюмер»(Слайд 1)(Слайд2)
Ход урока :
Вступительное слово учителя (мотивация на изучаемую тему)
Действительно, приятные ароматы способны не просто доставить нам удовольствие, а стать причиной хорошего настроения, повысить работоспособность, они могут понижать кровеносное давление и повышать температуру кожи. Когда в орган обоняния человека попадает неприятный запах, человек непроизвольно задерживает свое дыхание, стараясь по возможности вдохнуть как можно меньше неприятного воздуха. Нежелательный запах снижать работоспособность и значительно угнетать человека. (Обращаю внимание учащихся на предметы, находящиеся на столе учителя.)Все они обладают запахами. Какие же вещества являются причиной разнообразных запахов? В основном это - сложные эфиры.(Объявляется тема урока)(Слайд3)
Опрос :
Задание1 (на 4 мин), затем контроль ответов учащихся у доски.(Слайд 4)
1 группа : Записать общую формулу предельных одноатомных спиртов. Привести примеры четырех любых спиртов;дать им название по международной и тривиальной номенклатуре.
С n Н2 n +2 О или С n Н2 n +1 ОН R - OH СН3ОН - метанол, метиловій спирт, С2 Н5ОН-этанол, этиловый спирт
С3 Н7ОН - пропанол, пропиловый спирт С4 Н9ОН - бутанол, бутиловый спирт
2 группа : Записать общую формулу предельных одноосновных карбоновых кислот, привести примеры четырех любых карбоновых кислот; дать им название по международной и тривиальной номенклатуре. С n Н2 n О R - CO - OH H-CO-OH метановая. муравьиная,
СH3 - CO-OH этановая, уксусная. СH3 - СН2 - CO-OH пропановая, пропионовая
СH3 - СН2 - СН2 - CO-OH бутановая, масляная.
3 группа : составить уравнение взаимодействия метанола с муравьиной и уксусной карбоновыми кислотами, дать название образовавшимся орг. веществам.
Изучение нового материала: Прошу вспомнить название реакции взаимодействия карбоновой кислоты со спиртом (по материалам предыдущих уроков) и какое вещество образуется в результате этого взаимодействия.
Данная реакция называется реакцией этерификации(Слайд 5)
R-CO-OH + HO-R1 ↔ RCO-OR1 + H2O
Общая формула сложных эфиров
|
R-C –O-R |
С n H2nO2 |
Вопрос: Какой класс органических соединений имеет такую же общую формулу? (предельные одноосновные карбоновые кислоты)
Предлагаю учащимся записать в тетрадь определения сложным эфирам (Слайд 6)
Сложные эфиры - это вещества, образующиеся в результате реакции дегидратации карбоновых кислот и спиртов.
Сложными эфирами называются органические вещества, которые имеют общую формулу RCOOR1.
Сложными эфирами называются органические вещества, которые содержат функциональную группу атомов – СОО - ,соединённую с двумя углеводородными радикалами.
Задаю вопрос: А как называют сложные эфиры по международной номенклатуре? (Слайд 7)
По международной номенклатуре названия сложным эфирам дается так: к названию предельного углеводородного радикала в спирте добавляется название соответствующей кислоты, в которой окончание - вая заменяется на суффикс – ат.
Задание 2
Группы1 и 2: Записать в таблице названия эфиров по международной номенклатуре по предложенным формулам (распечатаны в файлах) .(Слайд 8)
Формула эфира | Название эфира |
||
С4Н9-СОО-С5Н11 С3Н7- СОО-С2Н5 СН3-СН(СН3)-СН2СОО- С2Н5 СН3-СОО - С2Н5 Н – СОО – С2Н5 | Апельсиновый Абрикосовый Яблочный Грушевый Вишнёвый |
Группа 3: По названиям составить формулы сложных эфиров
Формула эфира | Название эфира |
||
Грушевый Вишнёвый Абрикосовый Апельсиновый Яблочный | Этилэтанат Этилметанат Этилбутанат Пентилтентанат Этил,3-метилбутанат |
Учащиеся сверяют данные таблицы на слайде с записями в тетради, исправляют ошибки(Слайд9)
Задание3 (использование таблицы) (слайд 10)
1гр. Составить уравнение реакции этерификации получения эфира - с вишневым ароматом.
1.Н-СООН + С2Н5ОН ↔ Н - СООС2Н5 + Н2О
2 гр. Составить уравнение реакции этерификации получения эфира с грушевым ароматом.
2.СН3 - СООН + С2Н5ОН ↔ Н - СООС2Н5 + Н2О
3 гр Составить уравнение реакции этерификации получения эфира с яблочным ароматом.
3. СН3-СН(СН3)-СН2СООН + НО - С2Н5↔ СН3-СН(СН3)-СН2СОО- С2Н5+ Н2О
Виды изомерии сложных эфиров: (Слайд 11)
1. Углеродного скелета
2. Межклассовая (предельные одноосновные карбоновые кислоты)
Задание4 (Слайд 12)
С5Н10О2 |
1гр. Составить 2 формулы изомеров с различным углеродным скелетом и назвать их по МН.
2гр. Составить 2 формулы изомеров из различных классов и назвать их по МН.
3гр. Составить по одной формуле изомеров с различным углеродным скелетом и из класса карбоновых кислот и назвать их по МН.
Физические свойства сложных эфиров (Слайд13)
Сложные эфиры – жидкости, легче воды, летучие, обладающие приятным запахом в большинстве случаев, t°кип. и t° пл. ниже, чем t°кип. и t°пл. исходных карбоновых кислот, в воде плохо растворимы, за исключением эфиров с меньшим содержанием атомов углерода, хорошо растворимы в спиртах.
Химические свойства сложных эфиров(Слайд14)
Реакция этерификации протекает очень медленно и, как правило, не до конца т. к. происходит гидролиз сложных эфиров (омыление), при этом образуются вновь исходные вещества – спирт и кислота. Омыление проходит гораздо быстрее, если реакция проходит в щелочной среде.
RCO-OR1 + H2O ↔ R-CO-OH + HO-R1
Например:
Н - СООС2Н5 + Н2О ↔ Н-СООН + С2Н5ОН
Элемент исследования на уроке
Задание 5 (Слайд15)
С помощью предложенной информации (файлы с материалами на столах) подготовить небольшие сообщения по группам:
1 гр. Из чего сделаны духи?
2 гр. Сложные эфиры в лекарственных растениях
3 гр. Что такое воск?
Проверочный тест на закрепление изученного материала (Слайд16)
1. Общая формула сложных эфиров:
А)CnH2nO Б)CnH2nO2 В)CnH2n+2O Г) CnH2n
2. Cложные эфиры - это продукт взаимодействия:
1. Карбоновых кислот и альдегидов
2. Спиртов и альдегидов
3. Карбоновых кислот и спиртов
4. Спиртов и простых эфиров
3 .В результате какой реакции образуются сложные эфиры?:
1. Этерификации
2. Полимеризации
3. Поликонденсации
4. Гидролиза
А
Домашнее задание: §21 стр190-192 №1,2,3.стр195(схему 5 в тетрадь)
Номенклатура
Названия сложных эфиров производят от названия, углеводородного радикал а и названия кислоты, в котором вместо окончания "-овая кислота" используют суффикс "ат" (как и в названиях неорганических солей: карбонат натрия, нитрат хрома), например:

(Фрагменты молекул и соответствующие им фрагменты названий выделены одинаковым цветом.)
Сложные эфиры обычно рассматривают как продукты реакции между кислотой и спиртом, например, бутилпропионат можно воспринимать как результат взаимодействия пропионовой кислоты и бутанола.
Если используют тривиальное название исходной кислоты, то в название соединения включают слово «эфир» , например, С 3 Н 7 СООС 5 Н 11 – амиловый эфир масляной кислоты.
Гомологческий ряд

Изомерия
Для сложных эфиров характерны три вида изомерии:
1. Изомерия углеродной цепи, начинается по кислотному остатку с бутановой кислоты, по спиртовому остатку - с пропилового спирта, например:
2. Изомерия положения сложноэфирной группировки -СО-О- . Этот вид изомерии начинается со сложных эфиров, в молекулах которых содержится не менее 4 атомов углерода, например:
3. Межклассовая изомерия, сложные эфиры (алкилалканоаты) изомерны предельным монокарбоновым кислотам; например:
Для сложных эфиров, содержащих непредельную кислоту или непредельный спирт, возможны еще два вида изомерии: изомерия положения кратной связи; цис-транс-изомерия.
Физические свойства
Сложные эфиры низших гомологов кислот и спиртов - бесцветные легкокипящие жидкости с приятным запахом; используются как ароматические добавки к пищевым продуктам и в парфюмерии. В воде сложные эфиры растворяются плохо.
Способы получения
1. Извлечение из природных продуктов
2. Взаимодействие кислот со спиртами (реакции этерификации); например:

Химические свойства
1. Наиболее характерны для сложных эфиров реакции кислотного или щелочного гидролиза (омыление). Это реакции, обратные реакциям этерификации. Например:

2. Восстановление (гидрирование) сложных зфиров, в результате которого образуются спирты (один или два); например:

Важнейшими представителями сложных эфиров являются жиры.
Жиры, масла
Жиры – это сложные эфиры глицерина и высших одноатомных . Общее название таких соединений – триглицериды или триацилглицерины, где ацил – остаток карбоновой кислоты -C(O)R. В состав природных триглицеридов входят остатки насыщенных кислот (пальмитиновой C 15 H 31 COOH, стеариновой C 17 H 35 COOH) и ненасыщенных (олеиновой C 17 H 33 COOH, линолевой C 17 H 31 COOH). Высшие карбоновые кислоты, которые входят в состав жиров имеют всегда четное количество атомов углерода (С 8 – С 18) и неразветвленный углеводородный остаток. Природные жиры и масла – это смеси глицеридов высших карбоновых кислот.
Состав и строение жиров могут быть отражены общей формулой:

Этерификация — реакция образования сложных эфиров.

В состав жиров могут входить остатки как предельных, так и непредельных карбоновых кислот в различных сочетаниях.
В обычных условиях жиры, содержащие в своем составе остатки непредельных кислот, чаще всего бывают жидкими. Их называют маслами
. В основном, это жиры растительного происхождения — льняное, конопляное, подсолнечное и другие масла (исключения пальмовое и кокосовое масла – твердые в обычных условиях). Реже встречаются жидкие жиры животного происхождения, например рыбий жир. Большинство природных жиров животного происхождения при обычных условиях – твердые (легкоплавкие) вещества и содержат в основном остатки предельных карбоновых кислот, например бараний жир.
Состав жиров определяет их физические и химические свойства.
Физические свойства жиров
Жиры нерастворимы в воде, не имеют четкой температуры плавления и значительно увеличиваются в объеме при плавлении.
Агрегатное состояние жиров твердое, это связано с тем, что в состав жиров входят остатки предельных кислот и молекулы жиров способны к плотной упаковке. В состав масел, входят остатки непредельных кислот в cis – конфигурации, следовательно плотная упаковка молекул невозможна, и агрегатное состояние – жидкое.
Химические свойства жиров
Жиры (масла) являются сложными эфирами и для них характерны реакции сложных эфиров.
Понятно, что для жиров, содержащих остатки ненасыщенных карбоновых кислот, характерны все реакции непредельных соединений. Они обесцвечивают бромную воду, вступают в другие реакции присоединения. Наиболее важная в практическом плане реакция – гидрирование жиров. Гидрированием жидких жиров получают твердые сложные эфиры. Именно эта реакция лежит в основе получения маргарина — твердого жира из растительных масел. Условно этот процесс можно описать уравнением реакции:

Все жиры, как и другие сложные эфиры, подвергаются гидролизу:

Гидролиз сложных эфиров- обратимая реакция. Чтобы в сторону образования продуктов гидролиза, его проводят в щелочной среде (в присутствие щелочей или Na 2 CO 3). В этих условиях гидролиз жиров протекает обратимо, и приводит к образованию солей карбоновых кислот, которые называются . жиров в щелочной среде называют омылением жиров .
При омылении жиров образуются глицерин и мыла – натриевые и калиевые соли высших карбоновых кислот:
Омыление – щелочной гидролиз жиров, получение мыла.

Мыла – смеси натриевых (калиевых) солей высших предельных карбоновых кислот (натриевое мыло – твердое, калиевое — жидкое).
Мыла являются поверхностно-активными веществами (сокращенно: ПАВами, детергентами). Моющее действие мыла связано с тем, что мыла эмульгируют жиры. Мыла образуют мицеллы с загрязняющими веществами (условно — это жиры с различными включениями).
Липофильная часть молекулы мыла растворяется в загрязняющем веществе, а гидрофильная часть оказывается на поверхности мицеллы. Мицеллы заряжены одноименно, следовательно отталкиваются, при этом загрязняющее вещество и вода превращается в эмульсию (практически – это грязная вода).

В воде также происходит мыла, при этом создается щелочная среда.
Мыла нельзя использовать в жесткой и морской воде, так как образующиеся при этом стеараты кальция (магния) в воде нерастворимы.

Введение -3-
1. Строение -4-
2. Номенклатура и изомерия -6-
3. Физические свойства и нахождение в природе -7-
4. Химические свойства -8-
5. Получение -9-
6. Применение -10-
6.1 Применение сложных эфиров неорганических кислот -10-
6.2 Применение сложных эфиров органических кислот -12-
Заключение -14-
Использованные источники информации -15-
Приложение -16-
Введение
Среди функциональных производных кислот особое место занимают сложные эфиры - производные кислот, у которых кислотный водород заменён на алкильные (или вообще углеводородные) радикалы.
Сложные эфиры делятся в зависимости от того, производной какой кислоты они являются (неорганической или карбоновой).
Среди сложных эфиров особое место занимают природные эфиры - жиры и масла, которые образованы трехатомным спиртом глицерином и высшими жирными кислотами, содержащими четное число углеродных атомов. Жиры входят в состав растительных и животных организмов и служат одним из источников энергии живых организмов, которая выделяется при окислении жиров.
Цель моей работы заключается в подробном ознакомлении с таким классом органических соединений, как сложные эфиры и углублённом рассмотрении области применения отдельных представителей этого класса.
1. Строение
Общая формула сложных эфиров карбоновых кислот:
где R и R" - углеводородные радикалы (в сложных эфиpax муравьиной кислоты R - атом водорода).
Общая формула жиров:

гдеR", R", R"" - углеродные радикалы.
Жиры бывают “простыми” и “смешанными”. В состав простых жиров входят остатки одинаковых кислот (т. е. R’ = R" = R""), в состав смешанных - различных.
В жирах наиболее часто встречаются следующие жирные кислоты:
Алкановые кислоты
1. Масляная кислота СН 3 - (CH 2) 2 - СООН
3. Пальмитиновая кислота СН 3 - (CH 2) 14 - СООН
4. Стеариновая кислота СН 3 - (CH 2) 16 - СООН
Алкеновые кислоты
5. Олеиновая кислота С 17 Н 33 СООН
СН 3 -(СН 2) 7 -СН === СН-(СН 2) 7 -СООН
Алкадиеновые кислоты
6. Линолевая кислота С 17 Н 31 СООН
СН 3 -(СН 2) 4 -СН = СН-СН 2 -СН = СН-СООН
Алкатриеновые кислоты
7. Линоленовая кислота С 17 Н 29 СООН
СН 3 СН 2 СН = CHCH 2 CH == CHCH 2 CH = СН(СН 2) 4 СООН
2. Номенклатура и изомерия
Названия сложных эфиров производят от названия углеводородного радикала и названия кислоты, в котором вместо окончания -овая используют суффикс - ат, например:
Для сложных эфиров характерны следующие виды изомерии:
1. Изомерия углеродной цепи начинается по кислотному остатку с бутановой кислоты, по спиртовому остатку - с пропилового спирта, например, этилбутирату изомерны этилизобутират, пропилацетат и изопропилацетат.
2. Изомерия положения сложноэфирной группировки -СО-О-. Этот вид изомерии начинаетсясо сложных эфиров, в молекулах которых содержится не менее 4 атомов углерода, например этилацетат и метилпропионат.
3. Межклассовая изомерия, например, метилацетату изомерна пропановая кислота.
Для сложных эфиров, содержащих непредельную кислоту или непредельный спирт, возможны еще два вида изомерии: изомерия положения кратной связи и цис-, транс-изомерия.
3. Физические свойства и нахождение в природе
Сложные эфиры низших карбоновых кислот и спиртов представляют собой летучие, нерастворимые в воде жидкости. Многие из них имеют приятный запах. Так, например, бутилбутират имеет запах ананаса, изоамилацетат - груши и т. д.
Сложные эфиры высших жирных кислот и спиртов - воскообразные вещества, не имеют запаха, в воде не растворимы.
Приятный аромат цветов, плодов, ягод в значительной степени обусловлен присутствием в них тех или иных сложных эфиров.
Жиры широко распространены в природе. Наряду с углеводородами и белками они входят в состав всех растительных и животных организмов и составляют одну из основных частей нашей пищи.
По агрегатному состоянию при комнатной температуре жиры делятся на жидкие и твердые. Твердые жиры, как правило, образованы предельными кислотами, жидкие жиры (их часто называют маслами) - непредельными. Жиры растворимы в органических растворителях и нерастворимы в воде.
4. Химические свойства
1. Реакция гидролиза, или омыления. Так, как реакция этерификации является обратимой, поэтому в присутствии кислот протекает обратная реакция гидролиза:
Реакция гидролиза катализируется и щелочами; в этом случае гидролиз необратим, так как получающаяся кислота со щелочью образует соль:
2. Реакция присоединения. Сложные эфиры, имеющие в своем составе непредельную кислоту или спирт, способны к реакциям присоединения.
3. Реакция восстановления. Восстановление сложных эфиров водородом приводит к образованию двух спиртов:
4. Реакция образования амидов. Под действием аммиака сложные эфиры превращаются в амиды кислот и спирты:
5. Получение
1. Реакция этерификации:
Спирты вступают в реакции с минеральными и органическими кислотами, образуя сложные эфиры. Реакция обратима (обратный процесс – гидролиз сложных эфиров).

Реакционная способность одноатомных спиртов в этих реакциях убывает от первичных к третичным.
2. Взаимодействием ангидридов кислот со спиртами:

3. Взаимодействием галоидангидридов кислот со спиртами:

6. Применение
6.1 Применение сложных эфиров неорганических кислот
Эфиры борной кислоты - триалкилбораты - легко получаются нагреванием спирта и борной кислоты с добавкой концентрированной серной кислоты. Борнометиловый эфир (триметилборат) кипит при 65° С, борноэтиловый (триэтилборат) - при 119° С. Эфиры борной кислоты легко гидролизуются водой.
Реакция с борной кислотой служит для установления конфигурации многоатомных спиртов и была неоднократно использована при изучении Сахаров.
Ортокремневые эфиры - жидкости. Метиловый эфир кипит при 122° С, этиловый при 156° С. Гидролиз водой проходит легко уже на холоду, но идет постепенно и при недостатке воды приводит к образованию высокомолекулярных ангидридных форм, в которых атомы кремния соединены друг с другом через кислород (силоксановые группировки):
Эти высокомолекулярные вещества (полиалкоксисилоксаны) находят применение в качестве связующих, выдерживающих довольно высокую температуру, в частности для покрытия поверхности форм для точной отливки металла.Аналогично SiCl 4 реагируют диалкилдихлорсиланы, например ((СН 3) 2 SiCl 2 , образуя диалкоксильные производные:
Их гидролиз при недостатке воды дает так называемые полиалкилсилоксаны:
Они обладают разным (но очень значительным) молекулярным весом и представляют собой вязкие жидкости, используемые в качестве термостойких смазок, а при еще более длинных силоксановых скелетах - термостойкие электроизоляционные смолы и каучуки.
Эфиры ортотитановой кислоты. Их получают аналогично ортокремневым эфирам по реакции:
Это жидкости, легко гидролизующиеся до метилового спирта и TiO 2 применяются для пропитки тканей с целью придания им водонепроницаемости.
Эфиры азотной кислоты. Их получают действием на спирты смеси азотной и концентрированной серной кислот. Метилнитрат СН 3 ONO 2 , (т. кип. 60° С) и этилнитрат C 2 H 5 ONO 2 (т. кип. 87° С) при осторожной работе можно перегнать, но при нагревании выше температуры кипения или при детонации они очень сильно взрывают.

Нитраты этиленгликоля и глицерина, неправильно называемые нитрогликолем и нитроглицерином, применяются в качестве взрывчатых веществ. Сам нитроглицерин (тяжелая жидкость) неудобен и опасен в обращении.
Пентрит - тетранитрат пентаэритрита С(CH 2 ONO 2) 4 , получаемый обработкой пентаэритрита смесью азотной и серной кислот, - тоже сильное взрывчатое вещество бризантного действия.
Нитрат глицерина и нитрат пентаэритрита обладают сосудорасширяющим эффектом и применяются как симптоматические средства при стенокардии.
Производные карбоновых или неорганических кислот, в которых атом водорода в гидроксильной группе замещён радикалом, называются сложными эфирами. Обычно общую формулу сложных эфиров обозначают как два углеводородных радикала, присоединённых к карбоксильной группе - C n H 2n+1 -COO-C n H 2n+1 или R-COOR’.
Номенклатура
Названия сложных эфиров составляются из названий радикала и кислоты с суффиксом «-ат». Например:
- CH 3 COOH - метилформиат;
- HCOOCH 3 - этилформиат;
- CH 3 COOC 4 H 9 - бутилацетат;
- CH 3 -CH 2 -COO-C 4 H 9 - бутилпропионат;
- CH 3 -SO 4 -CH 3 - диметилсульфат.
Также используются тривиальные названия кислоты, входящей в состав соединения:
- С 3 Н 7 СООС 5 Н 11 - амиловый эфир масляной кислоты;
- HCOOCH 3 - метиловый эфир муравьиной кислоты;
- CH 3 -COO-CH 2 -CH(CH 3) 2 - изобутиловый эфир уксусной кислоты.

Рис. 1. Структурные формулы сложных эфиров с названиями.
Классификация
В зависимости от происхождения сложные эфиры делятся на две группы:
- эфиры карбоновых кислот - содержат углеводородные радикалы;
- эфиры неорганических кислот - включают остаток минеральных солей (C 2 H 5 OSO 2 OH, (CH 3 O)P(O)(OH) 2 , C 2 H 5 ONO).
Наиболее разнообразны сложные эфиры карбоновых кислот. От сложности строения зависят их физические свойства. Эфиры низших карбоновых кислот - летучие жидкости с приятным ароматом, высших - твёрдые вещества. Это плохо растворимые соединения, плавающие на поверхности воды.
Виды сложных эфиров карбоновых кислот приведены в таблице.
|
Вид |
Описание |
Примеры |
|
Фруктовые эфиры |
Жидкости, молекулы которых включают не более восьми атомов углерода. Обладают фруктовым ароматом. Состоят из одноатомных спиртов и карбоновых кислот |
|
|
Жидкие (масла) и твёрдые вещества, содержащие от девяти до 19 атомов углерода. Состоят из глицерина и остатков карбоновых (жирных) кислот |
Оливковое масло - смесь глицерина с остатками пальмитиновой, стеариновой, олеиновой, линолевой кислот |
|
|
Твёрдые вещества с 15-45 атомами углерода |
CH 3 (CH 2) 14 -CO-O-(CH 2) 29 CH 3 -мирицилпальмитат |

Рис. 2. Воск.
Сложные эфиры карбоновых кислот - главная составляющая ароматных эфирных масел, которые содержатся в плодах, цветах, ягодах. Также входят в состав пчелиного воска.

Рис. 3. Эфирные масла.
Получение
Получают сложные эфиры несколькими способами:
- реакцией этерификации карбоновых кислот со спиртами:
CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O;
- реакцией ангидридов карбоновых кислот со спиртами:
(CH 3 CO) 2 O + 2C 2 H 5 OH → 2CH 3 COOC 2 H 5 + H 2 O;
- реакцией солей карбоновых кислот с галогенуглеводородами:
CH 3 (CH 2) 10 COONa + CH 3 Cl → CH 3 (CH 2) 10 COOCH 3 + NaCl;
- реакцией присоединения карбоновых кислот к алкенам:
CH 3 COOH + CH 2 =CH 2 → CH 3 COOCH 2 CH 3 + H 2 O.
Свойства
Химические свойства сложных эфиров обусловлены функциональной группой -COOH. Основные свойства сложных эфиров описаны в таблице.
Сложные эфиры используются в косметологии, медицине, пищевой промышленности в качестве ароматизаторов, растворителей, наполнителей.
Что мы узнали?
Из темы урока химии 10 класса узнали, что такое сложные эфиры. Это соединения, включающие два радикала и карбоксильную группу. В зависимости от происхождения могут содержать остатки минеральных или карбоновых кислот. Сложные эфиры карбоновых кислот делятся на три группы: жиры, воски, фруктовые эфиры. Это плохо растворимые в воде вещества с небольшой плотностью и приятным ароматом. Сложные эфиры реагируют со щелочами, водой, галогенами, спиртами и аммиаком.
Тест по теме
Оценка доклада
Средняя оценка: 4.6 . Всего получено оценок: 88.