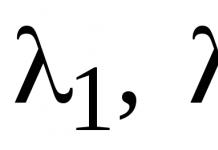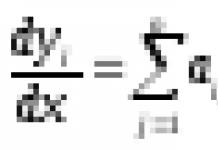Вода является наиболее распространённым растворителем на планете Земля, во многом определяющим характер земной химии, как науки. Большая часть химии, при её зарождении как науки, начиналась именно как химия водных растворов веществ. Её иногда рассматривают, как амфолит — и кислоту и основание одновременно (катион H+ анион OH−). В отсутствие посторонних веществ в воде одинакова концентрация гидроксид-ионов и ионов водорода (или ионов гидроксония), pKa ≈ ок. 16.
Вода химически довольно активное вещество. Сильнополярные молекулы воды сольватируют ионы и молекулы, образуют гидраты и кристаллогидраты. Сольволиз, и в частности гидролиз, происходит в живой и неживой природе, и широко используется в химической промышленности.
Вода реагирует при комнатной температуре:
С активными металлами (натрий, калий, кальций, барий и др.)
С галогенами (фтором, хлором) и межгалоидными соединениями
С солями, образованными слабой кислотой и слабым основанием, вызывая их полный гидролиз
С ангидридами и галогенангидридами карбоновых и неорганических кислот
С активными металлорганическими соединениями (диэтилцинк, реактивы Гриньяра, метил натрий и т. д.)
С карбидами, нитридами, фосфидами, силицидами, гидридами активных металлов (кальция, натрия, лития и др.)
Со многими солями, образуя гидраты
С боранами, силанами
С кетенами, недоокисью углерода
С фторидами благородных газов
Вода реагирует при нагревании:
С железом, магнием
С углем, метаном
С некоторыми алкилгалогенидами
Вода реагирует в присутствии катализатора:
С амидами, эфирами карбоновых кислот
С ацетиленом и другими алкинами
С алкенами
С нитрилами
Химические свойства воды определяются особенностями ее строения. Вода довольно устойчивое вещество, она начинает разлагаться на водород и кислород при нагревании по крайней мере до 1000°С (происходит термическая диссоциация) или под действием ультрафиолетового излучения (фотохимическая диссоциация).
Вода относится к химически активным соединениям. Например, реагирует с фтором. Хлор при нагревании или на свету разлагает воду с выделением атомарного кислорода:
H2O + Cl2 = HCl + HClO (НСlО = НСl + О)
При обычных условиях она взаимодействует с активными металлами:
2H2O + Ca = Ca(ОН) 2 + H2
2H2O + 2Na = 2NaOH + H2
Вода вступает в реакцию и со многими неметаллами. Например, при взаимодействии с атомарным кислородом образуется пероксид водорода:
H2O + O = H2O2
Многие оксиды реагируют с водой, образуя основания и кислоты:
CO2 + H2O = H2CO3
CaO + H2O = Ca(OH)2
При взаимодействии с некоторыми солями образуются кристаллогидраты. При нагревании они теряют кристаллизационную воду:
Na2CO3 + 10H2O = Na2CO3*10H2O
Вода также разлагает большинство солей (так называемый гидролиз).
Благородные металлы с водой не реагируют.
Кроме главных ионов, содержание которых в воде достаточно велико, ряд элементов: азот, фосфор, кремний, алюминий, железо, фтор - присутствуют в ней в концентрациях от 0,1 до 10 мг/л. Они называются мезоэлементами (от греч. "мезос" - "средний", "промежуточный").
Азот в форме нитратов NO3- попадает в водоёмы с дождевой водой, а в форме аминокислот, мочевины (NH2)2CO и солей аммония NH4+ - при разложении органических остатков.
Фосфор существует в воде в форме гидрофосфатов HPO32- и дигидрофосфатов H2PO3-, образующихся в результате разложения органических остатков.
Кремний является постоянным компонентом химического состава природных вод. Этому способствует в отличие от других компонентов повсеместная распространенность соединений кремния в горных породах, и только малая растворимость последних объясняет малое содержание кремния в воде. Концентрация кремния в природных водах обычно составляет несколько миллиграммов в 1 л. В подземных водах она повышается и часто достигает десятков миллиграммов в 1 л, а в горячих термальных водах - даже сотен. На растворимость кремния, кроме температуры сильно влияет повышение pH раствора. Сравнительно малое содержание кремния в поверхностных водах, уступающее растворимости диоксида кремния (125 мг/л при 26 °С, 170 мг/л при 38 °С), указывает на наличие в воде процессов уменьшающих ее концентрацию. К ним надо отнести потребление кремния водными организмами, многие из которых, например диатомовые водоросли, строят свой скелет из кремния. Кроме того, кремниевая кислота как более слабая вытесняется из раствора угольной кислотой:
Na4SiO4 + 4CO2 + 4H2O = H4SiO4 + 4NaHCO3
Способствует неустойчивости кремния в растворе и склонность кремниевой кислоты при определенных условиях переходить в гель. В очень мало минерализованных водах кремний составляет существенную, а иногда и преобладающую часть химического состава воды, несмотря на его малое абсолютное содержание. Присутствие кремния в воде является серьезной помехой в технике, так как при продолжительном кипячении воды кремний образует в котлах очень твердую силикатную накипь.
Алюминий поступает в водоёмы в результате действия кислот на глины (каолин):
Al2(OH)4 + 6H+ = 2SiO2 + 5H2O + 2Al3+
Основной источник железа - железосодержащие глины. Органические остатки (ниже обозначаются как "С"), находящиеся в контакте с ними, восстанавливают железо до двухвалентного, которое медленно вымывается в форме гидрокарбоната или солей гуминовых кислот:
2Fe2O3 + "C" + 4H2O + 7CO2 = 4Fe(HCO3)2
Когда вода с растворёнными в ней ионами Fe2+ вступает в контакт с воздухом, железо быстро окисляется, образуя коричневый осадок гидроксида Fe(OH)3. Со временем он превращается в болотную руду - бурый железняк (лимонит) FeO(OH). Карельская болотная руда использовалась в XVIII-XIX столетиях для получения железа.
Синеватая плёнка на поверхности воды - это Fe(OH)3, образующийся, когда подземные воды, содержавшие ионы Fe2+, вступают в контакт с воздухом. Ее часто путают с масляной пленкой, однако различить их очень легко: у пленки гидроксида железа рваные края. Если поверхность воды слегка взволновать, гидроксидная пленка, в отличие от масляной, не будет переливаться.
Химический состав природной воды определяет предшествующая ему история, т.е. путь, совершенный водой в процессе своего круговорота. Количество растворенных веществ в такой воде будет зависеть, с одной стороны, от состава тех веществ, с которыми она соприкасалась, с другой - от условий, в которых происходили эти взаимодействия. Влиять на химический состав воды могут следующие факторы: горные породы, почвы, живые организмы, деятельность человека, климат, рельеф, водный режим, растительность, гидрогеологические и гидродинамические условия и пр. Рассмотрим лишь некоторые факторы, влияющие на состав воды.
Почвенный раствор и фильтрующиеся через почву атмосферные осадки способны усиливать растворение пород и минералов. Это одно из важнейших свойств почвы, влияющее на формирование состава природных вод, является результатом увеличения концентрации диоксида углерода в почвенном растворе, выделяющегося при дыхании живых организмов и корневой системы в почвах и биохимическом распаде органических остатков. Вследствие этого концентрация CO2 в почвенном воздухе возрастает от 0,033 %, свойственных атмосферному воздуху, до 1 % и более в почвенном воздухе (в тяжелых глинистых почвах концентрация CO2 в почвенном воздухе достигает иногда 5-10 %, придавая тем самым раствору сильное агрессивное действие по отношению к породам). Другим фактором, усиливающим агрессивное действие фильтрующейся через почву воды, является органическое вещество - почвенный гумус, образующийся в почвах при трансформации растительных остатков. В составе гумуса в качестве активных реагентов прежде всего следует назвать гуминовые и фульвокислоты и более простые соединения, например органические кислоты (лимонная, щавелевая, уксусная, яблочная и др.), амины и т.п. Почвенный раствор, обогащаясь органическими кислотами и CO2, во много раз ускоряет химическое выветривание алюмосиликатов, содержащихся в почвах. Аналогично вода, фильтрующаяся через почву, ускоряет химическое выветривание алюмосиликатов и карбонатных пород, подстилающих почву. Известняк легко образует растворимый (до 1,6 г/л) гидрокарбонат кальция:
CaCO3 + H2O + CO2 ↔ Ca(HCO3)2
Почти на всей европейской части России (кроме Карелии и Мурманской области) известняки, а также доломиты MgCO3 CaCO3 залегают довольно близко к поверхности. Поэтому вода здесь содержит преимущественно гидрокарбонаты кальция и магния. В таких реках, как Волга, Дон, Северная Двина, и основных их притоках гидрокарбонаты кальция и магния составляют от 3/4 до 9/10 всех растворённых солей.
Соли попадают в водоёмы и в результате деятельности человека. Так, хлоридами натрия и кальция зимой посыпают дороги, чтобы растапливать лёд. Весной вместе с талой водой хлориды стекают в реки. Треть хлоридов в реках европейской части России привнесена туда человеком. В реках, на которых стоят крупные города, эта доля гораздо больше.
Рельеф местности косвенно влияет на состав воды, способствуя вымыванию солей из толщи пород. Глубина эрозионного вреза реки облегчает поступление в реку более минерализованных грунтовых вод нижних горизонтов. Этому же способствуют и другие виды депрессий (речные долины, балки, овраги), улучшающие дренирование водосбора.
Климат же, создает общий фон, на котором происходит большинство процессов, влияющих на формирование химическою состава природных вод. Климат прежде всего определяет баланс тепла и влаги, от которого зависит увлажненность местности и объем водного стока, а следовательно, и разбавление или концентрирование природных растворов и возможность растворения веществ или выпадения их в осадок.
Огромное влияние на химический состав воды и его изменение с течением времени оказывают источники питания водного объекта и их соотношение. В период таяния снега вода в реках, озерах и водохранилищах имеет более низкую минерализацию, чем в период, когда большая часть питания осуществляется за счет грунтовых и подземных вод. Это обстоятельство используют при регулировании наполнения водохранилищ и сброса из них воды. Как правило, водохранилища наполняют в период весеннего половодья, когда приточная вода имеет меньшую минерализацию.
ВОДА
Молекула воды состоит из атома кислорода и двух атомов водорода, присоединившихся к нему под углом 104,5°.
Угол 104,5° между связями в молекуле воды обусловливает рыхлость льда и жидкой воды и как следствие аномальную зависимость плотности от температуры. Именно поэтому крупные водоемы не промерзают до дна, что делает возможным существование в них жизни.
ВОДА, ЛЁД И ПАР, соответственно жидкое, твердое и газообразное состояния химического соединения молекулярной формулы Н 2 О.
Благодаря сильному притяжению между молекулами у воды высокие температуры плавления (0С) и кипения (100С). Толстый слой воды имеет голубой цвет, что обусловливается не только ее физическими свойствами, но и присутствием взвешенных частиц примесей. Вода горных рек зеленоватая из-за содержащихся в ней взвешенных частиц карбоната кальция. Чистая вода – плохой проводник электричества. Плотность воды максимальна при 4С она равна 1 г/см 3 . Лёд имеет меньшую плотность, чем жидкая вода и всплывает на её поверхность, что очень важно для обитателей водоёмов зимой.
Вода обладает исключительно большой теплоёмкостью, поэтому она медленно нагревается и медленно остывает. Благодаря этому водные бассейны регулируют температуру на нашей планете.
Химические свойства воды
Вода - весьма реакционноспособное вещество. При обычных условиях она взаимодействует со многими основными и кислотными оксидами, а также со щелочными и щелочно-земельными металлами. Вода образует многочисленные соединения - кристаллогидраты.
Под действием электрического тока вода разлагается на водород и кислород:
2 H 2 O электрический ток = 2 H 2 + O 2
Видео "Электролиз воды"
- Магний с горячей водой реагирует с образованием нерастворимого основания:
Mg + 2H 2 O = Mg(OH) 2 + H 2
- Бериллий с водой образует амфотерный оксид: Be + H 2 O = BeO + H 2
1. Активные металлы - это:
Li , Na , K , Rb , Cs , Fr – 1 группа «А»
Ca , Sr , Ba , Ra – 2 группа «А»
2. Ряд активности металлов

3. Щёлочь – это растворимое в воде основание, сложное вещество в состав которого входит активный металл и гидроксильная группа ОН ( I ).
4. Металлы средней активности в ряду напряжений стоят от Mg до Pb (алюминий на особом положении)
Видео "Взаимодействие натрия с водой"
Помните!!!
Алюминий реагирует с водой подобно активным металлам, образуя основание:
2Al + 6H 2 O = 2Al ( OH ) 3 + 3H 2


Используя образец, запишите уравнения реакций взаимодействия:
С O 2 + H 2 O =
SO 3 + H 2 O =
Cl 2 O 7 + H 2 O =
P 2 O 5 + H 2 O ( горячая ) =
N 2 O 5 + H 2 O =

Помните! С водой реагируют только оксиды активных металлов. Оксиды металлов средней активности и металлов, стоящих после водорода в ряду активности в воде не растворяются, например, CuO + H 2 O = реакция не возможна.
Видео "Взаимодействие оксидов металлов с водой"
Li + H 2 O =
Cu + H 2 O =
ZnO + H 2 O =
Al + H 2 O =
Ba + H 2 O =
K 2 O + H 2 O =
Mg + H 2 O =
N 2 O 5 + H 2 O =
Самое важное, уникальное по свойствам и составу вещество нашей планеты - это, конечно, вода. Ведь именно благодаря ей на Земле жизнь есть, в то время как на других известных сегодня объектах Солнечной системы ее нет. Твердая, жидкая, в виде пара - она нужна и важна любая. Вода и ее свойства составляют предмет изучения целой научной дисциплины - гидрологии.
Количество воды на планете
Если рассматривать показатель количества данного оксида во всех агрегатных состояниях, то его на планете около 75% от общей массы. При этом следует учитывать связанную воду в органических соединениях, живых существах, минералах и прочих элементах.
Если учитывать только жидкое и твердое состояние воды, показатель падет до 70,8%. Рассмотрим, как распределяются эти проценты, где содержится рассматриваемое вещество.
- Соленой воды в океанах и морях, солончаковых озерах на Земле 360 млн км 2 .
- Пресная вода распределена неравномерно: ее в ледниках Гренландии, Арктики, Антарктиды заковано во льды 16,3 млн км 2 .
- В пресных реках, болотах и озерах сосредоточено 5,3 млн км 2 оксида водорода.
- Подземные воды составляют 100 млн м 3 .
Именно поэтому космонавтам из далекого космического пространства видно Землю в форме шара голубого цвета с редкими вкраплениями суши. Вода и ее свойства, знание особенностей строения являются важными элементами науки. К тому же, в последнее время человечество начинает испытывать явную нехватку пресной воды. Может быть, такие знания помогут в решении данной проблемы.
Состав воды и строение молекулы
Если рассмотреть эти показатели, то сразу станут понятны и свойства, которые проявляет это удивительное вещество. Так, молекула воды состоит из двух атомов водорода и одного атома кислорода, поэтому имеет эмпирическую формулу Н 2 О. Кроме того, при построении самой молекулы большую роль играют электроны обоих элементов. Посмотрим, что собой представляют структура воды и ее свойства.

Очевидно, что каждая молекула ориентирована вокруг другой, и все вместе они формируют общую кристаллическую решетку. Интересно то, что оксид построен в форме тетраэдра - атом кислорода в центре, а две пары электронов его и два атома водорода вокруг асимметрично. Если провести через центры ядер атомов линии и соединить их, то получится именно тетраэдрическая геометрическая форма.
Угол между центром атома кислорода и ядрами водородов составляет 104,5 0 С. Длина связи О-Н = 0,0957 нм. Наличие электронных пар кислорода, а также его большее в сравнении с водородами сродство к электрону обеспечивают формирование в молекуле отрицательно заряженного поля. В противовес ему ядра водородов образуют положительно заряженную часть соединения. Таким образом, выходит, что молекула воды - диполь. Это определяет то, какой может быть вода, и ее физические свойства также зависят от строения молекулы. Для живых существ эти особенности играют жизненно важную роль.
Основные физические свойства
К таковым принято относить кристаллическую решетку, температуры кипения и плавления, особенные индивидуальные характеристики. Все их и рассмотрим.
- Строение кристаллической решетки оксида водорода зависит от агрегатного состояния. Оно может быть твердым - лед, жидким - основная вода при обычных условиях, газообразным - пар при повышении температуры воды свыше 100 0 С. Красивые узорные кристаллы формирует лед. Решетка в целом рыхлая, но соединение очень прочное, плотность низкая. Видеть ее можно на примере снежинок или морозных узоров на стеклах. У обычной воды решетка не имеет постоянной формы, она изменяется и переходит из одного состояния в другое.
- Молекула воды в космическом пространстве имеет правильную форму шара. Однако под действием земной силы тяжести она искажается и в жидком состоянии принимает форму сосуда.
- То, что по структуре оксид водорода - диполь, обуславливает следующие свойства: высокая теплопроводность и теплоемкость, которая прослеживается в быстром нагревании и долгом остывании вещества, способность ориентировать вокруг себя как ионы, так и отдельные электроны, соединения. Это делает воду универсальным растворителем (как полярным, так и нейтральным).
- Состав воды и строение молекулы объясняют способность этого соединения образовывать множественные водородные связи, в том числе с другими соединениями, имеющими неподеленные электронные пары (аммиак, спирт и прочие).
- Температура кипения жидкой воды - 100 0 С, кристаллизация наступает при +4 0 С. Ниже этого показателя - лед. Если же увеличивать давление, то температура кипения воды резко возрастет. Так, при высоких атмосферах в ней можно растопить свинец, но она при этом даже не закипит (свыше 300 0 С).
- Свойства воды весьма значимы для живых существ. Например, одно из самых важных - поверхностное натяжение. Это формирование тончайшей защитной пленки на поверхности оксида водорода. Речь идет о воде в жидком состоянии. Эту пленку разорвать механическим воздействием очень сложно. Учеными установлено, что понадобится сила, равная весу в 100 тонн. Как ее заметить? Пленка очевидна, когда вода капает из крана медленно. Видно, что она словно в какой-то оболочке, которая растягивается до определенного предела и веса и отрывается в виде круглой капельки, слегка искаженной силой тяжести. Благодаря поверхностному натяжению многие предметы могут находиться на поверхности воды. Насекомые, имеющие особые приспособления, могут свободно передвигаться по ней.
- Вода и ее свойства аномальны и уникальны. По органолептическим показателям данное соединение - бесцветная жидкость без вкуса и запаха. То, что мы называем вкусом воды, - это растворенные в ней минералы и другие компоненты.
- Электропроводность оксида водорода в жидком состоянии зависит от того, сколько и каких солей в нем растворены. Дистиллированная вода, не содержащая никаких примесей, электрический ток не проводит.
Лед - это особое состояние воды. В структуре этого ее состояния молекулы связаны друг с другом водородными связями и формируют красивую кристаллическую решетку. Но она достаточно неустойчива и легко может расколоться, растаять, то есть деформироваться. Между молекулами сохраняется множество пустот, размеры которых превышают размеры самих частиц. Благодаря этому плотность льда меньше, чем жидкого оксида водорода.

Это имеет большое значение для рек, озер и прочих пресных водоемов. Ведь в зимний период вода в них не замерзает полностью, а лишь покрывается плотной коркой более легкого льда, всплывающего наверх. Если бы данное свойство не было характерно для твердого состояния оксида водорода, то водоемы промерзали бы насквозь. Жизнь под водой была бы невозможна.
Кроме того, твердое состояние воды имеет большое значение как источник огромного количества питьевых пресных запасов. Это ледники.
Особенным свойством воды можно назвать явление тройной точки. Это такое состояние, при котором лед, пар и жидкость могут существовать одновременно. Для этого требуются такие условия, как:
- высокое давление - 610 Па;
- температура 0,01 0 С.
Показатель прозрачности воды варьируется в зависимости от посторонних примесей. Жидкость может быть полностью прозрачной, опалесцентной, мутной. Поглощаются волны желтого и красного цветов, глубоко проникают лучи фиолетовые.

Химические свойства
Вода и ее свойства - важный инструмент в понимании многих процессов жизнедеятельности. Поэтому они изучены очень хорошо. Так, гидрохимию интересуют вода и ее химические свойства. Среди них можно назвать следующие:
- Жесткость. Это такое свойство, которое объясняется наличием солей кальция и магния, их ионов в растворе. Подразделяется на постоянную (соли названных металлов: хлоридов, сульфатов, сульфитов, нитратов), временную (гидрокарбонаты), которая устраняется кипячением. В России воду перед использованием смягчают химическим путем для лучшего качества.
- Минерализация. Свойство, основанное на дипольном моменте оксида водорода. Благодаря его наличию молекулы способны присоединять к себе множество других веществ, ионов и удерживать их. Так формируются ассоциаты, клатраты и прочие объединения.
- Окислительно-восстановительные свойства. Как универсальный растворитель, катализатор, ассоциат, вода способна взаимодействовать с множеством простых и сложных соединений. С одними она выступает в роли окислителя, с другими - наоборот. Как восстановитель реагирует с галогенами, солями, некоторыми менее активными металлами, с многими органическими веществами. Последние превращения изучает органическая химия. Вода и ее свойства, в частности, химические, показывают, насколько она универсальна и уникальна. Как окислитель она вступает в реакции с активными металлами, некоторыми бинарными солями, многими органическими соединениями, углеродом, метаном. Вообще химические реакции с участием данного вещества нуждаются в подборе определенных условий. Именно от них и будет зависеть исход реакции.
- Биохимические свойства. Вода является неотъемлемой частью всех биохимических процессов организма, являясь растворителем, катализатором и средой.
- Взаимодействие с газами с образованием клатратов. Обычная жидкая вода может поглощать даже неактивные химически газы и располагать их внутри полостей между молекулами внутренней структуры. Такие соединения принято называть клатратами.
- Со многими металлами оксид водорода формирует кристаллогидраты, в которые он включен в неизменном виде. Например, медный купорос (CuSO 4 *5H 2 O), а также обычные гидраты (NaOH*H 2 O и другие).
- Для воды характерны реакции соединения, при которых происходит образование новых классов веществ (кислот, щелочей, оснований). Они не являются окислительно-восстановительными.
- Электролиз. Под действием электрического тока молекула разлагается на составные газы - водород и кислород. Один из способов получения их в лаборатории и промышленности.
С точки зрения теории Льюиса вода - это слабая кислота и слабое основание одновременно (амфолит). То есть можно сказать о некоей амфотерности в химических свойствах.

Вода и ее полезные свойства для живых существ
Сложно переоценить то значение, которое имеет оксид водорода для всего живого. Ведь вода и есть сам источник жизни. Известно, что без нее человек не смог бы прожить и недели. Вода, ее свойства и значение просто колоссальны.
- Это универсальный, то есть способный растворять и органические, и неорганические соединения, растворитель, действующий в живых системах. Именно поэтому вода - источник и среда для протекания всех каталитических биохимических преобразований, с формированием сложных жизненно важных комплексных соединений.
- Способность образовывать водородные связи делает данное вещество универсальным в выдерживании температур без изменения агрегатного состояния. Если бы это было не так, то при малейшем снижении градусов она превращалась бы в лед внутри живых существ, вызывая гибель клеток.
- Для человека вода - источник всех основных бытовых благ и нужд: приготовление пищи, стирка, уборка, принятие ванны, купание и плавание и прочее.
- Промышленные заводы (химические, текстильные, машиностроительные, пищевые, нефтеперерабатывающие и другие) не сумели бы осуществлять свою работу без участия оксида водорода.
- Издревле считалось, что вода - это источник здоровья. Она применялась и применяется сегодня как лечебное вещество.
- Растения используют ее как основной источник питания, за счет чего они продуцируют кислород - газ, благодаря которому существует жизнь на нашей планете.
Можно назвать еще десятки причин того, почему вода - это самое широко распространенное, важное и необходимое вещество для всех живых и искусственно созданных человеком объектов. Мы привели только самые очевидные, главные.

Гидрологический цикл воды
Иными словами, это ее круговорот в природе. Очень важный процесс, позволяющий постоянно пополнять исчезающие запасы воды. Как он происходит?
Основных участников трое: подземные (или грунтовые) воды, поверхностные воды и Мировой океан. Важна также и атмосфера, конденсирующая и выдающая осадки. Также активными участниками процесса являются растения (в основном деревья), способные поглощать огромное количество воды в сутки.
Итак, процесс происходит следующим образом. Грунтовые воды заполняют подземные капилляры и стекаются к поверхности и Мировому океану. Затем поверхностные воды поглощаются растениями и транспирируются в окружающую среду. Также происходит испарение с огромных площадей океанов, морей, рек, озер и прочих водоемов. Попав в атмосферу, вода что делает? Конденсируется и проливается обратно в виде осадков (дождь, снег, град).
Если бы не происходили эти процессы, то запасы воды, особенно пресной, давно бы уже закончились. Именно поэтому охране и нормальному гидрологическому циклу уделяется людьми большое внимание.
Понятие о тяжелой воде
В природе оксид водорода существует в виде смеси изотопологов. Это связано с тем, что водород формирует три вида изотопа: протий 1 Н, дейтерий 2 Н, тритий 3 Н. Кислород, в свою очередь, также не отстает и образует три устойчивые формы: 16 О, 17 О, 18 О. Именно благодаря этому существует не просто обычная протиевая вода состава Н 2 О (1 Н и 16 О), но еще и дейтериевая, и тритиевая.

При этом устойчива по структуре и форме именно дейтериевая (2 Н), которая включается в состав практически всех природных вод, но в малом количестве. Именно ее называют тяжелой. Она несколько отличается от обычной или легкой по всем показателям.
Тяжелая вода и ее свойства характеризуются несколькими пунктами.
- Кристаллизуется при температуре 3,82 0 С.
- Кипение наблюдается при 101,42 0 С.
- Плотность составляет 1,1059 г/см 3 .
- Как растворитель в несколько раз хуже легкой воды.
- Имеет химическую формулу D 2 O.
При проведении опытов, показывающих влияние подобной воды на живые системы, было установлено, что жить в ней способны лишь некоторые виды бактерий. Для приспособления и акклиматизации колониям потребовалось время. Но, приспособившись, они полностью восстановили все жизненно важные функции (размножение, питание). Кроме того, стали очень устойчивы к воздействию радиоактивного излучения. Опыты на лягушках и рыбах положительного результата не дали.
Современные области применения дейтерия и образованной им тяжелой воды - атомная и ядерная энергетика. Получить в лабораторных условиях такую воду можно при помощи электролиза обычной - она образуется как побочный продукт. Сам дейтерий формируется при многократных перегонках водорода в специальных устройствах. Применение его основано на способности замедлять нейтронные синтезы и протонные реакции. Именно тяжелая вода и изотопы водорода - основа для создания ядерной и водородной бомбы.
Опыты на применении дейтериевой воды людьми в небольших количествах показали, что задерживается она недолго - полный вывод наблюдается через две недели. Употреблять ее в качестве источника влаги для жизни нельзя, однако техническое значение просто огромно.
Талая вода и ее применение
Свойства такой воды издревле были определены людьми как целебные. Давно было замечено, что при таянии снега животные стараются напиться водой из образовавшихся лужиц. Позже были тщательно исследованы ее структура и биологическое воздействие на организм человека.

Талая вода, ее признаки и свойства находятся посередине между обычной легкой и льдом. Изнутри она образована не просто молекулами, а набором кластеров, сформированных кристаллами и газом. То есть внутри пустот между структурными частями кристалла находятся водород и кислород. По общему виду строение талой воды сходно со строением льда - сохраняется структурность. Физические свойства такого оксида водорода незначительно меняются в сравнении с обычным. Однако биологическое воздействие на организм отличное.
При замораживании воды первой фракцией превращается в лед более тяжелая часть - это дейтериевые изотопы, соли и примеси. Поэтому эту сердцевину следует удалять. А вот остальная часть - чистая, структурированная и полезная вода. Каково воздействие на организм? Учеными Донецкого НИИ были названы следующие виды улучшений:
- Ускорение восстановительных процессов.
- Укрепление иммунитета.
- У детей после ингаляций такой водой происходит восстановление и излечение простудных заболеваний, проходит кашель, насморк и прочее.
- Улучшается дыхание, состояние гортани и слизистых оболочек.
- Общее самочувствие человека, активность повышаются.
Сегодня существует ряд сторонников лечения именно талой водой, которые пишут свои положительные отзывы. Однако есть ученые, в том числе медики, которые эти взгляды не поддерживают. Они считают, что вреда от такой воды не будет, но и пользы мало.
Энергетика
Почему свойства воды могут изменяться и восстанавливаться при переходе в разные агрегатные состояния? Ответ на этот вопрос следующий: у данного соединения существует своя информационная память, которая записывает все изменения и приводит к восстановлению структуры и свойств в нужное время. Биоэнергетическое поле, через которое проходит часть воды (та, что поступает из космоса), несет в себе мощный заряд энергии. Эту закономерность часто используют при лечении. Однако с медицинской точки зрения не каждая вода способна оказать благоприятный эффект, в том числе и информационный.
Структурированная вода - что это?
Это такая вода, которая имеет несколько иное строение молекул, расположение кристаллических решеток (такое, которое наблюдается у льда), но это все же жидкость (талая также относится к этому типу). В этом случае состав воды и ее свойства с научной точки зрения не отличаются от тех, что характерны для обычного оксида водорода. Поэтому структурированная вода не может иметь такого широкого лечебного эффекта, который ей приписывают эзотерики и сторонники нетрадиционной медицины.
Оксид водорода (H 2 O), гораздо более известный всем нам под названием "вода", без преувеличения, является главной жидкостью в жизнедеятельности организмов на Земле, ибо все химико-билогические реакции проходят, либо с участием воды, либо в растворах.
Вода является вторым, после воздуха, самым важным веществом для организма человека. Прожить без воды человек может не более 7-8 суток.
Чистая вода в природе может существовать в трех агрегатных состояниях: в твердом - в виде льда, в жикдом, собственно вода, в газообразном - в виде пара. Таким разнообразием агрегатных состояний в природе больше не может похвастаться ни одно вещество.
Физические свойства воды
- при н.у. - это жидкость без цвета, запаха и вкуса;
- вода обладает высокой теплоёмкостью и низкой электропроводностью;
- температура плавления 0°C;
- температура кипения 100°C;
- максимальная плотность воды при 4°C равна 1 г/см 3 ;
- вода - хороший растворитель.
Строение молекулы воды
Молекула воды состоит из одного атома кислорода, который соединен с двумя атомами водорода, при этом связи O-H образуют угол в 104,5°, при при этом общие электронные пары смещены к атому кислорода, который более электроотрицателен по сравнению с атомами водорода, поэтому, на атоме кислорода формируется частичный отрицательный заряд, соответственно, на атомах водорода - положительный. Таким образом, молекулу воды можно рассматривать, как диполь.
Молекулы воды могут между собой образовывать водородные связи, притягиваясь противоположно заряженными частями (на рисунке водородные связи показаны пунктиром):

Формирование водородных связей объясняет высокую плотность воды, температуру ее кипения и плавления.
Количество водородных связей зависит от температуры - чем выше температура, тем меньшее кол-во связей образуется: в парах воды присутствуют только отдельные ее молекулы; в жидком состоянии - образуются ассоциаты (H 2 O) n , в кристаллическом состоянии каждая молекула воды связана с соседними молекулами четырьмя водородными связями.
Химические свойства воды
Вода "охотно" вступает в реакции с другими веществами:
- с щелочными и щелочноземельными металлами вода реагирует при н.у.: 2Na+2H 2 O = 2NaOH+H 2
- с менее активными металлами и неметаллами вода реагирует только при высокой температуре: 3Fe+4H 2 O=FeO → Fe 2 O 3 +4H 2 C+2H 2 O → CO 2 +2H 2
- с основными оксидами при н.у. вода реагирует с образованием оснований: CaO+H 2 O = Ca(OH) 2
- с кислотными оксидами при н.у. вода реагирует с образованием кислот: CO 2 +H 2 O = H 2 CO 3
- вода является главным участником реакций гидролиза (подробнее см. Гидролиз солей);
- вода участвует в реакциях гидратации, присоединяясь к органическим веществам с двойными и тройными связями.
Растворимость веществ в воде
- хорошо растворимые вещества - в 100 г воды растворяется более 1 г вещества при н.у.;
- малорастворимые вещества - в 100 г воды растворяется 0,01-1 г вещества;
- практически нерастворимые вещества - в 100 г водры растворяется менее 0,01 г вещества.
Совершенно нерастворимых веществ в природе не существует.
Основания – сложные вещества, которые состоят из катиона металла Ме + (или металлоподобного катиона, например, иона аммония NH 4 +) и гидроксид-аниона ОН — .
По растворимости в воде основания делят на растворимые (щелочи) и нерастворимые основания . Также есть неустойчивые основания , которые самопроизвольно разлагаются.
Получение оснований
1. Взаимодействие основных оксидов с водой. При этом с водой реагируют в обычных условиях только те оксиды, которым соответствует растворимое основание (щелочь). Т.е. таким способом можно получить только щёлочи:
основный оксид + вода = основание
Например , оксид натрия в воде образует гидроксид натрия (едкий натр):
Na 2 O + H 2 O → 2NaOH
При этом оксид меди (II) с водой не реагирует :
CuO + H 2 O ≠
2. Взаимодействие металлов с водой. При этом с водой реагируют в обычных условиях только щелочные металлы (литий, натрий, калий. рубидий, цезий) , кальций, стронций и барий. При этом протекает окислительно-восстановительная реакция, окислителем выступает водород, восстановителем является металл.
металл + вода = щёлочь + водород
Например , калий реагирует с водой очень бурно :
2K 0 + 2H 2 + O → 2K + OH + H 2 0
3. Электролиз растворов некоторых солей щелочных металлов . Как правило, для получения щелочей электролизу подвергают растворы солей, образованных щелочными или щелочноземельными металлами и бескилородными кислотами (кроме плавиковой) – хлоридами, бромидами, сульфидами и др. Более подробно этот вопрос рассмотрен в статье .
Например , электролиз хлорида натрия:
2NaCl + 2H 2 O → 2NaOH + H 2 + Cl 2
4. Основания образуются при взаимодействии других щелочей с солями. При этом взаимодействуют только растворимые вещества, а в продуктах должна образоваться нерастворимая соль, либо нерастворимое основание:
либо
щелочь + соль 1 = соль 2 ↓ + щелочь
Например: карбонат калия реагирует в растворе с гидроксидом кальция:
K 2 CO 3 + Ca(OH) 2 → CaCO 3 ↓ + 2KOH
Например: хлорид меди (II) взаимодействет в растворе с гидроксидом натрия. При этом выпадает голубой осадок гидроксида меди (II) :
CuCl 2 + 2NaOH → Cu(OH) 2 ↓ + 2NaCl
Химические свойства нерастворимых оснований
1. Нерастворимые основания взаимодействуют с сильными кислотами и их оксидами (и некоторыми средними кислотами). При этом образуются соль и вода .
нерастворимое основание + кислота = соль + вода
нерастворимое основание + кислотный оксид = соль + вода
Например , гидроксид меди (II) взаимодействует с сильной соляной кислотой:
Cu(OH) 2 + 2HCl = CuCl 2 + 2H 2 O
При этом гидроксид меди (II) не взаимодействует с кислотным оксидом слабой угольной кислоты – углекислым газом:
Cu(OH) 2 + CO 2 ≠
2. Нерастворимые основания разлагаются при нагревании на оксид и воду.
Например , гидроксид железа (III) разлагается на оксид железа (III) и воду при прокаливании:
2Fe(OH) 3 = Fe 2 O 3 + 3H 2 O
3. Нерастворимые основания не взаимодействуют с амфотерными оксидами и гидроксидами.
нерастворимое оснвоание + амфотерный оксид ≠
нерастворимое основание + амфотерный гидроксид ≠
4. Некоторые нерастворимые основания могут выступать в качестве восстановителей . Восстановителями являются основания, образованные металлами с минимальной или промежуточной степенью окисления , которые могут повысить свою степень окисления (гидроксид железа (II), гидроксид хрома (II) и др.).
Например , гидроксид железа (II) можно окислить кислородом воздуха в присутствии воды до гидроксида железа (III):
4Fe +2 (OH) 2 + O 2 0 + 2H 2 O → 4Fe +3 (O -2 H) 3
Химические свойства щелочей
1. Щёлочи взаимодействуют с любыми кислотами – и сильными, и слабыми . При этом образуются средняя соль и вода. Эти реакции называются реакциями нейтрализации . Возможно и образование кислой соли , если кислота многоосновная, при определенном соотношении реагентов, либо в избытке кислоты . В избытке щёлочи образуется средняя соль и вода:
щёлочь (избыток) + кислота = средняя соль + вода
щёлочь + многоосновная кислота (избыток) = кислая соль + вода
Например , гидроксид натрия при взаимодействии с трёхосновной фосфорной кислотой может образовывать 3 типа солей: дигидрофосфаты , фосфаты или гидрофосфаты .
При этом дигидрофосфаты образуются в избытке кислоты, либо при мольном соотношении (соотношении количеств веществ) реагентов 1:1.
NaOH + H 3 PO 4 → NaH 2 PO 4 + H 2 O
При мольном соотношении количества щелочи и кислоты 2:1 образуются гидрофосфаты:
2NaOH + H 3 PO 4 → Na 2 HPO 4 + 2H 2 O
В избытке щелочи, либо при мольном соотношении количества щелочи и кислоты 3:1 образуется фосфат щелочного металла.
3NaOH + H 3 PO 4 → Na 3 PO 4 + 3H 2 O
2. Щёлочи взаимодействуют с амфотерными оксидами и гидроксидами. При этом в расплаве образуются обычные соли , а в растворе – комплексные соли .
щёлочь (расплав) + амфотерный оксид = средняя соль + вода
щёлочь (расплав) + амфотерный гидроксид = средняя соль + вода
щёлочь (раствор) + амфотерный оксид = комплексная соль
щёлочь (раствор) + амфотерный гидроксид = комплексная соль
Например , при взаимодействии гидроксида алюминия с гидроксидом натрия в расплаве образуется алюминат натрия. Более кислотный гидроксид образует кислотный остаток:
NaOH + Al(OH) 3 = NaAlO 2 + 2H 2 O
А в растворе образуется комплексная соль:
NaOH + Al(OH) 3 = Na
Обратите внимание, как составляется формула комплексной соли: сначала мы выбираем центральный атом (к ак правило, это металл из амфотерного гидроксида). Затем дописываем к нему лиганды — в нашем случае это гидроксид-ионы. Число лигандов, как правило, в 2 раза больше, чем степень окисления центрального атома. Но комплекс алюминия — исключение, у него число лигандов чаще всего равно 4. Заключаем полученный фрагмент в квадртаные скобки — это комплексный ион. Определяем его заряд и снаружи дописываем нужное количество катионов или анионов.
3. Щёлочи взаимодействуют с кислотными оксидами. При этом возможно образование кислой или средней соли , в зависимости от мольного соотношения щёлочи и кислотного оксида. В избытке щёлочи образуется средняя соль, а в избытке кислотного оксида образуется кислая соль:
щёлочь (избыток) + кислотный оксид = средняя соль + вода
либо:
щёлочь + кислотный оксид (избыток) = кислая соль
Например , при взаимодействии избытка гидроксида натрия с углекислым газом образуется карбонат натрия и вода:
2NaOH + CO 2 = Na 2 CO 3 + H 2 O
А при взаимодействии избытка углекислого газа с гидроксидом натрия образуется только гидрокарбонат натрия:
2NaOH + CO 2 = NaHCO 3
4. Щёлочи взаимодействуют с солями. Щёлочи реагируют только с растворимыми солями в растворе , при условии, что в продуктах образуется газ или осадок . Такие реакции протекают по механизму ионного обмена .
щёлочь + растворимая соль = соль + соответствующий гидроксид
Щёлочи взаимодействуют с растворами солей металлов, которым соответствуют нерастворимые или неустойчивые гидроксиды.
Например , гидроксид натрия взаимодействует с сульфатом меди в растворе :
Cu 2+ SO 4 2- + 2Na + OH — = Cu 2+ (OH) 2 — ↓ + Na 2 + SO 4 2-
Также щёлочи взаимодействуют с растворами солей аммония .
Например , гидроксид калия взаимодействует с раствором нитрата аммония:
NH 4 + NO 3 — + K + OH — = K + NO 3 — + NH 3 + H 2 O
! При взаимодействии солей амфотерных металлов с избытком щёлочи образуется комплексная соль!
Давайте рассмотрим этот вопрос подробнее. Если соль, образованная металлом, которому соответствует амфотерный гидроксид , взаимодействует с небольшим количеством щёлочи, то протекает обычная обменная реакция, и в осадок выпадает гидроксид этого металла .
Например , избыток сульфата цинка реагирует в растворе с гидроксидом калия:
ZnSO 4 + 2KOH = Zn(OH) 2 ↓ + K 2 SO 4
Однако, в данной реакции образуется не основание, а амфотерный гидроксид . А, как мы уже указывали выше, амфотерные гидроксиды растворяются в избытке щелочей с образованием комплексных солей . Таким образом, при взаимодействии сульфата цинка с избытком раствора щёлочи образуется комплексная соль, осадок не выпадает:
ZnSO 4 + 4KOH = K 2 + K 2 SO 4
Таким образом, получаем 2 схемы взаимодействия солей металлов, которым соответствуют амфотерные гидроксиды, с щелочами:
соль амф.металла (избыток) + щёлочь = амфотерный гидроксид↓ + соль
соль амф.металла + щёлочь (избыток) = комплексная соль + соль
5. Щёлочи взаимодействуют с кислыми солями. При этом образуются средние соли, либо менее кислые соли.
кислая соль + щёлочь = средняя соль + вода
Например , гидросульфит калия реагирует с гидроксидом калия с образованием сульфита калия и воды:
KHSO 3 + KOH = K 2 SO 3 + H 2 O
Свойства кислых солей очень удобно определять, разбивая мысленно кислую соль на 2 вещества — кислоту и соль. Например, гидрокарбонта натрия NaHCO 3 мы разбиваем на уольную кислоту H 2 CO 3 и карбонат натрия Na 2 CO 3 . Свойства гидрокарбоната в значительной степени определяются свойствами угольной кислоты и свойствами карбоната натрия.
6. Щёлочи взаимодействуют с металлами в растворе и расплаве. При этом протекает окислительно-восстановительная реакция, в растворе образуется комплексная соль и водород , в расплаве — средняя соль и водород .
Обратите внимание! С щелочами в растворе реагируют только те металлы, у которых оксид с минимальной положительной степенью окисления металла амфотерный!
Например , железо не реагирует с раствором щёлочи, оксид железа (II) — основный. А алюминий растворяется в водном растворе щелочи, оксид алюминия — амфотерный:
2Al + 2NaOH + 6H 2 + O = 2Na + 3H 2 0
7. Щёлочи взаимодействуют с неметалами. При этом протекают окислительно-восстановительные реакции. Как правило, неметаллы диспропорционируют в щелочах . Не реагируют с щелочами кислород, водород, азот, углерод и инертные газы (гелий, неон, аргон и др.):
NaOH +О 2 ≠
NaOH +N 2 ≠
NaOH +C ≠
Сера, хлор, бром, йод, фосфор и другие неметаллы диспропорционируют в щелочах (т.е. самоокисляются-самовосстанавливаются).
Например , хлор при взаимодействии с холодной щелочью переходит в степени окисления -1 и +1:
2NaOH +Cl 2 0 = NaCl — + NaOCl + + H 2 O
Хлор при взаимодействии с горячей щелочью переходит в степени окисления -1 и +5:
6NaOH +Cl 2 0 = 5NaCl — + NaCl +5 O 3 + 3H 2 O
Кремний окисляется щелочами до степени окисления +4.
Например , в растворе:
2NaOH +Si 0 + H 2 + O= NaCl — + Na 2 Si +4 O 3 + 2H 2 0
Фтор окисляет щёлочи:
2F 2 0 + 4NaO -2 H = O 2 0 + 4NaF — + 2H 2 O
Более подробно про эти реакции можно прочитать в статье .
8. Щёлочи не разлагаются при нагревании.
Исключение — гидроксид лития:
2LiOH = Li 2 O + H 2 O