Гродно" href="/text/category/grodno/" rel="bookmark">Гродненский государственный медицинский университет», кандидат химических наук, доцент;
Доцент кафедры общей и биоорганической химии Учреждения образования «Гродненский государственный медицинский университет», кандидат биологических наук, доцент
Рецензенты:
Кафедра общей и биоорганической химии Учреждения образования «Гомельский государственный медицинский университет»;
– зав. кафедрой биоорганической химии Учреждение образования «Белорусский государственный медицинский университет», кандидат медицинских наук, доцент.
Кафедрой общей и биоорганической химии Учреждения образования «Гродненский государственный медицинский университет»
(протокол от 01.01.01 г.)
Центральным научно-методическим советом Учреждения образования «Гродненский государственный медицинский университет»
(протокол от 01.01.01 г.)
Секцией по специальности 1Медико-психологическое дело учебно-методического объединения вузов Республики Беларусь по медицинскому образованию
(протокол от 01.01.01 г.)
Ответственный за выпуск:
Первый проректор Учреждения образования «Гродненский государственный медицинский университет», профессор, доктор медицинских наук
Пояснительная записка
Актуальность изучения учебной дисциплины
«Биоорганическая химия»
Биоорганическая химия – это фундаментальная естественнонаучная дисциплина. Биоорганическая химия сформировалась как самостоятельная наука во 2-й половине XX века на стыке органической химии и биохимии . Актуальность изучения биоорганической химии обусловлена практическими задачами, стоящими перед медициной и сельским хозяйством (получение, витаминов , гормонов, антибиотиков , стимуляторов роста растений, регуляторов поведения животных и насекомых, других лекарственных средств), решение которых без использования теоретического и практического потенциала биоорганической химии невозможно.
Биоорганическая химия постоянно обогащается новыми методами выделения и очистки природных соединений, способами синтеза природных соединений и их аналогов, знаниями о взаимосвязи структуры и биологической активности соединений и т. д.
Новейшие подходы к медицинскому образованию, связанные с преодолением репродуктивного стиля в обучении, обеспечением познавательной и исследовательской активности студентов, открывают и новые перспективы для реализации потенциала как личности, так и коллектива .
Цель и задачи учебной дисциплины
Цель: формирование уровня химической компетентности в системе медицинского образования, обеспечивающего последующее изучение медико-биологических и клинических дисциплин.
Задачи:
Освоении студентами теоретических основ химических превращений органических молекул во взаимосвязи с их строением и биологической активностью;
Формирование: знаний молекулярных основ процессов жизнедеятельности;
Развития умений ориентироваться в классификации, строении и свойствах органических соединений, выступающих в роли лекарственных средств;
Формирование логики химического мышления;
Развитие умений использовать методы качественного анализа
органических соединений;
Химические знания и навыки, составляющие основу химической компетентности, будут способствовать формированию профессиональной компетенции выпускника.
Требования к освоению учебной дисциплины
Требования к уровню освоения содержания дисциплины «Биоорганическая химия» определены образовательным стандартом высшего образования первой ступени по циклу общих профессиональных и специальных дисциплин, который разработан с учетом требований компетентностного подхода, где указан минимум содержания по дисциплине в виде обобщенных химических знаний и умений, составляющих биоорганическую компетентность выпускника вуза:
а) обобщенные знания:
- понимать сущность предмета как науки и его связи с другими дисциплинами;
Значимость в понимании процессов метаболизма;
Концепцию единства структуры и реакционной способности органических молекул;
Фундаментальные законы химии, необходимые для объяснения процессов, протекающих в живых организмах;
Химические свойства и биологическую значимость основных классов органических соединений.
б) обобщенные умения:
Прогнозировать механизм реакции на основе знаний о строении органических молекул и способов разрыва химических связей;
Объяснять значение реакций для функционирования живых систем;
Использовать полученные знания при изучении биохимии, фармакологии и других дисциплин.
Структура и содержание учебной дисциплины
В данной программе структура содержания дисциплины «биоорганическая химия» состоит из введения в дисциплину и двух разделов, которые охватывают общие вопросы реакционной способности органических молекул, а также свойства гетеро- и полифункциональных соединений, участвующих в процессах жизнедеятельности. Каждый раздел делится на темы, расположенные в последовательности, обеспечивающей оптимальное изучение и усвоение программного материала. Для каждой темы представлены обобщенные знания и умения, составляющие суть биоорганической компетентности студентов. В соответствии с содержанием каждой темы определены требования к компетенциям (в виде системы обобщенных знаний и умений), для формирования и диагностики которых могут быть разработаны тесты.
Методы обучения
Основными методами обучения, адекватно отвечающими целям изучения данной дисциплины, являются:
Объяснение и консультация;
Лабораторное занятие;
Элементы проблемного обучения (учебно-исследовательская работа студентов);
Введение в биоорганическую химию
Биоорганическая химия как наука, изучающая строение органических веществ и их превращения во взаимосвязи с биологическими функциями. Объекты изучения биоорганической химии. Роль биоорганической химии в формировании научной основы для восприятия биологических и медицинских знаний на современном молекулярном уровне.
Теория строения органических соединений и ее развитие на современном этапе. Изомерия органических соединений как основа многообразия органических соединений. Типы изомерии органических соединений.
Физико-химические методы выделения и исследования органических соединений, имеющие значение для биомедицинского анализа.
Основные правила систематической номенклатуры IUPAC для органических соединений: заместительная и радикально-функциональная номенклатура.
Пространственное строение органических молекул, его связь с типом гибридизации атома углерода (sp3-, sp2- и sp-гибридизация). Стереохимические формулы. Конфигурация и конформация. Конформации открытых цепей (заслоненная, заторможенная, скошенная). Энергетическая характеристика конформаций. Проекционные формулы Ньюмена. Пространственное сближение определенных участков цепи как следствие конформационного равновесия и как одна из причин преимущественного образования пяти - и шестичленных циклов. Конформации циклических соединений (циклогексан, тетрагидропиран). Энергетическая характеристика конформаций кресла и ванны. Аксиальные и экваториальные связи. Связь пространственного строения с биологической активностью.
Требования к компетентности:
· Знать объекты изучения и основные задачи биоорганической химии,
· Уметь классифицировать органические соединения по строению углеродного скелета и по природе функциональных групп, пользоваться правилами систематической химической номенклатуры.
· Знать основные типы изомерии органических соединений, уметь по структурной формуле соединения определять возможные типы изомеров.
· Знать разные типы гибридизации атомных орбиталей углерода, пространственную направленность связей атома, их тип и число в зависимости от типа гибридизации.
· Знать энергетические характеристики конформаций циклических (конформации кресла, ванны) и ациклических (заторможенная, скошенная, заслоненная конформации) молекул, уметь их изображать проекционными формулами Ньюмена.
· Знать виды напряжений (торсионные, угловые, ван-дер-ваальсовые), возникающие в различных молекулах, их влияние на устойчивость конформации и молекулы в целом.
Раздел 1. Реакционная способность органических молекул как результат взаимного влияния атомов, механизмы протекания органических реакций
Тема 1. Сопряженные системы, ароматичность, электронные эффекты заместителей
Сопряженные системы и ароматичность. Сопряжение (p, p - и р, p-сопряжение). Сопряженные системы с открытой цепью: 1,3-диены (бутадиен, изопрен), полиены (каротиноиды, витамин А). Сопряженные системы с замкнутой цепью. Ароматичность: критерии ароматичности, правило ароматичности Хюккеля. Ароматичность бензоидных (бензол, нафталин, фенантрен) соединений. Энергия сопряжения. Строение и причины термодинамической устойчивости карбо - и гетероциклических ароматических соединений. Ароматичность гетероциклических (пиррол, имидазол, пиридин, пиримидин, пурин) соединений. Пиррольный и пиридиновый атомы азота , p-избыточные и p-недостаточные ароматические системы.
Взаимное влияние атомов и способы его передачи в органических молекулах. Делокализация электронов как один из факторов повышения устойчивости молекул и ионов, ее широкая распространенность в биологически важных молекулах (порфин, гем, гемоглобин и др.). Поляризация связей. Электронные эффекты заместителей (индуктивный и мезомерный) как причина неравномерного распределения электронной плотности и возникновения реакционных центров в молекуле. Индуктивный и мезомерный эффекты (положительный и отрицательный), их графическое обозначение в структурных формулах органических соединений. Электронодонорные и электроноакцепторные заместители.
Требования к компетентности:
· Знать виды сопряжения и уметь определять вид сопряжения по структурной формуле соединения.
· Знать критерии ароматичности, уметь по структурной формуле определять принадлежность к ароматическим соединениям карбо - и гетероциклических молекул.
· Уметь оценивать электронный вклад атомов в создание единой сопряженной системы, знать электронное строение пиридинового и пиррольного атомов азота.
· Знать электронные эффекты заместителей, причины их возникновения и уметь графически изображать их действие.
· Уметь относить заместители к электронодонорным или электроноакцепторным на основании проявляемых ими индуктивного и мезомерного эффектов.
· Уметь прогнозировать влияние заместителей на реакционную способность молекул.
Тема 2. Реакционная способность углеводородов. Реакции радикального замещения, электрофильного присоединения и замещения
Общие закономерности реакционной способности органических соединений как химическая основа их биологического функционирования. Химическая реакция как процесс. Понятия: субстрат, реагент, реакционный центр, переходное состояние, продукт реакции, энергия активации , скорость реакции, механизм.
Классификация органических реакций по результату (присоединения, замещения, элиминирования, окислительно-восстановительные) и по механизму – радикальные, ионные (электрофильные, нуклеофильные), согласованные. Типы реагентов: радикальные, кислотные, основные, электрофильные, нуклеофильные. Гомолитический и гетеролитический разрыв ковалентной связи в органических соединениях и образующиеся при этом частицы: свободные радикалы, карбкатионы и карбанионы. Электронное и пространственное строение этих частиц и факторы, обусловливающие их относительную устойчивость.
Реакционная способность углеводородов. Реакции радикального замещения: гомолитические реакции с участием СН-связей sp3- гибридизированного атома углерода. Механизм радикального замещения на примере реакции галогенирования алканов и циклоалканов. Понятие о цепных процессах. Понятие о региоселективности.
Пути образования свободных радикалов: фотолиз, термолиз, окислительно-восстановительные реакции.
Реакции электрофильного присоединения (AE ) в ряду непредельных углеводородов: гетеролитические реакции с участием p-связи между sp2-гибридизированными атомами углерода. Механизм реакций гидратации и гидрогалогенирования. Кислотный катализ. Правило Марковникова. Влияние статических и динамических факторов на региоселективность реакций электрофильного присоединения. Особенности реакций электрофильного присоединения к диеновым углеводородам и малым циклам (циклопропан, циклобутан).
Реакции электрофильного замещения (SE ): гетеролитические реакции с участием p-электронного облака ароматической системы. Механизм реакций галогенирования, нитрования, алкилирования ароматических соединений: p - и s - комплексы. Роль катализатора (кислоты Льюиса) в образовании электрофильной частицы.
Влияние заместителей в ароматическом ядре на реакционную способность соединений в реакциях электрофильного замещения. Ориентирующее влияние заместителей (ориентанты I и II рода).
Требования к компетентности:
· Знать понятия субстрат, реагент, реакционный центр, продукт реакции, энергия активации, скорость реакции, механизм реакции.
· Знать классификацию реакций по различным признакам (по конечному результату, по способу разрыва связей, по механизму) и типы реагентов (радикальные, электрофильные, нуклеофильные).
· Знать электронное и пространственное строение реагентов и факторы, обусловливающие их относительную устойчивость, уметь сравнивать относительную устойчивость однотипных реагентов.
· Знать способы образования свободных радикалов и механизм реакций радикального замещения (SR) на примерах реакций галогенирования алканов и циклоалаканов.
· Уметь определять статистическую вероятность образования возможных продуктов в реакциях радикального замещения и возможность региоселективного протекания процесса.
· Знать механизм реакций электрофильного присоединения (АЕ) в реакциях галогенирования, гидрогалогенирования и гидратации алкенов, уметь качественно оценивать реакционную способность субстратов, исходя из электронных эффектов заместителей.
· Знать правило Марковникова и уметь определять региоселективность протекания реакций гидратации и гидрогалогенирования исходя из влияния статического и динамического факторов.
· Знать особенности реакций электрофильного присоединения к сопряженным диеновым углеводородам и малым циклам (циклопропан, циклобутан).
· Знать механизм реакций электрофильного замещения (SЕ) в реакциях галогенирования, нитрования, алкилирования, ацилирования ароматических соединений.
· Уметь исходя из электронных эффектов заместителей, определять их влияние на реакционную способность ароматического ядра и их ориентирующее действие.
Тема 3. Кислотно-основные свойства органических соединений
Кислотность и основность органических соединений: теории Бренстеда и Льюиса. Стабильность аниона кислоты – качественный показатель кислотных свойств. Общие закономерности в изменении кислотных или основных свойств во взаимосвязи с природой атомов в кислотном или основном центре, электронными эффектами заместителей при этих центрах. Кислотные свойства органических соединений с водородсодержащими функциональными группами (спирты, фенолы, тиолы, карбоновые кислоты, амины, СН-кислотность молекул и кабркатионов). p-основания и n -основания. Основные свойства нейтральных молекул, содержащих гетероатомы с неподеленными парами электронов (спирты, тиолы, сульфиды, амины) и анионов (гидроксид-, алкоксид-ионы, анионы органических кислот). Кислотно-основные свойства азотсодержащих гетероциклов (пиррол, имидазол, пиридин). Водородная связь как специфическое проявление кислотно-основных свойств.
Сравнительная характеристика кислотных свойств соединений, содержащих гидроксильную группу (одноатомные и многоатомные спирты, фенолы, карбоновые кислоты). Сравнительная характеристика основных свойств алифатических и ароматических аминов. Влияние электронной природы заместителя на кислотно-основные свойства органических молекул.
Требования к компетентности:
· Знать определения кислот и оснований согласно протолитической теории Бренстеда и электронной теории Льюиса.
· Знать классификацию кислот и оснований Бренстеда в зависимости от природы атомов кислотного или основного центров.
· Знать факторы, влияющие на силу кислот и стабильность сопряженных им оснований, уметь проводить сравнительную оценку силы кислот исходя из стабильности соответствующих им анионов.
· Знать факторы, влияющие на силу оснований Бренстеда, уметь проводить сравнительную оценку силы оснований с учетом этих факторов.
· Знать причины возникновения водородной связи, уметь трактоватьобразование водородной связи как специфическое проявление кислотно-основных свойств вещества.
· Знать причины возникновения кето-енольной таутомерии в органических молекулах, уметь объяснять их с позиции кислотно-основных свойств соединений во взаимосвязи с их биологической активностью.
· Знать и уметь проводить качественные реакции, позволяющие отличать многоатомные спирты, фенолы, тиолы.
Тема 4. Реакции нуклеофильного замещения у тетрагонального атома углерода и конкурентные им реакции элиминирования
Реакции нуклеофильного замещения у sp3-гибридизированного атома углерода: гетеролитические реакции, обусловленные поляризацией связи углерод-гетероатом (галогенопроизводные, спирты). Легко и трудно уходящие группы: связь легкости ухода группы с ее строением. Влияние растворителя, электронных и пространственных факторов на реакционную способность соединений в реакциях моно - и бимолекулярного нуклеофильного замещения (SN1 и SN2). Стереохимия реакций нуклеофильного замещения.
Реакции гидролиза галогенопроизводных. Реакции алкилирования спиртов, фенолов, тиолов, сульфидов, аммиака , аминов. Роль кислотного катализа в нуклеофильном замещении гидроксильной группы. Галогенопроизводные, спирты, эфиры серной и фосфорной кислот как алкилирующие реагенты. Биологическая роль реакций алкилирования.
Реакции моно - и бимолекулярного элиминирования (Е1 и Е2): (дегидратация, дегидрогалогенирование). Повышенная СН-кислотность как причина реакций элиминирования, сопровождающих нуклеофильное замещение у sp3- гибридизированного атома углерода.
Требования к компетентности:
· Знать факторы, определяющие нуклеофильность реагентов, строение важнейших нуклеофильных частиц.
· Знать общие закономерности реакций нуклеофильного замещения у насыщенного атома углерода, влияние статического и динамического факторов на реакционную способность вещества в реакции нуклеофильного замещения.
· Знать механизмы моно - и бимолекулярного нуклеофильного замещения, уметь оценивать влияние стерических факторов, влияние растворителей, влияние статического и динамического факторов на протекание реакции по одному из механизмов.
· Знать механизмы моно - и бимолекулярного элиминирования, причины конкуренции между реакциями нуклеофильного замещения и элиминирования.
· Знать правило Зайцева и уметь определять главный продукт в реакциях дигидратации и дегидрогалогенирования несимметричных спиртов и галогеналканов.
Тема 5. Реакции нуклеофильного присоединения и замещения у тригонального атома углерода
Реакции нуклеофильного присоединения: гетеролитические реакции с участием p-связи углерод-кислород (альдегиды, кетоны). Механизм реакций взаимодействия карбонильных соединений с нуклеофильными реагентами (водой, спиртами, тиолами, аминами). Влияние электронных и пространственных факторов, роль кислотного катализа, обратимость реакций нуклеофильного присоединения. Полуацетали и ацетали, их получение и гидролиз. Биологическая роль реакций ацетализации. Реакции альдольного присоединения. Основной катализ. Строение енолят - иона.
Реакции нуклеофильного замещения в ряду карбоновых кислот. Электронное и пространственное строение карбоксильной группы. Реакции нуклеофильного замещения у sp2-гибридизированного атома углерода (карбоновые кислоты и их функциональные производные). Ацилирующие агенты (галогенангидриды, ангидриды, карбоновые кислоты, сложные эфиры, амиды), сравнительная характеристика их реакционной способности. Реакции ацилирования – образования ангидридов, сложных эфиров, тиоэфиров, амидов – и обратные им реакции гидролиза. Ацетилкофермент А – природный макроэргический ацилирующий агент. Биологическая роль реакций ацилирования. Понятие о нуклеофильном замещении у атомов фосфора, реакции фосфорилирования.
Реакции окисления и восстановления органических соединений. Специфика окислительно-восстановительных реакций органических соединений. Понятие об одноэлектронном переносе, переносе гидрид-иона и действии системы НАД+ ↔ НАДН. Реакции окисления спиртов, фенолов, сульфидов, карбонильных соединений, аминов, тиолов. Реакции восстановления карбонильных соединений, дисульфидов. Роль окислительно-восстановительных реакций в процессах жизнедеятельности.
Требования к компетентности:
· Знать электронное и пространственное строение карбонильной группы, влияние электронных и стерических факторов на реакционную способность оксо-группы в альдегидах и кетонах.
· Знать механизм реакций нуклеофильного присоединения воды, спиртов, аминов, тиолов к альдегидам и кетонам, роль катализатора.
· Знать механизм реакций альдольной конденсации, факторы, определяющие участие соедения в этой реакции.
· Знать механизм реакций восстановления оксосоединений гидридами металлов.
· Знать реакционные центры, имеющиеся в молекулах карбоновых кислот. Уметь проводить сравнительную оценку силы карбоновых кислот в зависимости от строения радикала.
· Знать электронное и пространственное строение карбоксильной группы, уметь проводить сравнительную оценку способности атома углерода оксо-группы в карбоновых кислотах и их функциональных производных (галогенангидриды, ангидриды, сложные эфиры, амиды, соли) подвергаться нуклеофильной атаке.
· Знать механизм реакций нуклефильного замещения на примерах реакций ацилирования, этерификации, гидролиза сложных эфиров, ангидридов, галогенангидридов, амидов.
Тема 6. Липиды, классификация, строение, свойства
Липиды омыляемые и неомыляемые. Нейтральные липиды. Естественные жиры как смесь триацилглицеринов. Основные природные высшие жирные кислоты, входящие в состав липидов: пальмитиновая, стеариновая, олеиновая, линолевая, линоленовая. Арахидоновая кислота. Особенности ненасыщенных жирных кислот, w-номенклатура.
Пероксидное окисление фрагментов ненасыщенных жирных кислот в клеточных мембранах. Роль пероксидного окисления липидов мембран в действии малых доз радиации на организм. Системы антиоксидантной защиты.
Фосфолипиды. Фосфатидные кислоты. Фосфатидилколамины и фосфатидилсерины (кефалины), фосфатидилхолины (лецитины) – структурные компоненты клеточных мембран. Липидный бислой. Сфинголипиды, церамиды, сфингомиелины. Гликолипиды мозга (цереброзиды, ганглиозиды).
Требования к компетентности:
· Знать классификацию липидов, их строение.
· Знать строение структурных компонентов омыляемых липидов – спиртов и высших жирных кислот.
· Знать механизм реакций образования и гидролиза простых и сложных липидов.
· Знать и уметь проводить качественные реакции на непредельные жирные кислоты и масла.
· Знать классификацию неомыляемых липидов, иметь представления о принципах классификации терпенов и стероидов, их биологической роли.
· Знать биологическую роль липидов, их основные функции, иметь представления об основных этапах перекисного окисления липидов и последствиях этого процесса для клетки.
Раздел 2. Стереоизомерия органических молекул. Поли - и гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Тема 7. Стереоизомерия органических молекул
Стереоизомерия в ряду соединений с двойной связью (p-диастереомерия). Цис - и транс-изомерия непредельных соединений. Е, Z – система обозначений p-диастереомеров. Сравнительная устойчивость p-диастереомеров.
Хиральные молекулы. Ассиметрический атом углерода как центр хиральности. Стереоизомерия молекул с одним центром хиральности (энантиомерия). Оптическая активность. Проекционные формулы Фишера. Глицериновый альдегид как конфигурационный стандарт, абсолютная и относительная конфигурация. D, L-система стереохимической номенклатуры. R, S-система стереохимиеской номенклатуры. Рацемические смеси и способы их разделения.
Стереоизомерия молекул с двумя и более центрами хиральности. Энантиомеры, диастереомеры, мезоформы.
Требования к компетентности:
· Знать причины возникновения стереоизомерии в ряду алкенов и диеновых углеводородов.
· Уметь по сокращенной структурной формуле непредельного соединения определять возможность существования p-диастереомеров, различать цис - транс –изомеры, оценивать их сравнительную устойчивость.
· Знать элементы симметрии молекул, необходимые условия для возникновения хиральности у органической молекулы.
· Знать и уметь изображать энантиомеры с помощью проекционных формул Фишера, высчитывать число ожидаемых стереоизомеров исходя из числа хиральных центров в молекуле, принципы определения абсолютной и относительной конфигурации, D - , L-систему стереохимической номенклатуры.
· Знать способы разделения рацематов, основные принципы R, S-системы стереохимической номенклатуры.
Тема 8. Физиологически активные поли - и гетерофункциональные соединения алифатического, ароматического и гетероциклического рядов
Поли - и гетерофункциональность как один из характерных признаков органических соединений, участвующих в процессах жизнедеятельности и являющихся родоначальниками важнейших групп лекарственных средств. Особенности во взаимном влиянии функциональных групп в зависимости от их относительного расположения.
Многоатомные спирты: этиленгликоль, глицерин. Сложные эфиры многоатомных спиртов с неорганическими кислотами (нитроглицерин, фосфаты глицерина). Двухатомные фенолы: гидрохинон. Окисление двухатомных фенолов. Система гидрохинон-хинон. Фенолы как антиоксиданты (ловушки свободных радикалов). Токоферолы.
Двухосновные карбоновые кислоты: щавелевая, малоновая, янтарная, глутаровая, фумаровая. Превращение янтарной кислоты в фумаровую как пример биологически важной реакции дегидрирования. Реакции декарбоксилирования, их биологическая роль.
Аминоспирты: аминоэтанол (коламин), холин, ацетилхолин. Роль ацетилхолина в химической передаче нервного импульса в синапсах. Аминофенолы: дофамин, норадреналин, адреналин . Понятие о биологической роли этих соединений и их производных. Нейротоксическое действие 6-гидроксидофамина и амфетаминов.
Гидрокси- и аминокислоты. Реакции циклизации: влияние различных факторов на процесс образования циклов (реализация соответствующих конформаций, размер образующегося цикла, энтропийный фактор). Лактоны. Лактамы. Гидролиз лактонов и лактамов. Реакция элиминирования b-гидрокси и аминокислот.
Альдегидо - и кетокислоты: пировиноградная, ацетоуксусная, щавелевоуксусная, a-кетоглутаровая. Кислотные свойства и реакционная способность. Реакции декарбоксилирования b-кетокислот и окислительного декарбоксилирования a-кетокислот. Ацетоуксусный эфир, кето-енольная таутомерия. Представители «кетоновых тел» - b-гидроксимасляная, b-кетомасляная кислоты, ацетон , их биологическое и диагностическое значение.
Гетерофункциональные производные бензольного ряда как лекарственные средства. Салициловая кислота и ее производные (ацетилсалициловая кислота).
Пара-аминобензойная кислота и ее производные (анестезин, новокаин). Биологическая роль п-аминобензойной кислоты. Сульфаниловая кислота и ее амид (стрептоцид).
Гетероциклы с несколькими гетероатомами. Пиразол, имидазол, пиримидин, пурин. Пиразолон-5 – основа ненаркотических анальгетиков. Барбитуровая кислота и ее производные. Гидроксипурины (гипоксантин, ксантин, мочевая кислота), их биологическая роль. Гетероциклы с одним гетероатомом. Пиррол, индол, пиридин. Биологически важные производные пиридина – никотинамид, пиридоксаль, производные изоникотиновой кислоты. Никотинамид – структурный компонент кофермента НАД+, обуславливающий его участие в ОВР.
Требования к компетентности:
· Уметь классифицировать гетерофункциональные соединения по составу и по их взаимному расположению.
· Знать специфические реакции амино- и гидроксикислот с a, b, g - расположением функциональных групп.
· Знать реакции, ведущие к образованию биологически активных соединений: холина, ацетилхолина, адреналина.
· Знать роль кето-енольной таутомерии в проявлении биологической активности кетокислот (пировиноградной, щавелевоуксусной, ацетоуксусной) и гетероциклических соединений (пиразола, барбитуровой кислоты, пурина).
· Знать способы окислительно-восстановительных превращений органических соединений, биологическую роль окислительно-восстановительных реакций в проявлении биологической активности двухатомных фенолов, никотинамида, образовании кетоновых тел.
Тема 9 . Углеводы, классификация, строение, свойства, биологическая роль
Углеводы, их классификация по отношению к гидролизу. Классификация моносахаридов. Альдозы, кетозы: триозы, тетрозы, пентозы, гексозы. Стереоизомерия моносахаридов. D - и L-ряды стереохимической номенклатуры. Открытые и циклические формы. Формулы Фишера и формулы Хеуорса. Фуранозы и пиранозы, a - и b-аномеры. Цикло-оксо-таутомерия. Конформации пиранозных форм моносахаридов. Строение наиболее важных представителей пентоз (рибоза, ксилоза); гексоз (глюкоза, манноза, галактоза, фруктоза); дезоксисахаров (2-дезоксирибоза); аминосахаров (глюкозамин, маннозамин, галактозамин).
Химические свойства моносахаридов. Реакции нуклеофильного замещения с участием аномерного центра. О - и N-гликозиды. Гидролиз гликозидов. Фосфаты моносахаридов. Окисление и восстановление моносахаридов. Восстановительные свойства альдоз. Гликоновые, гликаровые, гликуроновые кислоты.
Олигосахариды. Дисахариды: мальтоза, целлобиоза, лактоза, сахароза. Строение, цикло-оксо-таутомерия. Гидролиз.
Полисахариды. Общая характеристика и классификация полисахаридов. Гомо - и гетерополисахариды. Гомополисахариды: крахмал, гликоген, декстраны, целлюлоза. Первичная структура, гидролиз. Понятие о вторичной структуре (крахмал, целлюлоза).
Требования к компетентности:
· Знать классификацию моносахаридов (по числу атомом углерода, по составу функциональных групп), строение открытых и циклических форм (фуранозы, пиранозы) важнейших моносахаридов, их отношение D - и L - рядам стереохимической номенклатуры, уметь определять число возможных диастереомеров, относить стереоизомеры к диастереомерам, эпимерам, аномерам.
· Знать механизм реакций циклмизации моносахаридов, причины мутаротации растворов моносахаридов.
· Знать химические свойства моносахаридов: окислительно-восстановительные реакции, реакции образования и гидролиза О - и N-гликозидов, реакции этерификации, фосфорилирования.
· Уметь проводить качественные реакции на диольный фрагмент и наличие восстанавливающих свойств моносахаридов.
· Знать классификацию дисахаридов и их строение, конфигурацию аномерного атома углерода, образующего гликозидную связь, таутомерные превращения дисахаридов, их химические свойства, биологическую роль.
· Знать классификацию полисахаридов (по отношению к гидролизу, по моносахаридному составу), строение важнейших представителей гомополисахаридов, конфигурацию аномерного атома углерода, образующего гликозидную связь, их физические ихимические свойства, биологическую роль. Иметь представления о биологической роли гетерополисахаридов.
Тема 10. a -Аминокислоты, пептиды, белки. Строение, свойства, биологическая роль
Строение, номенклатура, классификация a-аминокислот, входящих в состав белков и пептидов. Стереоизомерия a-аминокислот.
Биосинтетические пути образования a-аминокислот из оксокислот: реакции восстановительного аминирования и реакции переаминирования. Незаменимые аминокислоты.
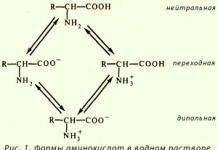
Химические свойства a-аминокислот как гетерофункциональных соединений. Кислотно-основные свойства a-аминокислот. Изоэлектрическая точка, методы разделения a-аминокислот. Образование внутрикомплексных солей. Реакции этерификации, ацилирования, алкилирования. Взаимодействие с азотистой кислотой и формальдегидом, значение этих реакций для анализа аминокислот.
g-Аминомасляная кислота – тормозной медиатор ЦНС. Антидепрессивное действие L-триптофана, серотонин – как нейромедиатор сна. Медиаторные свойства глицина, гистамина, аспарагиновой и глутаминовой кислот.
Биологически важные реакции a-аминокислот. Реакции дезаминирования и гидроксилирования. Декарбоксилирование a-аминокислот – путь к образованию биогенных аминов и биорегуляторов (коламин, гистамин, триптамин, серотонин.) Пептиды. Электронное строение пептидной связи. Кислотный и щелочной гидролиз пептидов. Установление аминокислотного состава с помощью современных физико-химических методов (методы Сенгера и Эдмана). Понятие о нейропептидах.
Первичная структура белков. Частичный и полный гидролиз. Понятие о вторичной, третичной и четвертичной структурах.
Требования к компетентности:
· Знать строение, стереохимическую классификацию a-аминокислот, принадлежность к D - и L-стереохимическим рядам природных аминокислот, незаменимые аминокислоты.
· Знать пути синтеза a-аминокислот in vivo и in vitro, знать кислотно-основные свойства и способы перевода a-аминокислот в изоэлектрическое состояние.
· Знать химические свойства a-аминокислот (реакции по амино - и карбоксильной группам), уметь проводить качественные реакции (ксантопротеиновую, с Сu(ОН)2, нингидрином).
· Знать электронное строение пептидной связи, первичную, вторичную, третичную и четвертичную структуру белков и петидов, знать способы определения аминокислотного состава и аминокислотной последовательности (метод Сенгера, метод Эдмана), уметь проводить биуретовую реакцию на пептиды и белки.
· Знать принцип метода синтеза пептидов с использованием защиты и активации функциональных групп.
Тема 11. Нуклеотиды и нуклеиновые кислоты
Нуклеиновые основания, входящие в состав нуклеиновых кислот. Пиримидиновые (урацил, тимин, цитозин) и пуриновые (аденин, гуанин) основания, их ароматичность, таутомерные превращения.
Нуклеозиды, реакции их образования. Характер связи нуклеинового основания с углеводным остатком; конфигурация гликозидного центра. Гидролиз нуклеозидов.
Нуклеотиды. Строение мононуклеотидов, образующих нуклеиновые кислоты. Номенклатура. Гидролиз нуклеотидов.
Первичная структура нуклеиновых кислот. Фосфодиэфирная связь. Рибонуклеиновые и дезоксирибонуклеиновые кислоты. Нуклеотидный состав РНК и ДНК. Гидролиз нуклеиновых кислот.
Понятие о вторичной структуре ДНК. Роль водородных связей в формировании вторичной структуры. Комплементарность нуклеиновых оснований.
Лекарственные средства на основе модифицированных нуклеиновых оснований (5-фторурацил, 6-меркаптопурин). Принцип химического подобия. Изменение структуры нуклеиновых кислот под действием химических веществ и радиации. Мутагенное действие азотистой кислоты.
Нуклеозидполифосфаты (АДФ, АТФ), особенности их строения, позволяющие выполнять функции макроэргических соединений и внутриклеточных биорегуляторов. Строение цАМФ – внутриклеточного «посредника» гормонов.
Требования к компетентности:
· Знать строение пиримидиновых и пуриновых азотистых оснований, их таутомерные превращения.
· Знать механизм реакций образования N-гликозидов (нуклеозидов) и их гидролиза, номенклатуру нуклеозидов.
· Знать принципиальные сходство и различия природных и синтетических нуклеозидов-антибиотиков в сравнении с нуклеозидами, входящимив состав ДНК и РНК.
· Знать реакции образования нуклеотидов, строение мононуклеотидов, входящих в состав нуклеиновых кислот, их номенклатуру.
· Знать строение цикло - и полифосфатов нуклеозидов, их биологическую роль.
· Знать нуклетидный состав ДНК и РНК, роль фосфодиэфирной связи в создании первичной структуры нуклеиновых кислот.
· Знать роль водородных связей в формировании вторичной структуры ДНК, комплементарность азотистых оснований, роль комплементарных взаимодействий в осуществлении биологической функции ДНК.
· Знать факторы, вызывающие возникновения мутаций, и принцип их действия.
Информационная часть
Список литературы
Основная:
1. Романовский, биоорганической химии: учебное пособие в 2-х частях / . - Минск: БГМУ, 20с.
2. Романовский, к практикуму по биоорганической химии: учебное пособие / под редакцией. – Минск: БГМУ, 1999. – 132 с.
3. Тюкавкина, Н. А., Биоорганическая химия: учебник / , . – Москва: Медицина, 1991. – 528 с.
Дополнительная:
4. Овчинников, химия: монография / .
– Москва: Просвещение, 1987. – 815 с.
5. Потапов, : учебное пособие / . - Москва:
Химия, 1988. – 464 с.
6. Райлс, А. Основы органической химии: учебное пособие / А. Райс, К. Смит,
Р. Уорд. – Москва: Мир, 1989. – 352 с.
7. Тейлор, Г. Основы органической химии: учебное пособие / Г. Тейлор. -
Москва: Мирс.
8. Терней, А. Современная органическая химия: учебное пособие в 2-х томах /
А. Терней. – Москва: Мир, 1981. – 1310 с.
9. Тюкавкина, к лабораторным занятиям по биоорганической
химии: учебное пособие / [и др.]; под редакцией Н. А.
Тюкавкиной. – Москва: Медицина, 1985. – 256 с.
10. Тюкавкина, Н. А., Биоорганическая химия: Учебник для студентов
медицинских институтов / , . – Москва.
План 1. Предмет и значение биоорганической химии 2. Классификация и номенклатура органических соединений 3. Способы изображения органических молекул 4. Химическая связь в биоорганических молекулах 5. Электронные эффекты. Взаимное влияние атомов в молекуле 6. Классификация химических реакций и реагентов 7. Понятие о механизмах химических реакций 2

Предмет биоорганической химии 3 Биоорганическая химия самостоятельный раздел химической науки, что изучает строение, свойства и биологические функции химических соединений органического происхождения, которые принимают участие в обмене веществ живых организмов.

Обектами изучения биоорганической химии являются низкомолекулярные биомолекулы и биополимеры (белки, нуклеиновые кислоты и полисахариды), биоре-гуляторы (ферменты, гормоны, витамины и другие), природные и синтетические физиологически активные соединения, в том числе лекарственные средства и вещества с токсичным действием. Биомолекулы - биоорганические соединения, которые входят в состав живых организмов и специализированные для образования клеточных структур и участия в биохимических реакциях, составляют основу обмена веществ (метаболизм) и физиологических функций живых клеток и многоклеточных организмов в целом. 4 Классификация биоорганических соединений

Обмен веществ - совокупность химических реакций, которые протекают в организме (in vivo). Обмен веществ называют также метаболизмом. Метаболизм может происходить в двух направлениях – анаболизм и катаболизм. Анаболизм - это синтез в организме сложных веществ из сравнительно простых. Он протекает с затратой энергии (эндотермический процесс). Катаболизм - напротив, распад сложных органических соединений на более простые. Проходит он с выделением энергии (экзотермический процесс). Метаболитические процессы проходят при участии ферментов. Ф е р м е н т ы исполняют в организме роль био катализаторов. Без ферментов биохимические процессы или совсем не протекали бы, или протекали бы очень медленно и организм не смог бы поддерживать жизнь. 5

Биоэлементы. В состав биоорганических соединений, кроме атомов углерода (С), которые составляют основу любой органической молекулы, входят также водород (Н), кислород (О), азот (N), фосфор (Р) и сера (S). Эти биоэлементы (органогены) сконцентрированы в живых организмах в количестве, что свыше 200 раз превышает их содержание в объектах неживой природы. Отмеченные элементы составляют свыше 99% элементного состава биомолекул. 6


Биоорганическая химия возникла из недр органической химии и базируется на ее идеях и методах. В истории развития для органической химии отведены такие этапы: эмпирический, аналитический, структурный и современный. Период от первого знакомства человека с органическими веществами до конца XVІІІ века считается эмпирическим. Основной итог этого периода – люди осознали значение элементного анализа и установление атомных и молекулярных масс. Теория витализма - жизненной силы (Берцелиус). До 60-х годов XІX века продолжался аналитический период. Он ознаменовался тем, что с конца первой четверти XІX века были сделаны ряд перспективных открытий, которые нанесли сокрушительный удар по виталистической теории. Первым в этом ряду был ученик Берцелиуса, немецкий химик Велер. Он осуществил ряд открытий в 1824 г. – синтез щавелевой кислоты из дициана: (CN) 2 НООС – СООН р. – синтез мочевины из аммония цианата: NH 4 CNO NH 2 – C – NH 2 О 8

В 1853 Ш. Жерар разработал «теорию типов» и и пользовал её для классификации органических соединений. Согласно Жерару, более сложные органические соединения могут быть произведены от следующих основных четырёх типов веществ: НННН тип ВОДОРОДА НННН O тип ВОДЫ Н Cl тип ХЛОРИСТОГО ВОДОРОДА ННHННH N тип АММИАКА С 1857 по предложению Ф. А. Кекуле углеводороды стали относить к типу метана ННHНННHН С 9

Основные положения теории строения органических соединений (1861) 1) атомы в молекулах соединены друг с другом химическими связями в соответствии с их валентностью; 2) атомы в молекулах органических веществ соединяются между собой в определенной последовательности, что обусловливает химическое строение (структуру) молекулы; 3) свойства органических соединений зависят не только от числа и природы входящих в их состав атомов, но и от химического строения молекул; 4) в органических молекулах существует взаимодействие между атомами, как связанными друг с другом, так и несвязанными; 5) химическое строение вещества можно определить в результате изучения его химических превращений и, наоборот, по строению вещества можно характеризовать его свойства. 10

Основные положения теории строения органических соединений (1861) Структурная формула это изображение последовательности связи атомов в молекуле. Брутто-формула – СН 4 О или CH 3 OH Структурная формула Упрощенные формулы строения иногда называют рациональными Молекулярная формула - формула органического соединения, которая указывает на количество атомов каждого элемента в молекуле. Например: С 5 Н 12 – пентан, С 6 Н 6 – бензин и т.д. 11



Етапы развития биоорганической химии Как отдельная область знаний, которая совмещает концептуальные принципы и методологию органической химии с одной стороны и молекулярной биохимии и молекулярной фармакологии с другой стороны, биоорганическая химия сформировалась в годах ХХ столетия на основании разработок химии природных веществ и биополимеров. Фундаментальное значение современная биоорганическая химия приобрела благодаря работам В. Стейна, С. Мура, Ф. Сенгера (анализ аминокислотного состава и определение первичной структуры пептидов и белков), Л. Полинга и Х. Астбери (выяснение строения -спирали и -структуры и их значение в реализации биологических функций белковых молекул), Е. Чаргаффа (расшифровывание особенностей нуклеотидного состава нуклеиновых кислот), Дж. Уотсона, Фр. Крика, М. Уилкинса, Р. Франклина (установление закономерностей пространственной структуры молекулы ДНК), Г. Корани (химический синтез гена) и т.д. 14

Классификация органических соединений по строению углеродного скелета и природе функциональной группы Огромное число органических соединений побудило химиков провести их классификацию. В основу классификации органических соединений положены два классификационных признака: 1. Строение карбонового скелета 2. Природа функциональных групп Классификация по способу строения карбонового скелета: 1. Ациклические (алканы, алкены, алкины, алкадиены); 2. Циклические 2.1. Карбоциклические (алициклические и ароматические) 2.2. Гетероциклические 15 Ациклические соединения называют еще алифатическими. К ним принадлежат вещества с незамкнутой углеродной цепью. Ациклические соединения делят на насыщенные (или предельные) С n H 2n+2 (алканы, парафины) и ненасыщенные (непредельные). К последним относят алкены С n H 2n, алкины С n H 2n -2, алкадиены С n H 2n -2.

16 Циклические соединения в составе своих молекул содержат кольца (циклы). Если в состав циклов входят лишь атомы углерода, то такие соединения называют карбоциклическими. В свою очередь карбоциклические соединения разделяют на алициклические и ароматические. К алициклическим углеводородам (циклоалканы) относят циклопропан и его гомологи - циклобутан, циклопентан, циклогексан и так далее. Если же в циклическую систему кроме углеводорода входят и другие элементы, то такие соединения относят к гетероциклическим.

Классификация по природе функциональной группы Функциональная группа – это атом или группа определенным образом связанных атомов, наличие которых в молекуле органического вещества определяет характерные свойства и его принадлежность к тому или другому классу соединений. По количеству и однородности функциональных групп органические соединения делят на моно-, поли- и гетерофункциональные. Вещества с одной функциональной группой называют монофунк-циональными, с несколькими одинаковыми функциональными группами полифункциональными. Соединения, содержащие несколько различных функциональных групп гетеро функциональными. Важно, что соединения одного класса объединены в гомологические ряды. Гомологический ряд это ряд органических соединений с одинаковыми функциональными группами и однотипным строением, каждый представитель гомологического ряда отличается от предыдущего на постоянную единицу (СН 2), которую называют гомологической разностью. Члены гомологического ряда называют гомологами. 17

Номенклатурные системы в органической химии – тривиальная, рациональная и международная (IUPAC) Химическая номенклатура совокупность названий индивидуальных химических веществ, их групп и классов, а также правила составления их названий.Химическая номенклатура совокупность названий индивидуальных химических веществ, их групп и классов, а также правила составления их названий. Тривиальная (историческая) номенклатура связана с процессом получения веществ (пирогаллол – продукт пиролиза галловой кислоты), источника происхождения, из которого получали (муравьиная кислота) и т.д. Тривиальные названия соединений широко применяют в химии природных и гетероциклических соединений (цитраль, гераниол, тиофен, пиррол, хинолин, и др.).Тривиальная (историческая) номенклатура связана с процессом получения веществ (пирогаллол – продукт пиролиза галловой кислоты), источника происхождения, из которого получали (муравьиная кислота) и т.д. Тривиальные названия соединений широко применяют в химии природных и гетероциклических соединений (цитраль, гераниол, тиофен, пиррол, хинолин, и др.). В основе рациональной номенклатуры используется принцип деления органических соединений на гомологические ряды. Все вещества в определенном гомологическом ряду рассматриваются как производные самого простого представителя данного ряда – первого или иногда второго. В частности, у алканов – метана, у алкенов – этилена и т.д.В основе рациональной номенклатуры используется принцип деления органических соединений на гомологические ряды. Все вещества в определенном гомологическом ряду рассматриваются как производные самого простого представителя данного ряда – первого или иногда второго. В частности, у алканов – метана, у алкенов – этилена и т.д. 18

Международная номенклатура (IUPAC). Правила современной номенклатуры были разработаны в 1957 году на ХІХ конгрессе Международного союза теоретической и прикладной химии (International Union of Pure and Applied Chemistry – IUPAC). Радикально-функциональная номенклатура. В основе этих названий лежит название функционального класса (спирт, эфир, кетон и др.), которому предшествуют названия углеводородных радикалов, например: алилхлорид, диэтиловый эфир, диметилкетон, пропиловый спирт и т.д. Заместительная номенклатура. Правила номенклатуры. Родоначальная структура - структурный фрагмент молекулы (молекулярный остов), лежащий в основе названия соединения, главная углеродная цепь атомов для алициклических соединений, для карбоциклических – цикл. 19

Химическая связь в органических молекулах Химическая связь – явление взаимодействия внешних электронных оболочек (валентных электронов атомов) и ядер атомов, обуславливающее существование молекулы или кристалла как целого. Как правило атом, принимая, отдавая электрон или образуя общую электронную пару, стремится приобрести конфигурацию внешней электронной оболочки аналогичную инертным газам. Для органических соединений характерны следующие типы химических связей: - ионная связь -ковалентная связь -донорно - акцепторная связь -водородная связь Также существуют некоторые другие типы химической связи (металлическая, одноэлектронная, двухэлектронная трехцентровая), однако в органических соединениях они практически не встречаются. 20



Типы связей в органических соединениях Наиболее характерной для органических соединений является ковалентная связь. Ковалентная связь - это взаимодействие атомов, которое реализуется посредством образования общей электронной пары. Данный тип связи образуется между атомами, которые имеют сравнимые значения электроотрицательности. Электроотрицательность - свойство атома, показывающее способность оттягивать к себе электроны от других атомов. Ковалентная связь может быть полярной или неполярной. Неполярная ковалентная связь возникает между атомами с одинаковым значением электроотрицательности

Типы связей в органических соединениях Ковалентная полярная связь образуется между атомами, которые имеют различные значения электроотрицательности. В данном случае связанные атомы приобретают частичные заряды δ+δ+ δ-δ- Особым подтипом ковалентной связи является донорно- акцепторная связь. Как и в предыдущих примерах данный тип взаимодействия обусловлен наличием общей электронной пары, однако последняя предоставляется одним из атомов образующих связь (донором) и принимается другим атомом (акцептором) 24

Типы связей в органических соединениях Ионная связь образуется между атомами, которые сильно отличаются по значениям электроотрицательности. В данном случае электрон менее электроотрицательного элемента (зачастую это металл) полностью переходит к более электроотрицательному элементу. Данный переход электрона обуславливает появление положительного заряда у менее электроотрицательного атома и отрицательного у более электроотрицательного. Таким образом, образуется два иона с противоположным зарядом, между которыми существует электровалентное взаимодействие. 25

Типы связей в органических соединениях Водородная связь является электростатическим взаимодействием между атомом водорода, который связан сильнополярной связью, и электронными парами кислорода, фтора, азота, серы и хлора. Данный тип взаимодействия является довольно слабым взаимодействием. Водородная связь может быть межмолекулярной и внутримолекулярной. Межмолекулярная водородная связь (взаимодействие между двумя молекулами этилового спирта) Внутримолекулярная водородная связь в салициловом альдегиде 26

Химическая связь в органических молекулах Современная теория химической связи основывается на квантово-механической модели молекулы как системы, состоящей из электронов и атомных ядер. Краеугольным понятием квантово-механической теории является атомная орбиталь. Атомная орбиталь – часть пространства, в котором вероятность нахождения электронов является максимальной. Связь, таким образом, может быть рассмотрена как взаимодействие («перекрывание») орбиталей, которые несут по одному электрону с противоположными спинами. 27

Гибридизация атомных орбиталей Согласно квантово-механической теории, количество образованных атомом ковалентных связей определяется количеством одноэлектронных атомных орбиталей (количеством неспаренных электронов). У атома углерода в основном состоянии всего два неспаренных электрона, однако возможный переход электрона с 2s на 2 рz обуславливает возможность образования четырех ковалентных связей. Состояние атома углерода, при котором он имеет четыре неспаренных электрона называется «возбужденным». Несмотря на то, что орбитали углерода являются неравноценными, известно, что возможно образование четырех эквивалентных связей вследствие гибридизации атомных орбиталей. Гибридизация – явление, при котором из нескольких разных по форме и близких по энергии орбиталей образуется такое же количество одинаковых по форме и количеству орбиталей. 28



Гибридные состояния атома углерода в органических молекулах ПЕРВОЕ ГИБРИДНОЕ СОСТОЯНИЕ Атом С находится в состоянии sp 3 –гибридизации, образует четыре σ-связи, формирует четыре гибридные орбитали, которые располагаются в форме тетраэдра (валентный угол) σ–связь 31

Гибридные состояния атома углерода в органических молекулах ВТОРОЕ ГИБРИДНОЕ СОСТОЯНИЕ Атом С находится в состоянии sp 2 –гибридизации, образует три σ- связи, формирует три гибридные орбитали, которые располагаются в форме плоского треугольника (валентный угол 120) σ–связи π–связь 32

Гибридные состояния атома углерода в органических молекулах ТРЕТЬЕ ГИБРИДНОЕ СОСТОЯНИЕ Атом С находится в состоянии sp–гибридизации, образует две σ- связи, формирует две гибридные орбитали, которые располагаются в линию (валентный угол 180) σ–связи π–связи 33




Характеристики химических связей Шкала ПОЛИНГА: F-4,0; O – 3,5; Cl – 3,0; N – 3,0; Br – 2,8; S – 2,5; C-2,5; H-2,1. разница 1,7
Характеристики химических связей Поляризуемость связи - смещение электронной плотности под действием внешних факторов. Поляризуемость связи - степень подвижности электронов. С увеличением атомного радиуса возростает поляризуемость электронов. Поэтому поляризуемость связи Карбон - галоген увеличивается следующим образом: C-F

Электронные эффекты. Взаимное влияние атомов в молекуле 39 По современным теоретическим представлениям, реакционная способность органических молекул предопределена смещением и подвижностью электронных облаков, которые образуют ковалентную связь. В органической химии различают два типа смещений электронов: а) электронные смещения, происходящие в системе -связей, б) электронные смещения, передающиеся системой -связей. В первом случае имеет место так называемый индуктивный эффект, во втором - мезомерный. Индуктивный эффект - перераспределение электронной плотности (поляризация), возникающее в результате разницы электроотрицательности между атомами молекулы в системе -связей. Через незначительную поляризуемость -связей индуктивний эффект быстро угасает и через 3-4 связи он почти не проявляется.

Электронные эффекты. Взаимное влияние атомов в молекуле 40 Понятие об индуктивном эффекте было введено К. Ингольдом, им же были введены обозначения: –I-эффект в случае понижения заместителем электронной плотности +I-эффект в случае повышения заместителем электронной плотности Положительный индуктивний эффект проявляют алкильные радикалы (СН 3, С 2 Н 5 - и т.д.). Все другие заместители, связанные с атомом углерода, проявляют отрицательный индуктивный эффект.

Электронные эффекты. Взаимное влияние атомов в молекуле 41 Мезомерным эффектом называют перераспределение электронной плотности вдоль сопряженной системы. К сопряженным системам принадлежат молекулы органических соединений, в которых чередуются двойные и одинарные связи или когда рядом с двойной связью размещен атом, имеющий на р-орбитали неподеленную пару электронов. В первом случае имеет место, - сопряжение, а во втором – р, -сопряжение. Сопряженные системы бывают с открытой и замкнутой цепью сопряжения. Примером таких соединений является 1,3-бутадиен и бензин. В молекулах этих соединений атомы углерода находятся в состоянии sp 2 -гибридизации и за счет негибридных p-орбиталей образуют -связи, которые взаимно перекрываются между собой и формируют единственное электронное облако, то есть имеет место сопряжение.

Электронные эффекты. Взаимное влияние атомов в молекуле 42 Существует два вида мезомерного эффекта – положительный мезомерный эффект (+М) и отрицательный мезомерный эффект (-М). Положительный мезомерный эффект проявляют заместители, предоставляющие p-электроны в сопряженную систему. К таковым относят: -O, -S -NН 2, -ОН, -OR, Hal (галогены) и другие заместители, которые имеют отрицательный заряд или неподеленную пару электронов. Отрицательный мезомерный эффект характерен для заместителей оттягивающих на себя -электронную плотность из сопряженной системы. К таковым относят заместители, имеющие кратные связи между атомами с разной электроотрицательностью: - N0 2 ; -SO 3 Н; >С=О; -СООН и другие. Мезомерный эффект графически отражается согнутой стрелкой, которая показывает направление смещения электронов В отличие от индукционного эффекта, мезомерный эффект не погасает. Он передается полностью по системе, независимо от длины цепи сопряжения.
С=О; -СООН и другие. Мезомерный эффект графически отражается согнутой стрелкой, которая показывает направление смещения электронов В отличие от индукционного эффекта, мезомерный эффект не погасает. Он передается полностью по системе, независимо от длины цепи сопряжения.">

Типы химических реакций 43 Химическую реакцию можно рассматривать как взаимо- действие реагента и субстрата. В зависимости от способа разрыва и образования химической связи в молекулах, органические реакции делят на: а) гомолитические б) гетеролитические в) молекулярные Гомолитические или свободно-радикальные реакции обусловлены гомолитическим разрывом связи, когда у каждого атома остается по одному электрону, то есть образуются радикалы. Гомолитический разрыв проис- ходит при высоких температурах, действии кванта света или катализе.

Гетеролитические или ионные реакции протекают таким образом, что пара связующих электронов остается около одного из атомов и образуются ионы. Частица с электронной парой называется нуклеофи- льной и имеет отрицательный заряд (-). Частица без электронной пары называется электрофи- льной и имеет положительный заряд (+). 44 Типы химических реакций

Механизм химической реакции 45 Механизмом реакции называют совокупность элементарных (простых) стадий, из которых состоит данная реакция. Механизм реакции чаще всего включает такие стадии: активация реагента с образованием электрофила, нуклеофила или свободного радикала. Для активации реагента нужен, как правило, катализатор. Во второй стадии происходит взаимодействие активированного реагента с субстратом. При этом образуются промежуточные частицы (интермедиаты). К последним принадлежат -комплексы, -комплексы (карбокатионы), карбанионы, новые свободные радикалы. На конечной стадии проходит присоединение или отщепление к (от) образованному во второй стадии интермедиату какой-то частицы с формированием конечного продукта реакции. Если реагент при активации генерирует нуклеофил, то это - нуклеофильные реакции. Их помечают буквой N -(в индексе). В случае, когда реагент генерирует электрофил, реакции принадлежат к электрофильным (Е). Аналогично можно сказать и о свободнорадикальных реакциях (R).

Нуклеофилы – реагенты, имеющие отрицательный заряд или обогащенный электронной плотностью атом: 1) анионы: OH -, CN -, RO -, RS -, Hal - и другие анионы; 2) нейтральные молекулы с неподеленными парами электронов: NH 3, NH 2 R, H 2 O, ROH и другие; 3) молекулы с избыточной электронной плотностью (имеющие - связи). Электрофилы – реагенты, имеющие положительный заряд или обедненный электронной плотностью атом: 1) катионы: Н + (протон), НSO 3 + (ион гидрогенсульфония), NO 2 + (ион нитрония), NO (ион нитрозония) и другие катионы; 2) нейтральные молекулы, имеющие вакантную орбиталь: AlCl 3, FeBr 3, SnCl 4, BF 4 (кислоты Льюиса), SO 3 ; 3) молекулы с обедненной электронной плотностью на атоме. 46



49

50

51

52


Привет! Многие студенты медицинских вузов сейчас разбирают биоорганическую химию, она же – БОХ.
В некоторых вузах этот предмет заканчивается зачётом, в некоторых – экзаменом. Иногда бывает, что зачёт в одном вузе сравним по сложности с экзаменом в другом.
В моём университете биоорганическая химия сдавалась как раз экзаменом во время летней сессии в самый конец первого курса. Надо сказать, что БОХ относится к тем предметам, которые поначалу ужасают и могут вселять мысль — «это сдать невозможно». Особенно это конечно касается людей со слабой базой органической химии (а таких в медицинских университетах, как ни странно, довольно много).
Программы изучения биоорганической химии в разных университетах могут очень сильно отличаться, а методики преподавания – ещё сильнее.
Однако требования к студентам везде примерно одинаковые. Если очень упростить, то чтобы сдать биоорганическую химию на 5, вы должны знать названия, свойства, особенности строения и типичные реакции ряда органических веществ.
Наш преподаватель, уважаемый профессор, подавал материал так, будто бы каждый студент был самым лучшим в школе по органической химии (а биоорганическая химия по сути представляет собой усложнённый курс школьной органической химии). Наверное, он был прав в своём подходе, все должны тянуться наверх и стараться быть лучшими. Однако это привело к тому, что некоторые студенты, которые на первых 2-3 парах не понимали материал частично, ближе к середине семестра вообще перестали понимать всё.
Я решил написать этот материал по большей части из-за того, что я как раз и был таким студентом. В школе я очень любил неорганическую химию, а вот с органикой у меня всегда не складывалось. Я даже когда готовился к ЕГЭ, выбрал стратегию усиления всех своих знания по неорганике, в то же время закрепляя только базу органики. Мне кстати это чуть не вышло боком в плане вступительных баллов, но это другая история.
Я не зря сказал про методику преподавания, потому что у нас она была тоже весьма необычная. Нам сразу же, чуть ли не на первой паре, продемонстрировали методички, по которым мы должны были сдавать зачёты и затем экзамен.
Биоорганическая химия — зачёты и экзамен
Весь курс у нас делился на 4 крупных темы, каждая из которых заканчивалась зачётным занятием. Вопросы к каждому из четырёх зачётов у нас уже были с первых пар. Они, конечно же, пугали, однако в то же время они служили своеобразной картой, по которой следует двигаться.
Первый зачёт был совсем элементарный. Он был посвящён, в основном, номенклатуре, тривиальным (бытовым) и международным названиям, и, конечно же, классификации веществ. Также в том или ином виде затрагивались признаки ароматичности.
Второй зачёт после первого казался значительно более сложным. Там необходимо было расписывать свойства и реакции таких веществ, как кетоны, альдегиды, спирты, карбоновые кислоты. Например, одна из типичнейших реакций альдегидов — это реакция серебряного зеркала. Довольно красивое зрелище. Если к какому-либо альдегиду вы добавите реактив Толленса, то есть ОН, то на стенке пробирки вы увидите осадок, напоминающий зеркало, вот как это выглядит:
Третий зачёт на фоне второго не казался таким грозным. Все уже привыкли писать реакции и запоминать свойства по классификациям. В третьем зачёте речь шла о соединениях с двумя функциональными группами – аминофенолы, аминоспирты, оксокислоты и другими. Также в каждом билете был минимум один билет про углеводы.
Четвёртый зачёт по биоорганической химии был почти целиком и полностью посвящён белкам, аминокислотам и пептидным связям. Особой изюминкой были вопросы, на которых требовалось собрать РНК и ДНК.
Кстати, как раз вот так выглядит аминокислота — вы можете увидеть аминогруппу (она подкрашена жёлтым на этом рисунке) и группу карбоксильной кислоты (она сиреневая). Именно с веществами этого класса приходилось иметь дело в четвертом зачёте.
Каждый зачёт сдавался у доски – студент должен без подсказок расписать и пояснить все необходимые свойства в виде реакций. Например, если вы сдаёте второй зачёт, у вас в билете свойства спиртов. Вам преподаватель говорит – возьми пропанол. Вы пишете формулу пропанола и 4-5 типичных реакций, чтобы проиллюстрировать его свойства. Могла быть и экзотика, вроде серосодержащих соединений. Ошибка даже в индексе одного продукта реакции зачастую отправляла дальше учить этот материал до следующей попытки (которая была через неделю). Страшно? Сурово? Конечно!
Однако у такого подхода есть очень приятный побочный эффект. Во время регулярных семинарских занятий приходилось тяжко. Многие сдавали зачёты по 5-6 раз. Но зато на экзамене было очень легко, ведь каждый билет содержал 4 вопроса. Именно, по одному из каждого уже выученного и решённого зачёта.
Поэтому я даже не буду расписывать тонкости подготовки к экзамену по биоорганической химии. В нашем случае вся подготовка сводилась к тому, как мы готовились к самим зачётам. Уверенно сдал каждый из четырёх зачётов – перед экзаменом просто просмотри свои же черновики, распиши ещё самые основные реакции и сразу всё восстановится. Дело в том, что органическая химия — это очень логичная наука. Запоминать нужно не огромные строки реакций, а сами механизмы.
Да, отмечу, что это работает далеко не со всеми предметами. Грозную анатомию не получится сдать, просто почитав свои записи накануне. Ряд других предметов также имеет свои особенности. Даже если в вашем медицинском университете биоорганическая химия преподаётся как-то иначе, возможно, вам нужно будет скорректировать вашу подготовку и осуществлять её немного не так, как делал я. В любом случае, удачи вам, понимайте и любите науку!
Химия - наука о строении, свойствах веществ, их превращениях и сопровождающих явлениях.
Задачи:
1. Исследование строения вещества, развитие теории строения и свойств молекул и материалов. Важно установление связи между строением и разнообразными свойствами веществ и на этой основе построение теорий реакционной способности вещества, кинетики и механизма химических реакций и каталитических явлений.
2. Осуществление направленного синтеза новых веществ с заданными свойствами. Здесь также важно найти новые реакции и катализаторы для более эффективного осуществления синтеза уже известных и имеющих промышленное значение соединений.
3. Традиционная задача химии приобрела особое значение. Оно связано как с увеличением числа химических объектов и изучаемых свойств, так и с необходимостью определения и уменьшения последствий воздействия человека на природу.
Химия является общетеоретической дисциплиной. Она призвана дать студентам современное научное представление о веществе как одном из видов движущейся материи, о путях, механизмах и способах превращения одних веществ в другие. Знание основных химических законов, владение техникой химических расчетов, понимание возможностей, предоставляемых химией с помощью других специалистов, работающих в отдельных и узких ее областях, значительно ускоряют получение нужного результата в различных сферах инженерной и научной деятельности.
Химическая отрасль - одна из важнейших отраслей промышленности в нашей стране. Производимые ею химические соединения, различные композиции и материалы применяются повсюду: в машиностроении, металлургии, сельском хозяйстве, строительстве, электротехнической и электронной промышленности, связи, транспорте, космической технике, медицине, быту, и др. Главными направлениями развития современной химической промышленности являются: производство новых соединений и материалов и повышение эффективности существующих производств.
В медицинском вузе студенты изучают общую, биоорганическую, биологическую химию, а также клиническую биохимию. Знания студентами комплекса химических наук в их преемственности и взаимосвязи дают большую возможность, больший простор в исследовании и практическом использовании различных явлений, свойств и закономерностей, способствует развитию личности.
Специфическими особенностями изучения химических дисциплин в медицинском вузе являются:
· взаимозависимость между целями химического и медицинского образования;
· универсальность и фундаментальность данных курсов;
· особенность построения их содержания в зависимости от характера и общих целей подготовки врача и его специализации;
· единство изучения химических объектов на микро- и макроуровнях с раскрытием разных форм их химической организации как единой системы и проявляемых ею разных функций (химических, биологических, биохимических, физиологических и др.) в зависимости от их природы, среды и условий;
· зависимость от связи химических знаний и умений с реальной действительностью и практикой, в том числе медицинской, в системе «общество - природа - производство - человек», обусловленных неограниченными возможностями химии в создании синтетических материалов и их значением в медицине, развитием нанохимии, а также в решении экологических и многих других глобальных проблем человечества.
1. Взаимосвязь между процессами обмена веществ и энергии в организме
Процессы жизнедеятельности на Земле обусловлены в значительной мере накоплением солнечной энергии в биогенных веществах - белках, жирах, углеводах и последующими превращениями этих веществ в живых организмах с выделением энергии. Особенно отчетливо понимание взаимосвязи химических превращений и энергетических процессов в организме было осознано после работы А. Лавуазье (1743-1794) и П. Лапласа (1749- 1827). Они прямыми калориметрическими измерениями показали, что энергия, выделяемая в процессе жизнедеятельности, определяется окислением продуктов питания кислородом воздуха, вдыхаемым животными.
Обмен веществ и энергии - совокупность процессов превращения веществ и энергии, происходящих в живых организмах, и обмен веществами и энергией между организмом и окружающей средой. Обмен веществ и энергии является основой жизнедеятельности организмов и принадлежит к числу важнейших специфических признаков живой материи, отличающих живое от неживого. В обмене веществ, или метаболизме, обеспеченном сложнейшей регуляцией на разных уровнях, участвует множество ферментных систем. В процессе обмена поступившие в организм вещества превращаются в собственные вещества тканей и в конечные продукты, выводящиеся из организма. При этих превращениях освобождается и поглощается энергия.
С развитием в XIX-XX вв. термодинамики - науки о взаимопревращениях теплоты и энергий - стало возможно количественно рассчитывать превращение энергии в биохимических реакциях и предсказывать их направление.
Обмен энергии может осуществляться передачей теплоты или совершением работы. Однако живые организмы не находятся в равновесии с окружающей средой и поэтому могут быть названы неравновесными открытыми системами. Тем не менее при наблюдении в течение определенного отрезка времени в химическом составе организма видимых изменений не происходит. Но это не значит, что химические вещества, составляющие организм, не подвергаются никаким превращениям. Напротив, они постоянно и достаточно интенсивно обновляются, о чем можно судить по скорости включения в сложные вещества организма стабильных изотопов и радионуклидов, вводимых в клетку в составе более простых веществ-предшественников.
Между обменом веществ и обменом энергии существует одно принципиальное различие . Земля не теряет и не получает сколько-нибудь заметного количества вещества. Вещество в биосфере обменивается по замкнутому циклу и т.о. используется многократно. Обмен энергией осуществляется иначе. Она не циркулирует по замкнутому циклу, а частично рассеивается во внешнее пространство. Поэтому для поддержания жизни на Земле необходим постоянный приток энергии Солнца. За 1 год в процессе фотосинтеза на земном шаре поглощается около 10 21 кал солнечной энергии. Хотя она составляет лишь 0,02% всей энергии Солнца, это неизмеримо больше, чем та энергия, которая используется всеми машинами, созданными руками человека. Столь же велико количество участвующего в кругообороте вещества.
2. Химическая термодинамика как теоретическая основа биоэнергетики. Предмет и методы химической термодинамики
Химическая термодинамика изучает переходы химической энергии в другие формы - тепловую, электрическую и т. п., устанавливает количественные законы этих переходов, а также направление и пределы самопроизвольного протекания химических реакций при заданных условиях.
Термодинамический метод основан на ряде строгих понятий: «система», «состояние системы», «внутренняя энергия системы», «функция состояния системы».
Объектом изучения в термодинамике является система
Одна и та же система может находиться в различных состояниях. Каждое состояние системы характеризуется определенным набором значений термодинамических параметров. К термодинамическим параметрам относятся температура, давление, плотность, концентрация и т. п. Изменение хотя бы только одного термодинамического параметра приводит к изменению состояния системы в целом. Термодинамическое состояние системы называют равновесным, если оно характеризуется постоянством термодинамических параметров во всех точках системы и не изменяется самопроизвольно (без затраты работы).
Химическая термодинамика изучает систему в двух равновесных состояниях (конечном и начальном) и на этом основании определяет возможность (или невозможность) самопроизвольного течения процесса при заданных условиях в указанном направлении.
Термодинамика изучает взаимные превращения различных видов энергии, связанные с переходом энергии между телами в форме теплоты и работы. Термодинамика базируется на двух основных законах, получивших название первого и второго начал термодинамики. Предметом изучения в термодинамике является энергия и законы взаимных превращений форм энергии при химических ре акциях, процессах растворения, испарения, кристаллизации.
Хими́ческая термодина́мика - раздел физической химии, изучающий процессы взаимодействия веществ методами термодинамики.
Основными направлениями химической термодинамики являются:
Классическая химическая термодинамика, изучающая термодинамическое равновесие вообще.
Термохимия, изучающая тепловые эффекты, сопровождающие химические реакции.
Теория растворов, моделирующую термодинамические свойства вещества исходя из представлений о молекулярном строении и данных о межмолекулярном взаимодействии.
Химическая термодинамика тесно соприкасается с такими разделами химии, как аналитическая химия; электрохимия; коллоидная химия; адсорбция и хроматография.
Развитие химической термодинамики шло одновременно двумя путями: термохимическим и термодинамическим.
Возникновением термохимии как самостоятельной науки следует считать открытие Германом Ивановичем Гессом, профессором Петербургского университета, взаимосвязи между тепловыми эффектами химических реакций ---законы Гесса.
3. Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные. Понятие о фазе.
Система – это совокупность взаимодействующих веществ, мысленно или фактически обособленная от окружающей среды (пробирка, автоклав).
Химическая термодинамика рассматривает переходы из одного состояния в другое, при этом могут изменяться или оставаться постоянными некоторые параметры :
· изобарические – при постоянном давлении;
· изохорические – при постоянном объеме;
· изотермические – при постоянной температуре;
· изобарно - изотермические – при постоянном давлении и температуре и т.д.
Термодинамические свойства системы можно выразить с помощью нескольких функций состояния системы , называемых характеристическими функциями : внутреннейэнергииU , энтальпии H , энтропии S , энергии Гиббса G , энергии Гельмгольца F . Характеристические функции обладают одной особенностью: они не зависят от способа (пути) достижения данного состояния системы. Их значение определяется параметрами системы (давлением, температурой и др.) и зависит от количества или массы вещества, поэтому принято относить их к одному молю вещества.
По способу передачи энергии, вещества и информации между рассматриваемой системы и окружающей средой термодинамические системы классифицируются:
1. Замкнутая (изолированная) система - это система в которой нет обмена с внешними телами ни энергией, ни веществом (в том числе и излучением) , ни информацией.
2. Закрытая система - система в которой есть обмен только с энергией.
3. Адиабатно изолированная система - это система в которой есть обмен энергией только в форме теплоты.
4. Открытая система - это система, которая обменивается и энергией, и веществом, и информацией.
Классификация систем
:
1) по возможности тепло- и массообмена: изолированные, закрытые, открытые. Изолированная система не обменивается с окружающей средой ни веществом, ни энергией. Закрытая система обменивается с окружающей средой энергией, но не обменивается веществом. Открытая система обменивается с окружающей средой и веществом и энергией. Понятие изолированной системы используется в физической химии как теоретическое.
2) по внутренней структуре и свойствам: гомогенные и гетерогенные. Гомогенной называется система, внутри которой нет поверхностей, делящих систему на части, различные по свойствам или химическому составу. Примерами гомогенных систем являются водные растворы кислот, оснований, солей; смеси газов; индивидуальные чистые вещества. Гетерогенные системы содержат внутри себя естественные поверхности. Примерами гетерогенных систем являются системы, состоящие из различных по агрегатному состоянию веществ: металл и кислота, газ и твёрдое вещество, две нерастворимые друг в друге жидкости.
Фаза
– это гомогенная часть гетерогенной системы, имеющая одинаковый состав, физические и химические свойства, отделённая от других частей системы поверхностью, при переходе через которую свойства системы меняются скачком. Фазы бывают твёрдые, жидкие и газообразные. Гомогенная система всегда состоит из одной фазы, гетерогенная – из нескольких. По числу фаз системы классифицируются на однофазные, двухфазные, трёхфазные и т.д.
5.Первое начало термодинамики. Внутренняя энергия. Изобарный и изохорный тепловые эффекты .
Первое начало термодинамики - один из трёх основных законов термодинамики, представляет собой закон сохранения энергии для термодинамических систем.
Первое начало термодинамики было сформулировано в середине XIX века в результате работ немецкого учёного Ю. Р. Майера, английского физика Дж. П. Джоуля и немецкого физика Г. Гельмгольца.
Согласно первому началу термодинамики, термодинамическая система может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии .
Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника. Процесс, протекающий при постоянной температуре, называется изотермическим , при постоянном давлении - изобарическим , при постоянном объеме – изохорическим. Если во время процесса система изолирована от внешней среды таким образом, что исключен теплообмен со средой, процесс называют адиабатическим.
Внутренняя энергия системы. При переходе системы из одного состояния в другое изменяются некоторые ее свойства, в частности внутренняя энергия U.
Внутренняя энергия системы представляет собой ее полную энергию, которая складывается из кинетической и потенциальной энергий молекул, атомов, атомных ядер и электронов. Внутренняя энергия включает в себя энергию поступательного, вращательного и колебательного движений, а также потенциальную энергию, обусловленную силами притяжения и отталкивания, действующими между молекулами, атомами и внутриатомными частицами. Она не включает потенциальную энергию положения системы в пространстве и кинетическую энергию движения системы как целого.
Внутренняя энергия является термодинамической функцией состояния системы. Это значит, что всякий раз, когда система оказывается в данном состоянии, ее внутренняя энергия принимает определенное присущее этому состоянию значение.
∆U = U 2 - U 1
где U 1 и U 2 - внутренняя энергия системы в конечном и начальном состояниях cсоответственно.
Первый закон термодинамики. Если система обменивается с внешней средой тепловой энергией Q и механической энергией (работой) А, и при этом переходит из состояния 1 в состоянии 2, количество энергии, которое выделится или поглощается системой форм теплоты Q или работой А равно полной энергии системы при переходе из одного состояния в другое и записывается.
Биоорганическая химия. Тюкавкина Н.А., Бауков Ю.И.

3-е изд., перераб. и доп. - М.: 2004 - 544 с.
Основная особенность учебника - сочетание медицинской направленности этого химического курса, необходимого для студентов-медиков, с его высоким, фундаментальным научным уровнем. В учебник включен базисный материал по строению и реакционной способности органических соединений, в том числе биополимеров, являющихся структурными компонентами клетки, а также основных метаболитов и низкомолекулярных биорегуляторов. В третьем издании (2-е - 1991 г.) особое внимание уделено соединениям и реакциям, имеющим аналогии в живом организме, усилен акцент на освещение биологической роли важных классов соединений, расширен спектр современных сведений экологического и токсикологического характера. Для студентов вузов, обучающихся по специальностям 040100 Лечебное дело, 040200 Педиатрия, 040300 Медико-профилактическое дело, 040400 Стоматология.
Формат: pdf
Размер: 15 Мб
Смотреть, скачать: drive.google
СОДЕРЖАНИЕ
Предисловие...................... 7
Введение......................... 9
Часть I
ОСНОВЫ СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Глава 1. Общая характеристика органических соединений 16
1.1. Классификация. "................ 16
1.2. .Номенклатура... ............ 20
1.2.1. Заместительная номенклатура........... 23
1.2.2. Радикально-функциональная номенклатура........ 28
Глава 2. Химическая связь и взаимное влияние атомов в органических
соединениях.................. 29
2.1. Электронное строение элементов-органогенов...... 29
2.1.1. Атомные орбитали................ 29
2.1.2. Гибридизация орбиталей............. 30
2.2. Ковалентные связи............... 33
2.2.1. а- и л-Связи.................. 34
2.2.2. Донорно-акцепторные связи............ 38
2.2.3. Водородные связи............... 39
2.3. Сопряжение и ароматичность............ 40
2.3.1. Системы с открытой цепью сопряжения... ,..... 41
2.3.2. Системы с замкнутой цепью сопряжения........ 45
2.3.3. Электронные эффекты.............. 49
Глава 3. Основы строения органических соединений....... 51
3.1. Химическое строение и структурная изомерия...... 52
3.2. Пространственное строение и стереоизомерия...... 54
3.2.1. Конфигурация................. 55
3.2.2. Конформация................. 57
3.2.3. Элементы симметрии молекул............ 68
3.2.4. Эиантиомерия............... 72
3.2.5. Диастереомерия................
3.2.6. Рацематы.................. 80
3.3. Энантиотопия, диастереотопия. . ......... 82
Глава 4 Общая характеристика реакций органических соединений 88
4.1. Понятие о механизме реакции..... 88
3
11.2. Первичная структура пептидов и белков........ 344
11.2.1. Состав и аминокислотная последовательность...... 345
11.2.2. Строение и синтез пептидов............ 351
11.3. Пространственное строение полипептидов и белков.... 361
Глава 12. Углеводы.................... 377
12.1. Моносахариды................. 378
12.1.1. Строение и стереоизомерия............. 378
12.1.2. Таутомерия..............." . 388
12.1.3. Конформации................. 389
12.1.4. Производные моносахаридов............ 391
12.1.5. Химические свойства............... 395
12.2. Дисахариды.................. 407
12.3. Полисахариды................. 413
12.3.1. Гомополисахариды............... 414
12.3.2. Гетерополисахариды............... 420
Глава 13. Нуклеотиды и нуклеиновые кислоты..........431
13.1. Нуклеозиды и нуклеотиды............. 431
13.2. Структура нуклеиновых кислот........... 441
13.3 Нуклеозидполифосфаты. Никотинамнднуклеотиды..... 448
Глава 14. Липиды и низкомолекулярные биорегуляторы...... 457
14.1. Омыляемые липиды............... 458
14.1.1. Высшие жирные кислоты - структурные компоненты омыля-емых липидов 458
14.1.2. Простые липиды................ 461
14.1.3. Сложные липиды................ 462
14.1.4. Некоторые свойства омыляемых липидов и их структурных компонентов 467
14.2. Неомыляемые липиды 472
14.2.1. Терпены.......... ...... 473
14.2.2. Низкомолекулярные биорегуляторы липидной природы. . . 477
14.2.3. Стероиды................... 483
14.2.4. Биосинтез терпенов и стероидов........... 492
Глава 15. Методы исследования органических соединений...... 495
15.1. Хроматография................. 496
15.2. Анализ органических соединений. . ........ 500
15.3. Спектральные методы............... 501
15.3.1. Электронная спектроскопия............. 501
15.3.2. Инфракрасная спектроскопия............ 504
15.3.3. Спектроскопия ядерного магнитного резонанса...... 506
15.3.4. Электронный парамагнитный резонанс......... 509
15.3.5. Масс-спектрометрия............... 510
Предисловие
На протяжении многовековой истории развития естествознания установилась тесная
взаимосвязь между- медициной и химией. Происходящее в настоящее время глубокое
взаимопроникновение этих наук приводит к появлению новых научных направлений,
изучающих молекулярную природу отдельных физиологических процессов, молекулярные
основы патогенеза болезней, молекулярные аспекты фармакологии и т. п.
Необходимость познания процессов жизнедеятельности на молекулярном уровне
объяснима, «ибо живая клетка - настоящее царство больших и малых молекул,
непрерывно взаимодействующих, возникающих и исчезающих»*.
Биоорганическая химия изучает биологически значимые вещества и может служить
«молекулярным инструментом» при разностороннем исследовании компонентов клетки.
Биоорганическая химия играет важную роль в развитии современных областей
медицины и является неотъемлемой частью естественнонаучного образования врача.
Прогресс медицинской науки и улучшение здравоохранения связаны с глубокой
фундаментальной подготовкой специалистов. Актуальность такого подхода во многом
определяется превращением медицины в крупную отрасль социальной сферы, в поле
зрения которой находятся проблемы экологии, токсикологии, биотехнологии и т. д.
Ввиду отсутствия в учебных планах медицинских вузов общего курса органической
химии в настоящем учебнике отводится определенное место основам органической
химии, необходимым для усвоения биоорганической химии. При подготовке третьего
издания (2-е - 1992 г.) материал учебника переработан и еще более приближен к
задачам восприятия медицинских знаний. Расширен круг соединений и реакций,
имеющих аналогии в живых организмах. Большее внимание уделено сведениям
экологического и токсикологического характера. Некоторому сокращению подверглись
элементы сугубо химического характера, не имеющие принципиального значения для
медицинского образования, в частности, способы получения органических
соединений, свойства ряда отдельных представителей и т. п. Вместе с тем
расширены разделы, включающие материал о взаимосвязи между структурой
органических веществ и их биологическим действием как молекулярной основы
действия лекарственных средств. Улучшена структура учебника, в отдельные рубрики
вынесен химический материал, имеющий специальное медико-биологическое значение.
Авторы выражают искреннюю благодарность профессорам С. Э. Зурабяну, И. Ю.
Белавину, И. А. Селивановой, а также всем коллегам за полезные советы и помощь в
подготовке рукописи к переизданию.